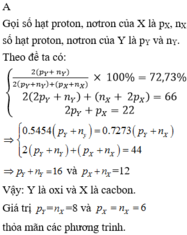1 hợp chất có công thức XY2 , trong đó X chiếm 50% về khối lượng , trong hạt nhân của X và Y đù có số proton bằng số notron . Tổng số proton trong XY2 là 32 : a) viết cấu hình electron của X và Y ; b) viết công thức phân tử XY2 và công thức cấu tạo

Những câu hỏi liên quan
Một hợp chất có công thức XY2 trong đó X chiếm 50% về khối lượng. Trong hạt nhân của X và Y đều có số proton bằng số nơtron. Tổng số proton trong phân tử XY2 là 32. Viết cấu hình electron của X. A. 1s22s22p63s23p4 B. 1s22s22p4 C. 1s22s22p63s2 D.1s22s22p63s23p2
Đọc tiếp
Một hợp chất có công thức XY2 trong đó X chiếm 50% về khối lượng. Trong hạt nhân của X và Y đều có số proton bằng số nơtron. Tổng số proton trong phân tử XY2 là 32. Viết cấu hình electron của X.
A. 1s22s22p63s23p4
B. 1s22s22p4
C. 1s22s22p63s2
D.1s22s22p63s23p2
Đáp án A.
Gọi số hạt proton, nơtron, electron của nguyên tử X là p, n, e và của Y là p’, n’, e’.
Theo bài : p = n = e và p’ = n’ = e’.
Trong hợp chất XY2, X chiếm 50% về khối lượng nên:
M X 2 M Y = 50 50 ⇒ p + n 2 ( p ' + n ' ) = 1 ⇒ p = 2 p '
Tổng số proton trong phân tử XY2 là 32 nên p + 2p’ = 32.
Từ đây tìm được: p = 16 (S) và p’ = 8 (O). Hợp chất cần tìm là SO2.
Cấu hình electron của S: 1s22s22p63s23p4
Đúng 0
Bình luận (0)
Một hợp chất có công thức XY2 trong đó X chiếm 50% về khối lượng. Trong hạt nhân của X và Y đều có số proton bằng số nơtron. Tổng số proton trong phân tử XY2 là 32.Cấu hình electron của X và Y A. X: 1s22s22p63s23p4 và Y: 1s22s22p4 B. X: 1s22s22p63s23p3 và Y: 1s22s22p4 C. X: 1s22s22p63s23p6 và Y: 1s22s22p4 D. X: 1s22s22p63s23p4 và Y: 1s22s22p6
Đọc tiếp
Một hợp chất có công thức XY2 trong đó X chiếm 50% về khối lượng. Trong hạt nhân của X và Y đều có số proton bằng số nơtron. Tổng số proton trong phân tử XY2 là 32.Cấu hình electron của X và Y
A. X: 1s22s22p63s23p4 và Y: 1s22s22p4
B. X: 1s22s22p63s23p3 và Y: 1s22s22p4
C. X: 1s22s22p63s23p6 và Y: 1s22s22p4
D. X: 1s22s22p63s23p4 và Y: 1s22s22p6
Đáp án A
Gọi số hạt prroton, nơtron, electron của nguyên tử X là P, N, E và của Y là P’, N’, E’
Theo bài: P = N = E và P’ = N’ = E’
Trong hợp chất XY2, X chiếm 50% về khối lượng nên: ![]() = 1 « P = 2P’
= 1 « P = 2P’
Tổng số proton trong phân tử XY2 là 32 nên P + 2P’ = 32
Từ đây tìm được: P = 16 (S) và P’ = 8 (O)
Hợp chất cần tìm là SO2
Cấu hình electron của S: 1s22s22p63s23p4 và của O: 1s22s22p4
Đúng 0
Bình luận (0)
Một hợp chất có công thức XY2 trong đó X chiếm 50% về khối lượng. Trong hạt nhân của X và Y đều có số proton bằng số nơtron. Tổng số proton trong phân tử XY2 là 32. Cấu hình electron phù hợp với X và Y là: A. X : 1s22s22p63s23p4, Y: 1s22s22p4 B. X : 1s22s22p63s2, Y: 1s22s22p4 C. X : 1s22s22p63s23p4, Y: 1s22s22p2 D. X : 1s22s22p63s23p2, Y: 1s22s22p6
Đọc tiếp
Một hợp chất có công thức XY2 trong đó X chiếm 50% về khối lượng. Trong hạt nhân của X và Y đều có số proton bằng số nơtron. Tổng số proton trong phân tử XY2 là 32. Cấu hình electron phù hợp với X và Y là:
A. X : 1s22s22p63s23p4, Y: 1s22s22p4
B. X : 1s22s22p63s2, Y: 1s22s22p4
C. X : 1s22s22p63s23p4, Y: 1s22s22p2
D. X : 1s22s22p63s23p2, Y: 1s22s22p6
Đáp án A.
Gọi số hạt proton, nơtron, electron của nguyên tử X là p, n, e và của Y là p’, n’, e’.
Theo bài : p = n = e và p’ = n’ = e’.
Trong hợp chất XY2, X chiếm 50% về khối lượng nên:
![]()
Tổng số proton trong phân tử XY2 là 32 nên p + 2p’ = 32.
Từ đây tìm được: p = 16 (S) và p’ = 8 (O). Hợp chất cần tìm là SO2.
Cấu hình electron của S: 1s22s22p63s23p4 và của O: 1s22s22p4.
Đúng 0
Bình luận (0)
Một hợp chất có công thức
X
Y
2
trong đó Y chiếm 50% về khối lượng. Trong hạt nhân của X có n p và hạt nhân Y có n’ p’. Tổng số proton trong phân tử
X
Y
2
là 32. Cấu hình electron của X và Y và liên kết trong phân tử
X
Y
2
là A.
3
s
2
3
p...
Đọc tiếp
Một hợp chất có công thức X Y 2 trong đó Y chiếm 50% về khối lượng. Trong hạt nhân của X có n = p và hạt nhân Y có n’ = p’. Tổng số proton trong phân tử X Y 2 là 32. Cấu hình electron của X và Y và liên kết trong phân tử X Y 2 là
A. 3 s 2 3 p 4 , 2 s 2 2 p 4 và liên kết cộng hóa trị
B. 3 s 2 , 2 s 2 2 p 5 và liên kết ion
C. 3 s 2 3 p 5 , 4 s 2 và liên kết ion
D. 3 s 2 3 p 3 , 2 s 2 2 p 3 và liên kết cộng hóa trị
Chọn A
Y chiếm 50% về khối lượng → MX = 2MY → nX + pX = 2 nY + 2 pY (1)
nX = pX; nY = pY (2)
pX + 2pY = 32 (3)
→ pX = 16 (S): [Ne]3s23p4; pY = 8 (O): [He]2s22p4
Liên kết trong phân tử SO2 là liên kết cộng hóa trị.
Đúng 1
Bình luận (0)
Hợp chất A có công thức là XY2 ; trong đó tổng số hạt proton, notron, electron là 66; .Hạt mang điện của X,Y hơn kém nhau 20 hạt. Trong hạt nhân của nguyên tử X và Y đều có số hạt mang điện bằng số hạt không mang điện. Tìm công thức hóa học của A.
Gọi m,n,p,q lần lượt số p và số n của X,Y (m,n,p,q:nguyên, dương)
=> 2m+n+4p+2q= 66 (1)
Mặt khác, số hạt mang điện X,Y hơn kém nhau 20 hạt:
=> 2m - 2p = 20 (2)
Tiếp theo, hạt nhân X,Y có số hạt không mang điện bằng số hạt mang điện:
=> m=n (3); p=q(4)
Từ (1), (2), (3), (4) ta lập hệ pt 4 ẩn giải ra được:
=> m=14; n=14; p=4;q=4
=> ZX=14 => X là Silic
=> ZY= 4 => Y là Beri
=> A: SiBe2 (thường viết là Be2Si nhiều hơn)
Đúng 1
Bình luận (0)
Hợp chất Z được tạo bởi hai nguyên tố X và Y có công thức X Y 2 trong đó Y chiếm 72,73% về khối lượng. Biết rằng trong phân tử Z, tổng số hạt (proton, nơtron, electron) là 66, số proton là 22. Nguyên tố Y là
A. cacbon
B. oxi
C. lưu huỳnh
D. magie
Hợp chất A có công thức MX2 trong đó M chiếm 46,67% về khối lượng. Trong hạt nhân M có số notron nhiều hơn số hạt proton là 4 hạt. Trong hạt nhân X, số notron bằng số proton. Tổng số proton trong MX2 là 58 hạt. Công thức của MX2 là A. FeS2 B. FeCl2 C. CuCl2 D. SO2
Đọc tiếp
Hợp chất A có công thức MX2 trong đó M chiếm 46,67% về khối lượng. Trong hạt nhân M có số notron nhiều hơn số hạt proton là 4 hạt. Trong hạt nhân X, số notron bằng số proton. Tổng số proton trong MX2 là 58 hạt. Công thức của MX2 là
A. FeS2
B. FeCl2
C. CuCl2
D. SO2
Tổng số proton trong MX2 là 58 hạt → ZM + 2.ZX = 58
Trong hạt nhân M có số notron nhiều hơn số hạt proton là 4 hạt → -ZM + NM = 4
Trong hạt nhân X, số notron bằng số proton → ZX = NX
MA =ZM + NM + 2.ZX + 2.NX = (ZM + 2.ZX ) + NM + 2NX= 58 + NM + 58 - ZM = 116 + NM- ZM
M chiếm 46,67% về khối lượng → ZM + NM =
7
15
. (116 + NM- ZM ) → 22ZM + 8NM = 812
Ta có hệ
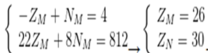
M là Fe
→ ZX =
58
-
26
2
= 16 → X là S
Công thức của A là FeS2.
Đáp án A.
Đúng 0
Bình luận (0)
Hợp chất A có công thức MX2 trong đó M chiếm 46,67% về khối lượng. Trong hạt nhân M có số notron nhiều hơn số hạt proton là 4 hạt. Trong hạt nhân X, số notron bằng số proton. Tổng số proton trong MX2 là 58 hạt. Công thức của MX2 là A. FeS2 B. FeCl2 C. CuCl2 D. SO2
Đọc tiếp
Hợp chất A có công thức MX2 trong đó M chiếm 46,67% về khối lượng. Trong hạt nhân M có số notron nhiều hơn số hạt proton là 4 hạt. Trong hạt nhân X, số notron bằng số proton. Tổng số proton trong MX2 là 58 hạt. Công thức của MX2 là
A. FeS2
B. FeCl2
C. CuCl2
D. SO2
Đáp án A
Tổng số proton trong MX2 là 58 hạt → ZM + 2.ZX = 58
Trong hạt nhân M có số notron nhiều hơn số hạt proton là 4 hạt → -ZM + NM = 4
Trong hạt nhân X, số notron bằng số proton → ZX = NX
MA =ZM + NM + 2.ZX + 2.NX = (ZM + 2.ZX ) + NM + 2NX
= 58 + NM + 58 - ZM = 116 + NM - ZM
M chiếm 46,67% về khối lượng
![]()
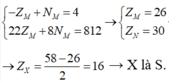
=> M là Fe
Đúng 0
Bình luận (0)
Hợp chất H có công thức MX2 trong đó M chiếm 140/3% về khối lượng, X là phi kim ở chu kỳ 3, trong hạt nhân của M có số proton ít hơn số nơtron là 4; trong hạt nhân của X có số proton bằng số nơtron. Tổng số proton trong 1 phân tử A là 58. Cấu hình electron ngoài cùng của M là. A. 3d104s1. B. 3s23p4. C. 3d64s2. D. 2s22p4.
Đọc tiếp
Hợp chất H có công thức MX2 trong đó M chiếm 140/3% về khối lượng, X là phi kim ở chu kỳ 3, trong hạt nhân của M có số proton ít hơn số nơtron là 4; trong hạt nhân của X có số proton bằng số nơtron. Tổng số proton trong 1 phân tử A là 58.
Cấu hình electron ngoài cùng của M là.
A. 3d104s1.
B. 3s23p4.
C. 3d64s2.
D. 2s22p4.
Đáp án C
Tổng số proton trong MX2 là 58 hạt
→ ZM + 2.ZX = 58
Trong hạt nhân M có số notron nhiều hơn số hạt proton là 4 hạt
→ -ZM + NM = 4
Trong hạt nhân X, số notron bằng số proton → ZX = NX
MA =ZM + NM + 2.ZX + 2.NX
= (ZM + 2.ZX ) + NM + 2NX
= 58 + NM + 58 - ZM = 116 + NM- ZM
M chiếm 46,67% về khối lượng
![]()
![]()
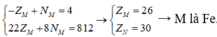
![]()
Cấu hình electron của M là [Ar]3d64s2.
Đúng 0
Bình luận (0)