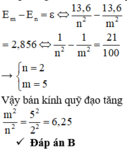Câu 15
a) Hãy xây dựng phương trình schrodinger cho nguyên tử He ở trạng thái dừng
b) Giải phương trình đó, với giả thiết năng lượng đẩy giữa 2 electron bị bỏ qua.
Nguyên tử hiđrô ở trạng thái cơ bản va chạm với một electron có năng lượng 13,2 (eV). Trong quá trình tương tác giả sử nguyên tử đứng yên và chuyển lên trạng thái kích thích thứ ba. Tìm động năng còn lại của electron sau va chạm. Biết các mức năng lượng của nguyên tử hiđrô ở trạng thái dừng được xác định bằng công thức: E n = - 13 , 6 / n 2 e V với n là số nguyên.
A. 0,45 eV.
B. 0,51 eV.
C. 1,11 eV.
D. 0,16 eV.
Năng lượng của nguyên tử hiđrô ở các trạng thái dừng được xác định bằng công thức: E n = − 13 , 6 n 2 e V , với n = 1, 2, 3,... ứng với trạng thái dừng có electron chuyển động trên quỹ đạo K, L, M,... Năng lượng ion hóa (năng lượng cần thiết để biến nguyên tử trung hòa về điện thành ion dương) của nguyên tử hiđrô khi nó đang ở trạng thái cơ bản là bao nhiêu ? Lấy e = 1 , 6 . 10 - 19 C
A. 2 , 024 . 10 - 18 J
B. 1 , 476 . 10 - 18 J
C. 4 , 512 . 10 - 18 J
D. 2 , 176 . 10 - 18 J
Một phôtôn có năng lượng 1,79 eV bay qua hai nguyên tử có mức kích thích 1,79 eV nằm trên cùng phương với phôtôn tới. Các nguyên tử này có thể ở trạng thái cơ bản hoặc trạng thái kích thích. Gọi x là số phôtôn có thể thu được sau đó, theo phương của phôtôn tới. Hãy chỉ ra đáp số sai.
A. x = 3
B. x = 0
C. x = 1
D. x = 2
Trong trường hợp đối với nguyên tử hidro hãy xác định các đại lượng sau: a. Năng lượng kích thích dùng để chuyển electron từ trạng thái cơ bản lên trạng thái có n = 3. b. Năng lượng ion hóa (để tách electron ở trạng thái cơ bản tới xa vô cùng). c. Bước sóng của bức xạ khi electron chuyển từ n =3 về n=2.
Cho gốc hydrocacbon có cấu tạo: CH2=CH-CH=CH.
a) Xây dựng hệ phương trình thế kỷ cho gốc hydrocacbon trên.
b) Tìm năng lượng và hàm sóng.
c) Xây dựng giản đồ năng lượng.
d) Tính mật độ electron pi, bậc liên kết, chỉ số hóa trị tự do. Xây dựng khung phân tử và nhận xét về khả năng phản ứng.
a. Theo phương pháp MO-Huckel. Ta dễ dàng xđ đc định thức thế kỷ:
D = \(\begin{matrix}x&1&0&0\\1&x&1&0\\0&1&x&1\\0&0&1&x\end{matrix}\)=> hệ phương trình thế kỷ : \(\begin{cases}xC_1+C_2=0\\C_1+xC_2+C_3=0\\C_2+xC_3+C_4=0\\C_3+xC_4=0\end{cases}\)
b. D = 0 \(\Leftrightarrow\)D= x4-3x2+1 = 0 \(\Leftrightarrow\begin{cases}x_1=-1,618\\x_2=-0,618\\x_3=0,618\\x_4=1,618\end{cases}\)
Thay các giá trị x1,x2,x3,x4 vào biểu thức tính năng lượng \(E=\alpha-x\beta\) ta sẽ thu đc 4 mức năng lượng electron \(\pi\).
\(\begin{cases}E_1=\alpha+1,618\beta\\E_2=\alpha+0,618\beta\\E_3=\alpha-0,618\beta\\E_4=\alpha-1,618\beta\end{cases}\)
ta có \(\psi=c_1\phi_1+c_2\phi_2+c_3\phi_3+c_4\phi_4\)
để xác định các hàm \(\psi\) ta phải tìm các hệ số ci trong biểu thức.
thay x1= -1,618 vào hệ phương trình thế kỷ ta được : \(\begin{cases}c_2=1,618c_1\\c_1+c_3=1,618c_2\\c_2+c_4=1,618c_3\\c_3=1,618c_4\end{cases}\)\(\Rightarrow\begin{cases}c_1=c_4\\c_2=c_3\end{cases}\)
kết hợp với điều kiện chuẩn hóa c12+c22+c32+c42=1 ta đc: c1=c4=0,372 và c2=c3=0,602
vậy khi x1= -1,618 ta có hàm MO tương ứng là: \(\psi_1=0.372\phi_1+0.602\phi_2+0.602\phi_3+0.372\phi_4\)
Làm tương tự với x2,x3,x4 ta sẽ thu đc \(\psi_2,\psi_3,\psi_4\)
Vậy 4 MO là : \(\begin{cases}\psi_1=0.372\phi_1+0.602\phi_2+0.602\phi_3+0.372\phi_4\\\psi_2=0.602\phi_1+0.372\phi_2-0.372\phi_3-0.602\phi_4\\\psi_3=0.602\phi_1-0.372\phi_2-0.372\phi_3+0.602\phi_4\\\psi_4=0.372\phi_1-0.602\phi_2+0.602\phi_3-0.372\phi_4\end{cases}\)
a) Hãy cho biết các luận điểm của phương pháp MO?
b) MO là gì?
c) Thiết lập phương trình Schrodinger cho phân tử H2 theo pp MO-LCAO?
câu trả lời quá mờ không nhìn thấy được, bạn nên ghi rõ câu trả lời hoặc gõ trực tiếp vào website.
a, - Phân tử - tổ hợp thống nhất gồm các hạt nhân và các e của các nguyên tử tương tác.
- Trạng thái của e được mô tả bằng các MO. Mỗi MO được xác định gần đúng bằng phương pháp tổ hợp tuyến tính các orbital nguyên tử
- Số MO tạo thành bằng số AO tham gia tổ hợp tuyến tính.
b, MO là một hàm sóng, biểu thị trạng thái chuyển động của từng e trong phân tử.
Năng lượng nguyên tử hiđrô gồm động năng của electron và thế năng của tương tác Cu-lông giữa hạt nhân và electron. Hãy tìm biểu thức năng lượng trạng thái dừng En theo r0. Cho biết r0 là bán kính quỹ đạo Bo.
A. 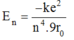
B. 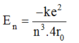
C. 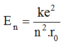
D. 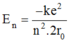
Đáp án: D
Năng lượng trạng thái dừng gồm động năng của electron và thế năng của tương tác Cu-lông:
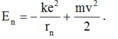
Do lực Cu-lông là lực hướng tâm nên:
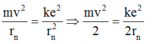
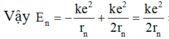
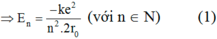
Các mức năng lượng của trạng thái dừng của nguyên tử hiđrô được xác định bằng biểu thức E n = − 13 , 6 n 2 e V (với n = 1, 2, 3,…). Ở trạng thái dừng này, electron trong nguyên tử chuyển động trên quỹ đạo dừng có bán kính r n = n 2 r o , với r 0 là bán kính Bo. Nếu một nguyên tử hiđrô hấp thụ một photon có năng lượng 2,856 eV thì bán kính quỹ đạo dừng của electron trong nguyên tử đó sẽ tăng lên
A. 2,25 lần
B. 6,25 lần
C. 4,00 lần
D. 9,00 lần
Các mức năng lượng của các trạng thái dừng của nguyên tử hiđrô được xác định bằng biểu thức E n = − 13 , 6 n 2 eV (với n = 1, 2, 3, …). Ở trạng thái dừng này, electron trong nguyên tử chuyển động trên quỹ đạo dừng có bán kính , với r0 là bán kính Bo. Nếu một nguyên tử hiđrô hấp thụ một phôtôn có năng lượng 2,856 eV thì bán kính quỹ đạo dừng của electron trong nguyên tử đó sẽ tăng lên
A. 2,25 lần.
B. 6,25 lần.
C. 4,00 lần
D. 9,00 lần.
+ Áp dụng tiên đề Bo về hấp thụ và bức xạ năng lượng, ta có