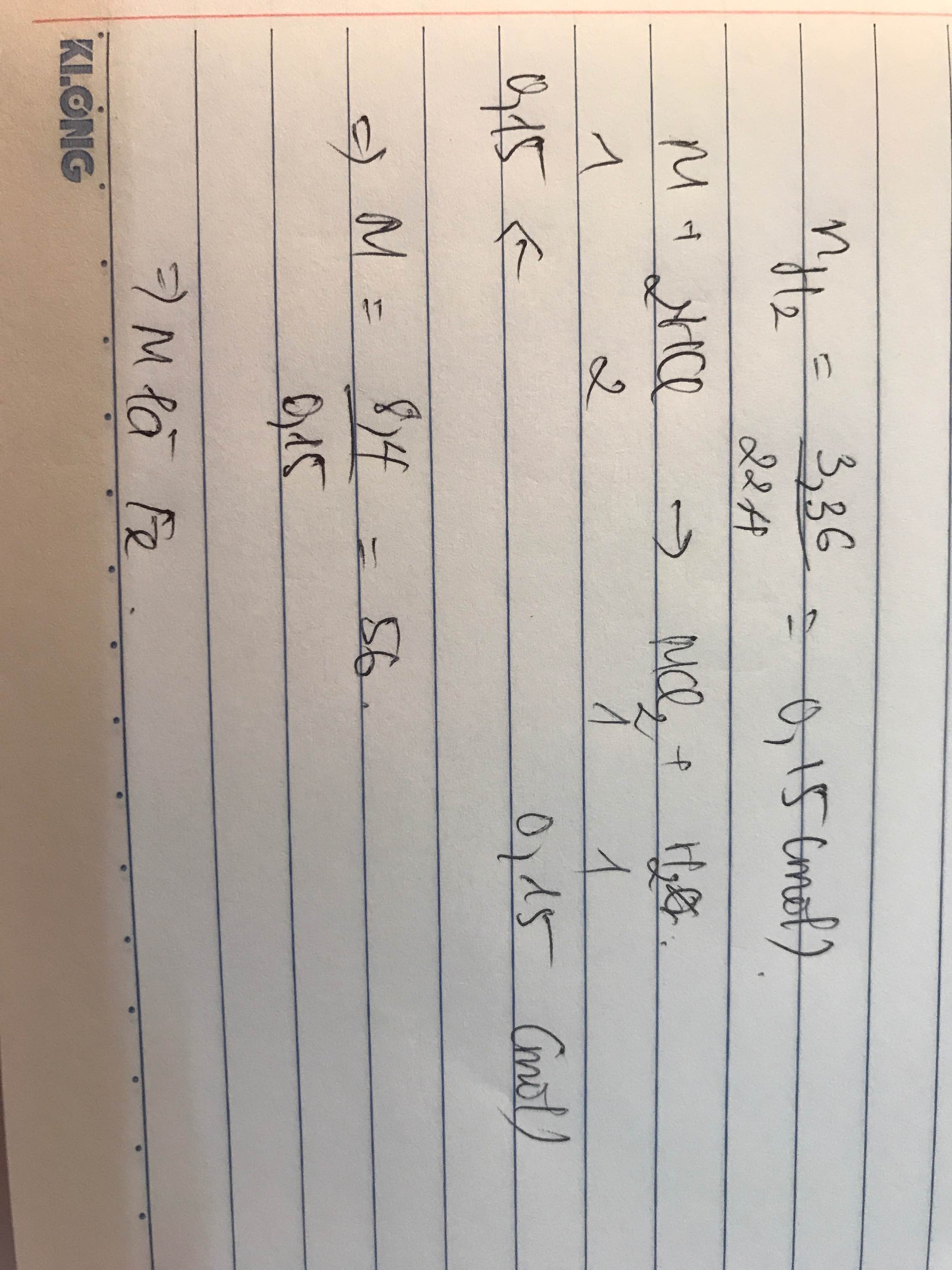Cho 2,875 g kim loại Na hòa tan vào 497,25 dung dịch NaOH a% ,thu được dung dịch mới có nồng độ 10,945%.Tính a?

Những câu hỏi liên quan
Hòa tan 4,6g kim loại Na vào H2O a,Viết PTHH b, Tính khối lượng NaOH thu được c, Tính nồng độ mol của dung dịch NaOH thu được biết thể tích dung dịch là 200ml
a, \(2Na+2H_2O\rightarrow2NaOH+H_2\)
b, \(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right)\)
Theo PT: \(n_{NaOH}=n_{Na}=0,2\left(mol\right)\Rightarrow m_{NaOH}=0,2.40=8\left(g\right)\)
c, \(C_{M_{NaOH}}=\dfrac{0,2}{0,2}=1\left(M\right)\)
Đúng 1
Bình luận (0)
hòa tan kim loại Na vài nước.sau phản ứng thu đc 300ml dung dịch NaOH 6,72lit H2 ở đktc A viết PTHH B tìm nồng độ mol/l dung dịch thu được C nêu cách pha chế 300ml dung dịch NaOH với nồng độ thu được ở trên
$a) 2Na + 2H_2O \to 2NaOH + H_2$
$b) $n_{H_2} = \dfrac{6,72}{22,4} = 0,3(mol)$
Theo PTHH : $n_{NaOH} = 2n_{H_2} = 0,6(mol)$
$C_{M_{NaOH}} = \dfrac{0,6}{0,3} = 2M$
c) $m_{NaOH} = 0,6.40 = 24(gam)$
Cách pha chế :
- Cân lấy 24 gam NaOH khan, nghiền nhỏ cho vào cốc có dung tích 500 ml có chia vạch
- Thêm từ từ nước vào cốc cho đến khi chạm vạch 300ml thì dừng, khuấy đều
Đúng 2
Bình luận (0)
Hòa tan kim loại sắt vào dung dịch HCl. Sau phản ứng cho vào dung dịch thu được 160 (g) dung dịch NaOH thấy xuất hiện 18 (g) kết tủa.
a) Viết phương trình hóa học.
b) Tính thể tích khí hidro thoát ra (đktc).
c) Tính nồng độ % của dung dịch NaOH đã dùng.
PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
\(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2\downarrow+2NaCl\)
Ta có: \(n_{Fe\left(OH\right)_2}=\dfrac{18}{90}=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{NaOH}=0,4\left(mol\right)\\n_{H_2}=0,2\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=0,2\cdot22,4=4,48\left(l\right)\\C\%_{NaOH}=\dfrac{0,4\cdot40}{160}\cdot100\%=10\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Đem hòa tan 2,7g kim loại A trong 50g dung dịch HCl được dung dịch X. Để trung hòa dung dịch X cần 50g dung dịch NaOH 8%, được dung dịch Y. Trong dung dịch Y, NaCl có nồng độ 5,71%.
a)Tìm kim loại A.
b) Tính nồng độ dung dịch HCl đã dùng.
c) Tính nồng độ muối của A trong dd Y.
NaOH = 0,1 mol => HCl dư 0,1 mol và NaCl = 0,1 mol
=> khối lượng dd Y = 0,1. 58,5: 5,71% = 102,452
BTKL => mH2 = 2,7+50+50 - 102,452 = 0,248g
=> Số mol H2 = 0,124 mol
=> HCl pư = 0,248 mol
=> tổng HCl = 0,348 mol
=> C% của HCl = 0,348. 36,5: 50 = 25,404%.
Đúng 0
Bình luận (3)
a: hòa tan hoàn toàn 0,3 mol NaOH vào nước thu được 0,5 lít dung dịch NaOH. tính nồng độ mol của dung dịch?
b: hòa tan hoàn tàn 24 gam NaOH vào nước thu được 400ml dung dịch NaOH. tính nồng độ mol của dung dịch?
\(a,C_{M\left(NaOH\right)}=\dfrac{0,3}{0,5}=0,6M\\ b,n_{NaOH}=\dfrac{24}{40}=0,6\left(mol\right)\\ C_{M\left(NaOH\right)}=\dfrac{0,6}{0,4}=1,5M\)
Đúng 1
Bình luận (0)
cho 8,4 gam một kim loại M hóa trị II vào dung dịch HCl 10% dư. Sau khi kim loại hòa tan hoàn toàn thu được 3,36 lít khí đo ở đktc và dung dịch A.
a. Xác định kim loại M
b.Để phản ứng hết dung dịch A cần 500ml dung dịch NaOH 1M. Tính nồng độ phần trăm các chất trong dung dịch A
dạ em làm xong câu B rồi mọi người khỏi cần trả lời nữa ạ
Đúng 0
Bình luận (2)
Hòa tan hoàn toàn 2,3 g một kim loại nhóm 1A vào 57,8 g nước thu được 1,12 lít khí h2 và dung dịch a
a. xác định tên kim loại
b .tính nồng độ phần trăm chất tan trong dung dịch a
a)Gọi A là kim loại cần tìm.
\(n_{H_2}=\dfrac{1,12}{22,4}=0,05mol\)
Ta có PTHH:
\(2A+2H_2O\rightarrow2AOH+H_2\uparrow\)
0,1-----------------0,1--------0,05-----(mol);
Vậy \(M_A=\dfrac{2,3}{0,1}=23\)(g/mol) => A là Na
b) Ta có: \(m_{dd}=2,3+57,8-0,05\cdot2=60g\)
Từ đó suy ra:\(\%C_{NaOH}=\dfrac{0,1\cdot40}{60}\cdot100\%=6,67\%\)
Đúng 1
Bình luận (0)
Hòa tan m gam rượu etylic ( D = 0,8 g/ml) vào 108 ml nước ( D= 1 g/ml) tạo thành dung dịch A. Cho dung dịch A tác dụng với kim loại Na dư, thu được 85,12 lít khí H2 (đktc). Tính giá trị m và nồng độ mol của rượu etylic
nH2 = 85,12 : 22,4 = 3,8 (mol) ; nH2O = VH2O.D = 108 (g) => nH2O = 108/18 = 6 (mol)
PTHH:
2Na + 2C2H5OH → 2C2H5ONa + H2↑
x → 0,5x (mol)
2Na + 2H2O → 2NaOH + H2↑
6 → 3 (mol)
Ta có: nH2 = 0,5x + 3 = 3,8
=> x = 1,6 (mol) = nC2H5OH
mC2H5OH = 1,6.46 = 73,6 (g)
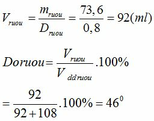
Đúng 0
Bình luận (0)
Hòa tan 3,68 g một kim loại kiềm M hòa tan vào nước dư, thu được 1,792 lit khí H, (đktc) và 200 ml dung dịch X. a-Xác định tên kim loại kiểm. b-Tính nồng độ moll của dung dịch X.
Gọi M là khối lượng mol trung bình của 2 nguyên tố
nH2=6.72/22.4=0.3 mol
M + H2O --> MOH + 1/2 H2
0.6mol---------------------0.3mol
-> M=20.2/0.3=67.3333
-->M1<67.33<M2
mà 2 kim loại này thuộc hai chu kì liên tiếp nhau
--> Kim loại đó là KI và Rb
Đúng 1
Bình luận (0)