Đại lượng đặc trưng cho đô biến thiên nồng độ của một trong các chất phản ứng hoặc sản phẩm phản ứng trong một đơn vị thời gian gọi là
A. tốc độ phản ứng.
B. cân bằng hoá học.
C. tốc độ tức thời.
D. quá trình hoá học.
Đại lượng đặc trưng cho đô biến thiên nồng độ của một trong các chất phản ứng hoặc sản phẩm phản ứng trong một đơn vị thời gian gọi là
A. tốc độ phản ứng.
B. cân bằng hoá học.
C. tốc độ tức thời.
D. quá trình hoá học.
Cho các phát biểu sau:
1, Phản ứng thuận nghịch là phản ứng xảy ra theo 2 chiều ngược nhau.
2, Chất xúc tác làm tăng tốc độ phản ứng thuận và nghịch.
3, Tại thời điểm cân bằng trong hệ vẫn luôn có mặt các chất phản ứng và các sản phẩm.
4, Khi phản ứng đạt trạng thái cân bằng hoá học, nồng độ các chất vẫn có sự thay đổi.
5, Khi phản ứng đạt trạng thái cân thuận nghịch bằng hoá học, phản ứng dừng lại.
Các phát biểu sai là
A. 2, 3.
B. 4, 5.
C. 3, 4.
D. 3, 5.
Đáp án B
(1) Đúng
(2) Đúng, xúc tác làm tăng tốc độ cả phản ứng thuận và nghịch
(3) Đúng do phản ứng thuận nghịch phản ứng xảy ra k hoàn toàn, tại thời điểm cân bằng luôn có mặt chất pu và chất sp
(4) Sai do nồng độ các chất k đổi thì phản ứng tiến tới trạng thái cân bằng
(5) Sai do cân bằng là cân bằng động nên phản ứng vẫn xảy ra, tốc độ phản ứng thuân và nghịch là bằng nhau
Chọn B
Cho các phát biểu sau:
1, Phản ứng thuận nghịch là phản ứng xảy ra theo 2 chiều ngược nhau trong cùng điều kiện.
2, Chất xúc tác làm tăng tốc độ phản ứng thuận và nghịch.
3, Tại thời điểm cân bằng trong hệ vẫn luôn có mặt các chất phản ứng và các sản phẩm.
4, Khi phản ứng đạt trạng thái cân bằng hoá học, nồng độ các chất vẫn có sự thay đổi.
5, Khi phản ứng đạt trạng thái cân thuận nghịch bằng hoá học, phản ứng dừng lại.
Số phát biểu sai là
A. 2
B. 3
C. 1
D. 4
Đáp án A
1, đúng
2, đúng
3, đúng
4, sai, nồng độ các chất sẽ không thay đổi ở trạng thái cân bằng (ở đây giả thiết các điều kiện khác không đổi)
5, sai, ở trạng thái cân bằng, phản ứng thuận và nghịch vẫn tiếp tục, nhưng nồng độ các chất đều không đổi.
=> Đáp án A
Để đánh giá mức độ xảy ra nhanh hay chậm của một phản ứng hoá học người ta dùng đại lượng nào sau đây ?
A. Độ tăng khối lượng sản phẩm.
B. Tốc độ phản ứng.
C. Độ tăng khối lượng chất tham gia phản ứng.
D. Thể tích chất tham gia phản ứng.
chọn từ trong ngoặc để diền vào chỗ trống
(nhỏ hơn ; bằng ; lớn hơn)
Trong một phản ứng hoá học ; tổng khối lượng của các chất sản phẩm ...............................tổng khối lượng của các chất tham gia phản ứng hoá học.
Trong một phản ứng hoá học ; tổng khối lượng của các chất sản phẩm bằng tổng khối lượng của các chất tham gia phản ứng hoá học
Trong một phản ứng hoá học ; tổng khối lượng của các chất sản phẩm .........bằng......................tổng khối lượng của các chất tham gia phản ứng hoá học.
Trong những điều khẳng định sau, điều nào là phù hợp với một phản ứng hoá học ở trạng thái cân bằng ?
A. Phản ứng thuận đã kết thúc.
B. Phản ứng nghịch đã kết thúc.
C. Tốc độ của phản ứng thuận và nghịch bằng nhau.
D. Nồng độ của các chất tham gia và tạo thành sau phản ứng như nhau.
Trong một phản ứng hoá học, tổng khối lượng của các chất sản phẩm bằng tổng khối lượng của các chất phản ứng là do trong phản ứng hoá học:
(1) chỉ có liên kết giữa các nguyên tử thay đổi.
(2) số nguyên tử của mỗi nguyên tố giữ nguyên.
(3) khối lượng của các không đổi.
(4) Cả 3 nhận định trên đều đúng.
Giải thích nào đúng:
A. (1).
B. (2) .
C. (3).
D. (4) .
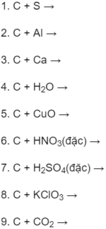
Ở nhiệt độ cao cacbon có thể phản ứng với nhiều đơn chất và hợp chất. Hãy lập các phương trình hoá học sau đây và cho biết ở phản ứng nào cacbon thể hiện tính khử. Ghi rõ số oxi hoá của cacbon trong từng phản ứng.
Ngâm một lá sắt có khối lượng 2,5 gam trong 25 ml dung dịch CuSO4 15% có khối lượng riêng là 1,12 g/ml. Sau một thời gian phản ứng, người ta lấy lá sắt ra khỏi dung dịch, rửa nhẹ, làm khô thì cân nặng 2,58 gam.
a) Hãy viết phương trình hoá học.
b) Tính nồng độ phần trăm của các chất trong dung dịch sau phản ứng.
* Nhận xét: “sau một thời gian phản ứng”, suy ra CuSO4 có thể vẫn còn dư. Gọi số mol Fe phản ứng là x mol.
a) Phương trình hóa học:
Fe + CuSO4 → FeSO4 + Cu
P/ư: x x x x mol
Khối lượng lá sắt tăng = 2,58 - 2,5 = 0,08 gam. Ta có phương trình:
64x - 56x = 0,08
x = 0,01 mol
b) Sô mol CuS04 ban đầu = 0,02625 mol
Trong dung dịch sau phản ứng có hai chất tan là FeSO4 0,01 mol và CuSO4 dư 0,01625 mol.
Khối lượng dung dịch:
mdd = + mFe(p.ư) – mCu = 25.1,12 + 0,01.56 - 0,01.64 = 27,91 g
C%, CuS04 = .100% ≈ 9,32%
C%, FeSO4 = .100% ≈ 5,45%
\(m_{ddCuSO_4}\) = 25.1,12 = 28g\(\Rightarrow m_{CuSO_4}\) = 4,2g\(\Rightarrow n_{CuSO_4}\) = 0,02625mol
Fe + CuSO4\(\rightarrow\) FeSO4 + Cu
x \(\rightarrow\) x-----------------x---------x
\(m_{tăng}\) = 64x-56x = 0,08g \(\Rightarrow\) x=0,01mol
\(n_{Fe\left(bđ\right)}\) = 5/112 mol \(\Rightarrow\) Fe dư, CuSO4 dư ( vì phản ứng ko hoàn toàn)
\(\Rightarrow\)trong dd sau pứ có \(FeSO_4=0,01mol\); \(CuSO_4=0,01625mol\)
mdd = mCuSO4 + mFepư - mCu = mddCuSO4 - \(m_{giảm}\) =28 - 0,08 = 27,92g
\(\Rightarrow\) C% FeSO4 = 0,01(56 + 96).100/ 27,92 = 5,44%
C% CuSO4 = 0,01625.(64 + 96).100/27,92 = 9,31%
Ngâm một lá sắt có khối lượng 2,5 gam trong 25 ml dung dịch CuSO4 15% có khối lượng riêng là 1,12 g/ml. Sau một thời gian phản ứng, người ta lấy lá sắt ra khỏi dung dịch, rửa nhẹ, làm khô thì cân nặng 2,58 gam.
a) Hãy viết phương trình hoá học.
b) Tính nồng độ phần trăm của các chất trong dung dịch sau phản ứng.
Bạn xem câu trả lời của mình nha :
a) Phương trình hóa học:
Fe + CuSO4 → FeSO4 + Cu
P/ư: x x x x mol
Khối lượng lá sắt tăng = 2,58 - 2,5 = 0,08 gam. Ta có phương trình:
64x - 56x = 0,08
x = 0,01 mol
b) Sô mol CuS04 ban đầu = 0,02625 mol
Trong dung dịch sau phản ứng có hai chất tan là FeSO4 0,01 mol và CuSO4 dư 0,01625 mol.
Khối lượng dung dịch:
mdd = + mFe(p.ư) – mCu = 25.1,12 + 0,01.56 - 0,01.64 = 27,91 g
C%, CuS04 = .100% ≈ 9,32%
C%, FeSO4 = .100% ≈ 5,45%