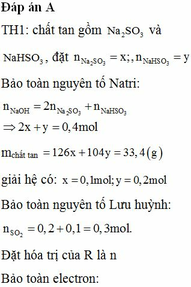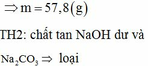Hoà tan hoàn toàn 0,32g một kim loại hoá trị 2 vào dung dịch H2SO4 đặc nóng,lượng khí thoát ra hấp thụ hết bởi 45 ml dung dịch NaOH 0,2M .Tạo dung dịch chứa 0,608g muối.Xác định tên kim loại?

Những câu hỏi liên quan
Hòa tan hoàn toàn 0,32 g một kim loại R hóa trị II vào dung dịch H2SO4 đặc nóng ,lượng khí SO2 sinh ra hấp thụ hết bởi 45 ml dung dịch NaOH 0,2M.Biết trong dung dịch chứa 0,608g muối.Xác định kim loại R
M+2H2SO4-->MSO4+SO2+2H2O
0.005<----------------------0.005
nNaOH=0.2.0.045=0.009
SO2 + 2NaOH-->Na2SO3+H2O
0.0045<0.009-------0.0045
SO2+Na2SO3+H2O-->2NaHCO3
amol>amol---------------->2amol
ta có :126(0.0045-a)+208=0.608
< = >0.567-126a+208a=0.608
< = > 82a=0.041
< = > a=0.0005
nSO2=0.0005+0.0045=0.005
MM=0.32/0.005=64
=> M là Đồng (Cu)
Đúng 1
Bình luận (1)
Giả sử R có hóa trị II duy nhất.
pt: R + 2H2SO4 -> RSO4 + SO2 + 2H2O
Gọi R là nguyên tử khối của nguyên tố R (cho dễ) => molSO2 = molR= 0,32/R
Khi cho SO2 vào NaOH:
SO2 + NaOH ->NaHSO3
x -------->x------------>x mol
SO2 + 2NaOH ->Na2SO3 + H2O
y------------>2y-------->y mol
Theo giả thiết của 2 cái NaOH và khối lượng muối có hpt:
x + 2y = 0,045*0,2
104x+ 126y = 0,608
=> x= 10^-3 mol
y= 4*10^-3 mol
=> molSO2 = 5*10^-3 = 0,32/R => R= 64 => nguyên tố R là Cu
Đúng 2
Bình luận (1)
Hoà tan a mol kim loại M trong dung dịch H2SO4 đặc nóng, trong điều kiện thí nghiệm thấy tiêu tốn hết 1,25a mol H2SO2 thu được khí X và 24 g muối Y. Cho khí X hấp thụ hoàn toàn vào 240 ml dung dịch NaOH 0,25M thu được 3,02g muối khan. Xác định kim loại M?
Hoà tan a mol kim loại M trong dung dịch H2SO4 đặc nóng, trong điều kiện thí nghiệm thấy tiêu tốn hết 1,25a mol H2SO2 thu được khí X và 24 g muối Y. Cho khí X hấp thụ hoàn toàn vào 240 ml dung dịch NaOH 0,25M thu được 3,02g muối khan. Xác định kim loại M?
Hòa tan hoàn toàn 11,2 gam một kim loại R bằng dung dịch H2SO4, thu được khí SO2. Cho toàn bộ lượng khí này hấp thụ hết vào 400 ml dung dịch NaOH 1M, thu được dung dịch chứa 33,4 gam chất tan. Mặt khác, hòa tan hoàn toàn 19,6 gam kim loại R vào 160 ml dung dịch HCl 2M thu được dung dịch X. Cho X tác dụng với dung dịch AgNO3 dư, thu được m gam kết tủa. Giá trị của m là A. 57,8. B. 45,92. C. 54,6 D. 83,72
Đọc tiếp
Hòa tan hoàn toàn 11,2 gam một kim loại R bằng dung dịch H2SO4, thu được khí SO2. Cho toàn bộ lượng khí này hấp thụ hết vào 400 ml dung dịch NaOH 1M, thu được dung dịch chứa 33,4 gam chất tan. Mặt khác, hòa tan hoàn toàn 19,6 gam kim loại R vào 160 ml dung dịch HCl 2M thu được dung dịch X. Cho X tác dụng với dung dịch AgNO3 dư, thu được m gam kết tủa. Giá trị của m là
A. 57,8.
B. 45,92.
C. 54,6
D. 83,72
Mn giúp em vs ạ
Hòa tan hoàn toàn 36 gam một oxit kim loại trong lượng dư dung dịch H2SO4 đặc, nóng thu được V lít khí SO2 (đktc) duy nhất và dung dịch chứa 80 gam một muối sunfat. Hấp thụ hoàn toàn lượng khí SO2 nói trên trong 600 ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng thu được 35,5 gam chất rắn khan. Tìm giá trị của V và xác định công thức của oxit kim loại ban đầu.
35,5 gam chất rắn gồm : $NaHSO_3(a\ mol) , Na_2SO_3(b\ mol)$
Ta có :
\(\left\{{}\begin{matrix}104a+126b=35,5\\a+2b=n_{NaOH}=0,6\end{matrix}\right.\). Suy ra : a = 1,8 ; b = -1,2<0 (loại)
35,5 gam chất rắn gồm : $Na_2SO_3(x\ mol) ; NaOH(y\ mol)$
Ta có :
\(\left\{{}\begin{matrix}126x+40y=35,5\\2x+y=n_{NaOH}=0,6\end{matrix}\right.\). Suy ra : x = 0,25 ; y = 0,1
Suy ra : $n_{SO_2} = x = 0,25(mol) \Rightarrow V = 0,25.22,4 = 5,6(lít)$
Coi oxit gồm kim loại R(hóa trị n) và 0
Gọi $n_R = m(mol) ; n_O = t(mol)$
Muối là $R_2(SO_4)_n : 0,5m(mol)$
Ta có :
$Rm + 16t = 36$
$m_{muối} = 0,5m(2R + 96n) = 80$
Bảo toàn e : $mn = 2t + 0,25.2$
Suy ra : Rm = 32 ; mn = 1 ; t = 0,25
$mn = 1 \Rightarrow m = \dfrac{1}{n}$
$Rm = 32 \Rightarrow R\dfrac{1}{n} = 32 \Rightarrow R = 32n$
Với n = 2 thì $R = 64(Cu)$
Vậy CTHH oxit là CuO
Đúng 0
Bình luận (0)
Cho 4,2g muối cacbonat của kim loại hoá trị II. Hoà tan vào dung dịch HCl dư, thì có khí thoát ra. Toàn bộ lượng khí được hấp thụ vào 100ml dung dịch Ba(OH)2 0,46M thu được 8,274g kết tủa. Kim loại là A. Ca hoặc Mg B. Ca C. Mg D. Ba hoặc Ca
Đọc tiếp
Cho 4,2g muối cacbonat của kim loại hoá trị II. Hoà tan vào dung dịch HCl dư, thì có khí thoát ra. Toàn bộ lượng khí được hấp thụ vào 100ml dung dịch Ba(OH)2 0,46M thu được 8,274g kết tủa. Kim loại là
A. Ca hoặc Mg
B. Ca
C. Mg
D. Ba hoặc Ca
Đáp án A
Vì chưa biết lương Ba(OH)2 dư hay thiếu => có 2 trường hợp
* TH1: khi Ba(OH)2 dư, tính theo lượng kết tủa
Gọi công thức muối là MCO3
CO2 + Ba(OH)2 → BaCO3 + H2O
0,042 0,042
MCO3 +2 HCl → MCl2 + CO2 + H2O
0,042 0,042
Mmuối = M+ 60 = 4,2/0,042=100 => M = 40 (Ca)
* TH2: khi Ba(OH)2 thiếu , Ba(OH)2 hết, 1 phẩn kết tủa bị hòa tan
CO2 + Ba(OH)2 → BaCO3 + H2O
0,046 0,046
nkết tủa bị hòa tan = 0,046- 0,042=0,004
BaCO3 + CO2 + H2O → Ba(HCO3)2
0,004 0,004
=> nCO2 = 0,004+ 0,0046=0,05
MCO3 +2 HCl → MCl2 + CO2 + H2O
0,05 0,05
Mmuối = M+ 60 = 4,2/0,05 = 84 => M = 24 (Mg)
Chú ý: Xét 2 trường hợp
Đúng 0
Bình luận (0)
Hoà tan 60,2g hỗn hợp gồm 2 muối cacbonat và sùnit của cùng một kim loại kiềm vào dung dịch HCl dư. Toàn bộ khí thoát ra được hấp thụ tối thiểu bởi 200ml dung dịch NaOH 2M.
a)Xác định kim loại kiềm,b) Xác định % khối lượng mỗi muối trong hỗn hợp ban đầu (Kim loại kiềm là kim loại có hoá trị I, tan trong nước,gồm : Li,Na,K,,Rb,Cs,Fr
Hòa tan hoàn toàn 0,8 g một kim loại hoá trị II hoà tan hoàn toàn trong 100 ml H 2 S O 4 0,5 M. Lượng axit còn dư phản ứng vừa đủ với 33,4 ml dung dịch NaOH 1,00 M. Xác định tên kim loại.
Số mol H 2 S O 4 trong 100ml dung dịch 0,5M là :
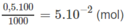
Số mol NaOH trong 33,4 ml nồng độ 1M :
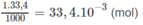
H 2 S O 4 + 2NaOH → N a 2 S O 4 + 2 H 2 O
Lượng H 2 S O 4 đã phản ứng với NaOH :

Số mol H 2 S O 4 đã phản ứng với kim loại là :
5. 10 - 2 - 1.67. 10 - 2 = 3,33. 10 - 2 mol
Dung dịch H 2 S O 4 0,5M là dung dịch loãng nên :
X + H 2 S O 4 → X S O 4 + H 2 ↑
Số mol X và số mol H 2 S O 4 phản ứng bằng nhau, nên :
3,33. 10 - 2 mol X có khối lượng 0,8 g
1 mol X có khối lượng: 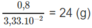
⇒ Mkim loại = 24 g/mol.
Vậy kim loại hoá trị II là magie.
Đúng 0
Bình luận (0)
hoà tan hoàn toàn 12,8g một kim loại hoá trị II vào dung dịch h2so4 đặc nóng thu được 4,48l khí kim loại đã dùng là
\(n_{SO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: \(R+2H_2SO_{4\left(đặc,nóng\right)}\rightarrow RSO_4+SO_2\uparrow+2H_2O\)
0,2<-------------------------------------0,2
\(\rightarrow M_R=\dfrac{12,8}{0,2}=64\left(\dfrac{g}{mol}\right)\\ \rightarrow R:Cu\)
Đúng 3
Bình luận (0)
Khí thoát ra là SO2
\(R\rightarrow R^{2+}+2e\\ S^{+6}+2e\rightarrow S^{+4}\\ n_{SO_2}=\dfrac{4,48}{22,4}=0,2\\ Bảotoàne:n_R.2=n_{S^{+4}}.2\\ \Rightarrow n_R=0,2\left(mol\right)\\ \Rightarrow M_R=\dfrac{12,8}{0,2}=64\left(Cu\right)\)
Đúng 2
Bình luận (0)