Hòa tan 12,8 gam Cu trong axit H2SO4 đặc, nóng dư. Thể tích khí SO2 thu được (đktc) là
A. 4,48 lít
B. 2,24 lít
C. 6,72 lít
D. 8,96 lít
Hòa tan 12,8 gam Cu trong axit H2SO4 đặc, nóng dư. Thể tích khí SO2 thu được (đktc) là
A. 4,48 lít
B. 2,24 lít
C. 6,72 lít
D. 8,96 lít
Hòa tan 12,8 gam Cu trong axit H 2 SO 4 đặc, nóng dư. Thể tích khí SO 2 thu được (đktc) là
A. 4,48 lít
B. 2,24 lít
C. 6,72 lít
D. 8,96 lít
Chọn A
nCu = 12 , 8 64 = 0,2 (mol)
Bảo toàn electron: 2 n S O 2 = 2nCu
=> n S O 2 = nCu = 0,2 (mol) => V = 0,2.22,4 = 4,48 (lít)
Bài 16. Hòa tan hoàn toàn 12,8 gam đồng bằng dung dịch H2SO4 đặc, nóng, dư thu được dung dịch X và V lít khí SO2 (đktc).Phương trình hóa học như sau: Cu + H2SO4 đặc,nóng CuSO4 + SO2 + H2O
a.Lập PTHH theo phương pháp thăng bằng electron, chỉ rõ chất khử, chất oxi hóa, QT oxi hóa, QT khử. b.Tính V.
Bài 17: Hòa tan hoàn toàn 11,2 gam sắt bằng dung dịch H2SO4 đặc, nóng, dư thu được dung dịch X và V lít khí SO2 (đktc). Phương trình phản ứng như sau: Fe + H2SO4 đặc,nóng Fe2(SO4)3 + SO2 + H2O a.Lập PTHH theo phương pháp thăng bằng electron, chỉ rõ chất khử, chất oxi hóa, QT oxi hóa, QT khử. b.Tính V
. Bài 18: Hoà tan hoàn toàn 8,8 gam hỗn hợp A gồm Cu và Fe trong 100ml dd H2SO4 x (mol/lít) theo các phản ứng sau: Fe + H2SO4 đặc,nóng Fe2(SO4)3 + SO2 + H2O (1) Cu + H2SO4 đặc,nóng CuSO4 + SO2 + H2O (2) Sau khi các phản ứng kết thúc thu được dung dịch B và 4,48 lít khí SO2 (đktc). a.Lập các phương trình hóa học (1) và (2). b.Tính % khối lượng mỗi chất có trong A. c.Để tác dụng vừa hết với các chất có trong dung dịch B cần 200ml dung dịch NaOH 4M. Tính giá trị của x
. Bài 19: Hoà tan hết 17 gam hỗn hợp bột A gồm Al và FeCO3 trong 300ml dung dịch HCl 2M thu được dung dịch B và 5,6 lít hỗn hợp khí C (đktc). a) Tính % khối lượng mỗi chất có trong A. b) Tính thể tích dung dịch NaOH 0,5M cần để trung hoà hết lượng axit có trong dung dịch B
. Bài 20: Hoà tan hết 13 gam hỗn hợp bột A gồm Mg và Na2CO3 trong Vml dung dịch H2SO4 1M (loãng) thu được 4,48 lít hỗn hợp khí B (đktc) và dung dịch C. a) Tính % khối lượng mỗi chất có trong A. b) Cho dung dịch C tác dụng với dung dịch Ba(OH)2 dư, lọc kết tủa nung đến khối lượng không đổi được 62,25 gam chất rắn. Tính V.
Câu 3: Hòa tan hoàn toàn 36,8 gam hỗn hợp X gồm Fe, Fe3O4 và CuO trong dd HCl dư thu được dd A và 2,24 lít khí H2 (đktc). Dẫn khí H2S dư vào dd A thu được 12,8 gam kết tủa. Nếu cho hỗn hợp X trên tác dụng với axit H2SO4 đặc, nóng, dư thì tạo ra V lít khí SO2 (sản phẩm khử duy nhất và đo ở đktc). Các p/ư xảy ra hoàn toàn. Viết các phương trình hóa học của các p/ư xảy ra và xác định chất khử, chất oxi hóa trong các p/ư đó. Tính giá trị của V
Hoà tan 12,8 gam Cu bằng axit H 2 S O 4 đặc, nóng (dư), sinh ra V lít khí S O 2 (sản phẩm khử duy nhất ở đktc). Giá trị của V là
A. 2,24.
B. 3,36.
C. 4,48.
D. 6,72.
Cho 12,8 gam hỗn hợp X gồm Fe và FeO vào dung dịch H2SO4 loãng dư thấy có 2,24 lít H2 thoát ra.a-Tính số mol Fe và FeO.Biết khí đo ở đktc .(1đ)b-Cho toàn bộ lượng hỗn hợp X trên tác dụng với H2SO4 đặc nóng dư thu được V lít khí SO2 ở đktc .Tính V
\(n_{Fe}=a\left(mol\right),n_{FeO}=b\left(mol\right)\)
\(m_X=56a+72b=12.8\left(g\right)\)
\(n_{H_2}=n_{Fe}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(\Rightarrow a=0.1\)
\(b=\dfrac{12.8-56\cdot0.1}{72}=0.1\left(mol\right)\)
\(BTe:\)
\(3n_{Fe}+n_{FeO}=2n_{SO_2}\)
\(\Rightarrow n_{SO_2}=\dfrac{3\cdot0.1+0.1}{2}=0.2\left(mol\right)\)
\(V_{SO_2}=0.2\cdot22.4=4.48\left(l\right)\)
\(\)
Hòa tan hoàn toàn 17,6 gam hỗn hợp Fe, Cu (tỉ lệ mol 2 : 1) bằng axit H2SO4 đặc, nóng, dư, thu được V lít khí SO2 (đktc). Giá trị của V là:
A. 5,6
B. 4,48
C. 3,36
D. 8,96
Hòa tan hết 12,8 gam kim loại M trong H2SO4 đặc, nóng, thu được 4,48 lít khí SO2 (sản phẩm khử duy nhất ở đktc). Kim lại M là
A. Fe.
B. Mg.
C. Cu.
D. Al.
Đáp án C
Số mol SO2 thu được là: n SO 2 = 0 , 2 mol
Gọi hóa trị của M là n
Số mol của M là : n M = 12 , 8 M mol
Sơ đồ phản ứng :
![]()
Các quá trình nhường, nhận electron :

Hòa tan hết 15,2 gam hỗn hợp hai kim loại Fe và Cu trong dung dịch H2SO4 đặc, nóng, dư, thu được 6,72 lít khí SO2 (sản phẩm khử duy nhất, ở đktc). Mặt khác cho 1,52 gam hỗn hợp vào dung dịch H2SO4 loãng dư thì thể tích khí thoát ra ở đktc là
A. 0,672 lít.
B. 2,24 lít.
C. 0,224 lít.
D. 0,448 lít.
Đáp án C
Trong 15,2 gam hỗn hợp kim loại
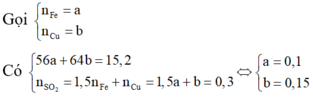
Do đó trong 1,52 gam hỗn hợp kim loại có 0,01 mol Fe.
Khi hòa tan 1,52 gam hỗn hợp kim loại vào dung dịch H2SO4 loãng dư thì nH = nF = 0,01
⇒ V H 2 = 0 , 224 ( lít )
Hòa tan hoàn toàn 7,68 gam kim loại M hóa trị II trong dung dịch H2SO4 đặc nóng dư, thu được dung dịch X và 2,688 lít khí SO2 ( sản phẩm khử duy nhất, đktc)
a, Xác định tên kim loại M
b, Dẫn toàn bộ lượng SO2 trên vào bình chứa 2,24 lít O2 (đkc) có 1 ít chất xúc tác V2O5 đun nóng t= 450-500 độ C sau 1 thời gian thu được 4,256 lít (đktc) hốn hợp khí B. TÍNH % THỂ TÍCH CÁC KHÍ TRONG KHÍ b?
C, hỖN HỢP y GỒM ( 6,72 gam Fe và 7,84 gam M trên) cho vào H2SO4 đặc nóng thu được dung dịch Z gồm 8,8 gam chất rắn không tan và V ( lít) SO2 ( đkc). Tính V?
Hóa học vô cơ
Mol SO2=2,688/22,4=0,12 mol
M \rightarrow M+2 +2e
0,12 mol<= 0,24 mol
S+6 +2e \rightarrow S+4
0,24 mol<=0,12 mol
=>0,12M=7,68=>M=64 M là Cu
b) mol O2=2,24/22,4=0,1 mol
Mol hhB=4,256/22,4=0,19 mol
2SO2 + O2 \rightleftharpoons 2SO3
Bđ:0,12 mol;0,1 mol
Pứ::x mol=>0,5x mol=>x mol
Sau:0,12-x mol;0,1-0,5x mol;x mol
Molhh B=0,12-x+0,1-0,5x+x=0,19=>x=0,06 mol
Vậy hh B gồm 0,06 mol SO2 0,07 mol O2 0,06 mol SO3 =>%V
c) mol Fe=6,72/56=0,12 mol
Mol Cu=7,84/64=0,1225 mol
mcr sau pứ=8,8g>mCu=>Cu chưa pư vs axit, Fe pứ 1phần
Fe \rightarrow Fe+3 +3e
x mol. => 3x mol
S+6 +2e \rightarrow S+4
3x mol=>1,5x mol
2Fe3+ + Fe \rightarrow 3Fe2+
x mol=>0,5 x mol
Fe dư:0,12-1,5x mol=>mFe=6,72-84x
mcr=8,8=6,72-84x+7,84=>x=0,06857 mol=>mol SO2=0,103 mol=>V=2,304l