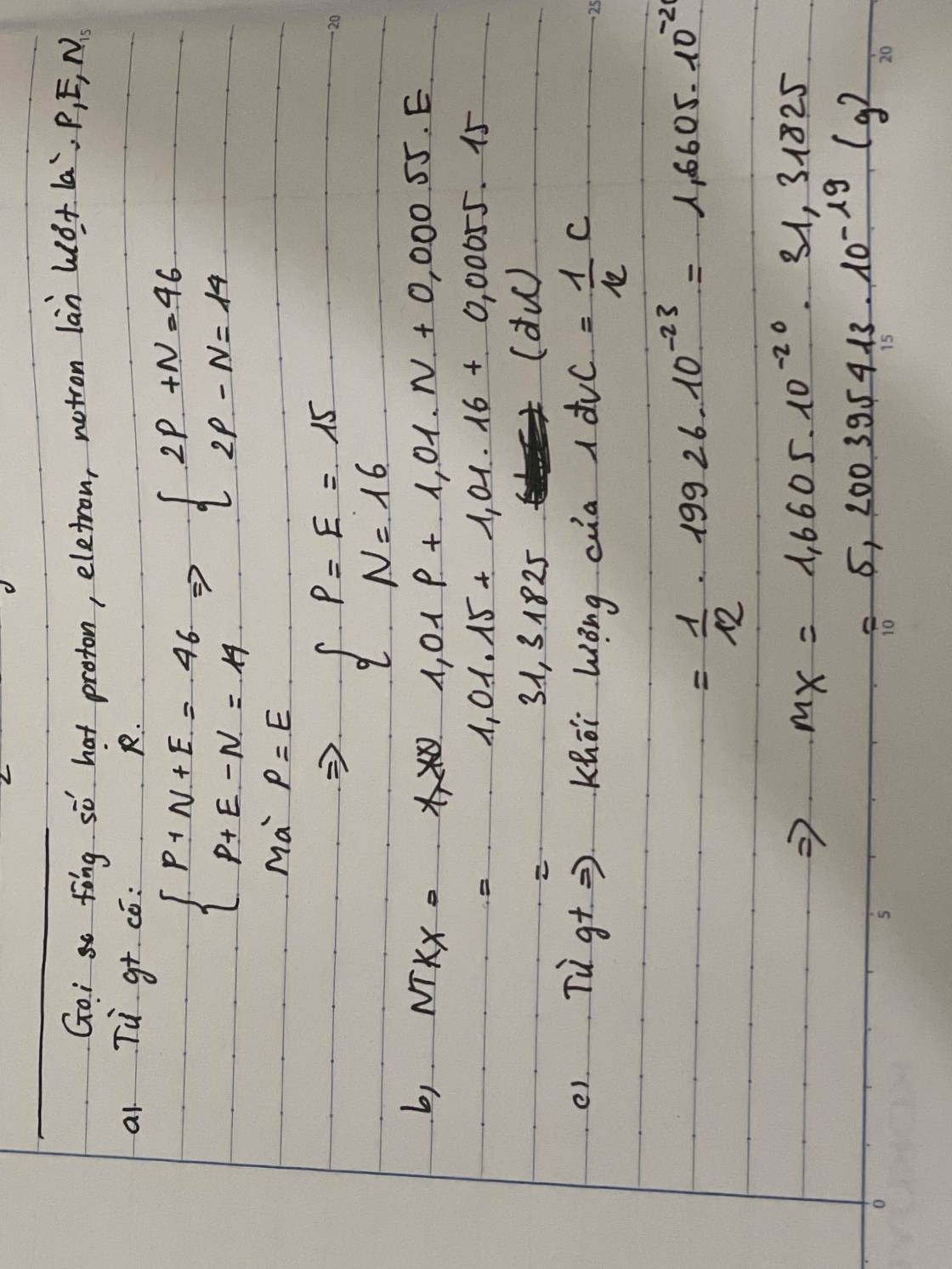Tìm số proton,notron, electron và số khối của các nguyên tử sau : a) X có tổng số hạt là 18, số p= số n b)Y có số khối là 27 và số hạt mang điện nhiều hơn số hạt không mang điện là 12 hạt c)Z có số khối là 35, số proton kém số notron 1 hạt

Những câu hỏi liên quan
Một nguyên tử X có tổng số hạt electron , proton , notron là 46 . Số hạt mang điện nhiều hơn số hạt ko mang điện 14 hạt .a) Tính số hạt proton, electron, notron.b) Tính nguyên tử khối của X, biết khối lượng proton khối lượng notron 1,01đvC.c) Tính khối lượng bằng gam của X, biết khôi lượng của nguyên tử C là 1,9926.10^{-23} gam.
Đọc tiếp
Một nguyên tử X có tổng số hạt electron , proton , notron là 46 . Số hạt mang điện nhiều hơn số hạt ko mang điện 14 hạt .
a) Tính số hạt proton, electron, notron.
b) Tính nguyên tử khối của X, biết khối lượng proton = khối lượng notron = 1,01đvC.
c) Tính khối lượng bằng gam của X, biết khôi lượng của nguyên tử C là 1,9926.10\(^{-23}\) gam.
1/ Phân tử A có công thức XYZ (X, Y, Z là ba nguyên tố khác nhau). Tổng số ba loại hạt proton, notron, electron trong một phân tử A là 141. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 35; hiệu nguyên tử khối giữa Y và Z gấp 64 lần nguyên tử khối của X; tổng số nguyên tử khối của Y và Z gấp 96 lần nguyên tử khối của X; trong nguyên tử Z có số hạt không mang điện bằng một nửa số hạt mang điện. Tìm công thức của chất A Xem nội dung đầy đủ tại:
Đọc tiếp
1/ Phân tử A có công thức XYZ (X, Y, Z là ba nguyên tố khác nhau). Tổng số ba loại hạt proton, notron, electron trong một phân tử A là 141. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 35; hiệu nguyên tử khối giữa Y và Z gấp 64 lần nguyên tử khối của X; tổng số nguyên tử khối của Y và Z gấp 96 lần nguyên tử khối của X; trong nguyên tử Z có số hạt không mang điện bằng một nửa số hạt mang điện. Tìm công thức của chất A Xem nội dung đầy đủ tại:
Tổng số hạt proton, notron, electron trong 2 nguyên tử A và B là 142 trong đó có số hạt mang điện nhiều hơn số hạt không mang điện là 42, số hạt mang điện của B nhièu hơn A là 12. Tính số proton mỗi loại.
gọi số hạt proton ,nơtron và electron của nt kim loại A là P1;N1 và E1
gọi số hạt proton ,nơtron và electron của nt kim loạiB là P2;N2;E2
Theo đb ta có :P1+N1+E1+P2+N2+E2=142 VÀ (P1+E1+P2+E2)-(N1+N2)=42
=> (P1+E1+P2+E2)=(142+42):2=92
Ta lại có:(P2+E2)-(P1+E1)=12
=>P2+E2=(92+12):2=52 VÌ SỐ P=E NÊN P2=E2=52/2=26
=>P1+E1=52-12=40 VÌ SỐ P=E NÊN P1=E1 =40/2=20
P2 = 26
P1 = 20
K nhé
tổng số hạt proton notron và electron trong 2 nguyên tử X và Y là 134. trong đó tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 38.Số hạt mang điện trong nguyên tử Y nhiều hơn số hạt mang điện trong nguyên tử X là 18. Xác định thành phần nguyên tử cửa X và Y
Tổng số hạt proton notron và electron trong 2 nguyên tử X và Y là 134
\(2\left(p_X+p_Y\right)+n_X+n_Y=134\left(1\right)\)
Tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 38
\(2\left(p_X+p_Y\right)-\left(n_X+n_Y\right)=38\left(2\right)\)
\(\left(1\right),\left(2\right):\)
\(p_X+p_Y=43\left(3\right)\)
\(n_X+n_Y=48\)
Số hạt mang điện trong nguyên tử Y nhiều hơn số hạt mang điện trong nguyên tử X là 18
\(2p_Y-2p_X=18\left(4\right)\)
\(\left(3\right),\left(4\right):\)
\(p_X=17,p_Y=26\)
Đề này tính được số proton thoi em nhé !
Đúng 5
Bình luận (0)
Tổng số hạt proton , notron và electron trong hai nguyên tử phi kim X và Y là 76 . Trong đó tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 24 . Tổng số hạt mang điên của nguyên tử Y nhiều hơn tổng số hạt mang điện của nguyên tử X là 18 . Xác định 2 kim loại X và Y.
Gọi tổng số hạt proton , electron , notron của 2 nguyên tử X và Y là M
gọi số proton , electron , notron của M lần lượt là p ,e ,n . TA CÓ :
p+e+n = 76 => 2p + n = 76 ( vì nguyên tử trung hòa về điện) (1)
do tổng số hạt mang điện tích lớn hơn tổng số hạt không mang điện tích là 24 hạt
=> 2p - n = 24
Kết hợp (1) ta được 2p = 50 => tổng số hạt mang điện tích của 2 nguyên tử X và Y là 50 hạt (*)
Từ đề ra ta lại có :
số hạt mang điện(Y) - số hạt mang điện(X) = 18(**)
Từ (*) và (**) => số hạt mang điện của Y = 34 (hạt) => Y có 17 proton => Y là nguyên tố Clo
=> số hạt mang điện của X = 16 (hạt) => X có 8 proton => X là nguyên tố Oxi
Đúng 0
Bình luận (1)
Nguyên tử của nguyên tố X có tổng số hạt là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12. Xác định số hạt proton, electron và notron trong X.
Gọi số hạt proton = số hạt electron = p
Gọi số hạt notron = n
Ta có :
$2p + n = 40$
$2p - n = 12$
Suy ra : p = 13 ; n = 14
Vậy X có 13 hạt proton, 13 hạt electron, 14 hạt notron
Đúng 3
Bình luận (0)
Nguyên tử nguyên tố x có tổng số hạt proton notron electron là 34 hạt trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 10 hạt
a, xác định nguyên tố x
b, tính khối lượng bằng gam của một nguyên tử x biết khối lượng của một nguyên tử C là 1,9926×10^_23 gam và nguyên tử khối của Cacbon bằng 12 dvc
Xem chi tiết
a, Gọi số proton, electron và notron của X lần lượt là p;e;n
Theo gt ta có:
\(\left\{{}\begin{matrix}2p+n=34\\2p-n=10\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}p=11\\n=12\end{matrix}\right.\)
Vậy X là Na
b, Ta có: $m_{Na}=23.1,9926.10^{-23}:12=3,819.10^{-23}$
Đúng 1
Bình luận (0)
Nguyên tử X có số hạt p, n, e là 34 → p + n + e = 34 → 2p + n = 34 (1)
Trong đó, số hạt mang điện nhiều hơn số hạt không mang điện là 10 → p + e – n = 10 → 2p – n = 10 (2)
Từ (1) và (2) → p = 11, n = 12
Số khối A = p + n = 11 + 12 = 23
Đúng 0
Bình luận (0)
64/Phân tử MX3 có tổng số hạt proton, notron, electron 238, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 70 hạt. Số hạt mang điện trong nguyên tử M trong nguyên tử X là 18 hạt. Số hạt ko mang điện trong nguyên tử X nhiều hơn số hạt mang điện dương là 1. Viết cấu hình electron tương ứng của M và X.65/Phân tử M2X có tổng số hạt proton, notron, electron 140, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 44. Số khối của nguyên tử M nhiều hơn số khối của nguyên tử X...
Đọc tiếp
64/Phân tử MX3 có tổng số hạt proton, notron, electron = 238, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 70 hạt. Số hạt mang điện trong nguyên tử M trong nguyên tử X là 18 hạt. Số hạt ko mang điện trong nguyên tử X nhiều hơn số hạt mang điện dương là 1. Viết cấu hình electron tương ứng của M và X.
65/Phân tử M2X có tổng số hạt proton, notron, electron =140, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 44. Số khối của nguyên tử M nhiều hơn số khối của nguyên tử X là 23. Tổng số hạt trong M nhiều hơn tổng số hạt trong X là 34. Viết cấu hình electron tương ứng của M và X.
Trong tự nhiên,A có hai đồng vị là X và Y.Đồng vị Y hơn đồng vị X một notron.X có dạng ion là X2+,có tổng số hạt proton,notron,electron là 36,trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12.Tính % đồng vị Y biết A có nguyên tử khối trung bình là 24,32.
A.68
B.32
C.79
D.21
Có \(\left\{{}\begin{matrix}2p_X+n_X=36\\2p_X-n_X=12\end{matrix}\right.\)
=> pX = eX = 12; nX = 12
=> AX = 24
=> AY = 25
Gọi a% là phần trăm đồng vị X
Có \(\dfrac{24.a+25\left(100-a\right)}{100}=24,32\)
=> a% = 68
=> Phần trăm đồng vị Y = 32%
=> B
Đúng 1
Bình luận (0)