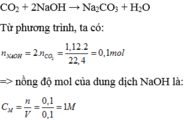Cho 2,24l khí \(SO_2\) (đktc) tác dụng vừa đủ với 100 ml dung dịch NaOH tạo thành muối trung hòa tính nồng độ mol/l của dung dịch NaOH

Những câu hỏi liên quan
Biết rằng 1,12 lít khí cacbon đioxit (đktc) tác dụng vừa đủ với 100 ml dung dịch NaOH tạo ra muối trung hòa. Nồng độ mol của dung dịch NaOH đã dùng là
A. 1M
B. 2M
C. 0,1M
D. 0,2M
Biết rằng 1,12 lít khí cacbon đioxit (đktc) tác dụng vừa đủ với 100 ml dung dịch NaOH tạo ra muối trung hoà. Tính nồng độ mol của dung dịch NaOH đã dùng.
n NaOH = 2 n CO 2 = 1,12x2 /22,4 = 0,1 (mol)
Nồng độ mol của dung dịch NaOH là 1M.
Đúng 0
Bình luận (0)
Biết rằng 1,2395 lít khí carbon dioxide (CO2) ở đkc tác dụng vừa đủ với 100 ml dung dịch NaOH tạo muối Na2CO3 và nước. a)Tính khối lượng muối tạo thành b) Tính nồng độ mol dung dịch NaOH đã dùng
PT: \(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
Ta có: \(n_{CO_2}=\dfrac{1,2395}{24,79}=0,05\left(mol\right)\)
a, Theo PT: \(n_{Na_2CO_3}=n_{CO_2}=0,05\left(mol\right)\Rightarrow m_{Na_2CO_3}=0,05.106=5,3\left(g\right)\)
b, \(n_{NaOH}=2n_{CO_2}=0,1\left(mol\right)\)
\(\Rightarrow C_{M_{NaOH}}=\dfrac{0,1}{0,1}=1\left(M\right)\)
Đúng 3
Bình luận (0)
Bài 1. Cho 16g CuO tác dụng vừa đủ với 500ml dung dịch HCLa, Tính khối lượng muối tạo thành?b, Tính nồng độ mol của dd HCL pứ?Bài 5. Trung hòa 200ml dung dịch NaOH 1M cần vừa đủ 400ml dd H2SO4a, Tính nồng độ mol của dd H2SO4b, Tính nồng độ mol của dd muối sau pức, Tính kl muối tạo thànhGiúp mình với!Mình đang cần gấp
Đọc tiếp
Bài 1. Cho 16g CuO tác dụng vừa đủ với 500ml dung dịch HCL
a, Tính khối lượng muối tạo thành?
b, Tính nồng độ mol của dd HCL pứ?
Bài 5. Trung hòa 200ml dung dịch NaOH 1M cần vừa đủ 400ml dd H2SO4
a, Tính nồng độ mol của dd H2SO4
b, Tính nồng độ mol của dd muối sau pứ
c, Tính kl muối tạo thành
Giúp mình với!Mình đang cần gấp
Bài 1
\(a,n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\\ CuO+2HCl\xrightarrow[]{}CuCl_2+H_2O\\ n_{CuCl_2}=n_{CuO}=0,2mol\\ m_{CuCl_2}=0,2.135=27\left(g\right)\\ b.n_{HCl}=0,2.2=0,4\left(mol\right)\\ C_{MHCl}=\dfrac{0,4}{0,5}=0,8\left(M\right)\)
Đúng 2
Bình luận (0)
Bài 5
\(a,n_{NaOH}=0,2.1=0,2\left(mol\right)\\ 2NaOH+H_2SO_4\xrightarrow[]{}Na_2SO_4+2H_2O\\ n_{H_2SO_4}=0,2:2=0,1\left(mol\right)\\ C_{MH_2SO_4}=\dfrac{0,1}{0,4}=0,25\left(M\right)\\ b,n_{Na_2SO_4}=0,2:2=0,1\left(mol\right)\\ C_{MNa_2SO_4}=\dfrac{0,1}{0,2+0,4}=\dfrac{1}{6}\left(M\right)\\ c,m_{Na_2SO_4}=0,1.142=14,2\left(g\right)\)
Đúng 2
Bình luận (0)
biết rằng 1,12 lít khí cacbon didoxxit ( đktc ) tác dụng vừa đủ với 100ml dung dịch NaOH tạo ra muối trung hòa . a) viết phương trình hóa học b) tính nồng độ mol của dung dịch NaOH đã dùng C) Tính C% của muối có trong dd sau lư ( D dd nạo = 1,2g/lít)
giúp e vs ạ!!!! Em cần gấp!!!
a) \(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
b) \(n_{CO_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Theo PT: \(n_{NaOH}=2n_{CO_2}=0,1\left(mol\right)\)
=> \(CM_{NaOH}=\dfrac{0,1}{0,1}=1M\)
c) Sửa đề DNaOH = 1,2g/ml
\(m_{ddsaupu}=0,05.44+100.1,2=122,2\left(g\right)\)
\(n_{Na_2CO_3}=n_{CO_2}=0,05\left(mol\right)\)
=> \(C\%_{Na_2CO_3}=\dfrac{0,05.106}{122,2}.100=4,34\%\)
Đúng 2
Bình luận (0)
Cho 2,24 lít khí CO2 (đktc) tác dụng vừa đủ với 100ml dung dịch NaOH tạo muối trung hoà.
a) Tính nồng độ phần trăm dung dịch sau phản ứng
b) Tính nồng độ mol NaOH đã dùng
nCO2= 2,24 :22,4= 0,1 Mol
a) lập pthh của pư
CO2 +2 NaOH -------->Na2CO3 + H2O
1mol 2mol 1mol 1mol
0,1mol 0,2mol 0,1mol 0,1mol
mCO2 =0,1 .44= 4,4 gam
mNa2CO3 = 0,1 . 106 =10,6 gam
mH2O= 0,1 . 18 = 1,8 gam
mdd sau pư = mct + m dung môi = 4,4+1,8 =6,2 gam
C%Na2CO3 =( mct /mdd ). 100% = (10,6 /6,2 ) .100% =170,97 %
b) CmNaOH = n/ v = 0,2 /0,1 =2 mol/lít
Đúng 2
Bình luận (0)
Cho 2,8 l khí cacbon điôxít ở điều kiện tiêu chuẩn tác dụng với 100 ml dung dịch KOH nồng độ a m vừa đủ để tạo muối trung hòa tìm a và tính nồng độ mol lít của dung dịch thu được sau phản ứng cho rằng thể tích của dung dịch thay đổi không đáng kể
\(n_{CO_2}=\dfrac{2,8}{22,4}=0,125\left(mol\right)\)
PTHH :
\(CO_2+2KOH\rightarrow K_2CO_3+H_2O\)
0,125 0,25 0,125
\(a,C_{M\left(KOH\right)}=\dfrac{0,25}{0,1}=2,5\left(M\right)\)
\(b,C_{M\left(K_2CO_3\right)}=\dfrac{0,125}{0,1}=1,25\left(M\right)\)
Đúng 1
Bình luận (0)
Cho 200 ml dung dịch CH3COOH 2M tác dụng hoàn toàn và vừa đủ với 100 ml dung dịch NaOH. Tính nồng độ mol của dung dịch NaOH
CH3COOH+NaOH->CH3COONa+H2O
0,4---------------0,4
n CH3COOH=0,4 mol
=>CM NaOH=\(\dfrac{0,4}{0,1}=4M\)
Đúng 5
Bình luận (0)
Trung hòa vừa đủ 200 ml dung dịch NaOH với 300 ml dung dịch HNO3 1M Tính nồng độ mol dung dịch NaOH Tính khối lượng muối thu được Tính nồng độ muối thu được sau phản ứng GIÚP MÌNH VỚI!
300ml = 0,3l
\(n_{HNO3}=1.0,3=0,3\left(mol\right)\)
Pt : \(NaOH+HNO_3\rightarrow NaNO_3+H_2O|\)
1 1 1 1
0,3 0,3 0,3
\(n_{NaOH}=\dfrac{0,3.1}{1}=0,3\left(mol\right)\)
200ml = 0,2l
\(C_{M_{NaOH}}=\dfrac{0,3}{0,2}=1,5\left(M\right)\)
\(n_{NaNO3}=\dfrac{0,3.1}{1}=0,3\left(mol\right)\)
⇒ \(m_{NaNO3}=0,3.85=25,5\left(g\right)\)
Sau phản ứng :
\(V_{dd}=0,2+0,3=0,5\left(l\right)\)
\(C_{M_{NaNO3}}=\dfrac{0,3}{0,5}=0,6\left(M\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (1)
\(n_{HNO_3}=0,3\left(mol\right)\)
\(NaOH+HNO_3\rightarrow NaNO_3+H_2O\)
Theo PT: \(n_{NaOH}=n_{NaNO_3}=n_{HNO_3}=0,3\left(mol\right)\)
\(\Rightarrow CM_{NaOH}=\dfrac{0,3}{0,2}=1,5M\)
\(m_{NaNO_3}=0,3.85=25,5\left(g\right)\)
Đúng 1
Bình luận (1)