Cho 1 oxit kim loại hóa trị X tác dụng vừa đủ với dung dịch H2SO4 20% sau p/ứ kết thúc thu được dung dịch muối sunfat 22,64%.Tìm oxit kim loại trên

Những câu hỏi liên quan
Hòa tan hoàn toàn 1 lượng Oxit kim loại hóa trị II bằng 1 lượng vừa đủ dung dịch H2SO4 20% . Sau phản ứng thu được muối sun phát có nồng độ là 22,64% . Xác định công thức hóa học của Oxit kim loại trên
Gọi CT của oxit : RO
n RO = a ( mol )
PTHH:
RO + H2SO4 ====> RSO4 + H2O
a--------a------------------a
theo pthh:
n H2SO4 = n RSO4 = n RO = a ( mol )
Có: n H2SO4=a ( mol ) => m H2SO4 = 98a ( g )
=> m dd H2SO4 20% = 490a ( g )
BTKL: m dd sau phản ứng = a ( R + 16 ) + 490a = aR + 506a ( g )
Lại có :
n RSO4 = a ( mol ) => m RSO4 = aR + 96a
=> \(\dfrac{aR+96a}{aR+506a}=\dfrac{22,64}{100}\Rightarrow\dfrac{a\left(R+96\right)}{a\left(R+506\right)}=\dfrac{22,64}{100}\)
\(\Rightarrow R=24\left(Mg\right)\)
Vậy CT: MgO
Đúng 0
Bình luận (0)
Cho kim loại sắt Fe tác dụng vừa đủ với 147gam dung dịch H2SO4 có nồng độ 20℅ thu được muối và khí hidro. Dân toàn bộ khí hidro qua 16g oxit kim loại có hóa trị III. Xác định công thức hóa học của oxit cầu cíu các cao nhân
\(n_{H_2SO_4}=\dfrac{147.20\%}{98}=0,3\left(mol\right)\\ Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ n_{H_2}=n_{axit}=0,3\left(mol\right)\\ Đặt:A_2O_3\\ A_2O_3+3H_2\rightarrow\left(t^o\right)2A+3H_2O\\ n_{oxit}=\dfrac{n_{H_2}}{3}=\dfrac{0,3}{3}=0,1\left(mol\right)\\ M_{oxit}=\dfrac{16}{0,1}=160\left(\dfrac{g}{mol}\right)=2M_A+48\\ \Rightarrow M_A=56\left(\dfrac{g}{mol}\right)\\ \Rightarrow A:Sắt\left(Fe=56\right)\\ \Rightarrow Oxit:Fe_2O_3\)
Đúng 1
Bình luận (0)
Cho X là hỗn hợp của 3 chất gồm kim loại M, oxit và muối sunfat của kim loại M. Biết M có hóa trị II không đổi trong các hợp chất. Chia 29,6 gam X thành hai phần bằng nhau: – Phần 1: đem hòa tan tỏng dung dịch H2SO4loãng dư thu được dung dịch A, khí B. Lượng khí B này vừa đủ để khử hết 16 gam CuO. Sau đó cho dung dịch A tác dụng với dung dịch KOH dư, đến khi kết thúc phản ứng thu được kết tủa C. Nung C đến khối lượng không đổi thì thu được 14 gam chất rắn. – Phần 2: cho tác dụng với 200 ml dung...
Đọc tiếp
Cho X là hỗn hợp của 3 chất gồm kim loại M, oxit và muối sunfat của kim loại M. Biết M có hóa trị II không đổi trong các hợp chất. Chia 29,6 gam X thành hai phần bằng nhau:
– Phần 1: đem hòa tan tỏng dung dịch H2SO4loãng dư thu được dung dịch A, khí B. Lượng khí B này vừa đủ để khử hết 16 gam CuO. Sau đó cho dung dịch A tác dụng với dung dịch KOH dư, đến khi kết thúc phản ứng thu được kết tủa C. Nung C đến khối lượng không đổi thì thu được 14 gam chất rắn.
– Phần 2: cho tác dụng với 200 ml dung dịch CuSO4 1,5M. Sau khi kết thúc phản ứng tách bỏ chất rắn, cô cạn phần dung dịch thì thu được 46 gam muối khan.
a) Viết phương trình phản ứng xảy ra và xác định kim loại M.
b) Tính phần trăm khối lượng các chất trong X.

Bảo toàn nguyên tố M: nMSO4 = 0,25mol
Bảo toàn nguyên tố Cu: nCuSO4 dư = 0,1 mol
=> M = 24 (Mg)
b.

Đúng 1
Bình luận (0)
Hoà tan 3,2g Oxit kim loại hoá trị III bằng 200g dung dịch H2SO4 loãng. Khi thêm vào hoà tan 1 oxit kim loai htri IV biết rằng hoà tan 8g oxit này bằng 300ml dd H2SO4 1M. sau p/ứ trung hoà lượng axit còn dư bằng 50g dd NaOH 24%. tìm cthỗn hợp sau phản ứng 1 lượng CaCO3 vừa đủ thấy 0,0224dm3 CO2 ở đktc sau đó cô cạn dung dịch thu được 9,36g muối sunfat khô. Tìn công thức õit kim loại và C% H2SO4
Hòa tan 1 oxit kim loại hóa trị 2 bằng dung dịch H2SO4 có nồng độ A% vừa đủ tạo ra dung dịch muối sunfat có B%.
-Nếu A% bằng 20%, B% bằng 22,64% thì kim loại cần tìm là bao nhiêu
Gọi CTHH của oxit kim loại là AO:
Ta có: AO+H2SO4--> ASO4+ H2O;
giả sử số mol H2SO4 là 1 mol ;
ta có mmuối sunfat/ mdd=22,64%;
<--> (MA+96) /MA +16+ 98/20% =22,64
--> MA=24 --> A là Mg
Đúng 0
Bình luận (0)
Gọi CTHH của oxit : MO
Đặt: nMO= 1 mol
MO + H2SO4 --> MSO4 + H2O
1_____1__________1
mH2SO4= 1*98=98g
mdd H2SO4= 98*100/20=490g
mdd sau phản ứng= mMO + mddH2SO4= 1(M+16) + 490= M + 506 g
mMSO4= M+96 g
C%MSO4= (M+96)/(M+506)*100%= 22.64%
=> M= 24 (Mg)
Vậy: kim loại cần tìm là : Magie
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn một oxit kim loại có hóa trị II bằng dung dịch
H
2
S
O
4
có nồng độ 14,00% vừa đủ thì thu được một dung dịch muối có nồng độ 16,22%. Oxit kim loại hóa trị II trên là A. FeO B. CuO C. MgO D. ZnO
Đọc tiếp
Hòa tan hoàn toàn một oxit kim loại có hóa trị II bằng dung dịch H 2 S O 4 có nồng độ 14,00% vừa đủ thì thu được một dung dịch muối có nồng độ 16,22%. Oxit kim loại hóa trị II trên là
A. FeO
B. CuO
C. MgO
D. ZnO
Chọn C
Gọi công thức của oxit hóa trị II là RO
Đặt mol RO = 1 (mol)
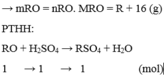
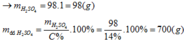
![]()
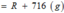
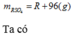

Vậy công thức của oxit kim loại là MgO
Đúng 0
Bình luận (0)
cho oxit kim loại A tác dụng với H2SO4 10% vừa đủ thu đc 15,09% muối
a, tìm công thức oxit hóa trị I-->III
b,cô cạn 159,05g dung dịch muối thu đc 37,5g tinh thể.tìm ct tinh thể
Hòa tan một lượng oxit kim loại hóa trị 2 vào một lượng dung dịch H2SO4 20% vừa đủ để tạo thành dung dịch muối sunfat 22,64%. Tìm CTHH của oxit kim loại đó
Bài giải:
Gọi công thức cần tìm là RO có số mol là 1
PTHH: RO + H2SO4 ---> RSO4 + H2O
Khối lượng H2SO4 đã dùng :98(g)
Khối lượng dung dịch axit ban đầu:
98:20%=490(g)
Khối lượng dung dịch sau phản ứng:
490+(MR+16).1=MR+506
Nồng độ của dung dịch muối sau phản ứng:
\(\dfrac{M_R+96}{M_R+506}.100\%=22,64\%\)
Từ đó ta suy ra được MR=24. CTHH của oxit cần dùng là: MgO
Đúng 0
Bình luận (0)
Cho m gam hỗn hợp kim loại có hóa trị không đổi thành hai phần bằng nhau. Phần I cho tác dụng hoàn toàn với dung dịch H2SO4 vừa đủ thu đượ 4,48l khí H2 (đktc) và m1 gam muối sunfat khan. Phần II cho tác dụng hoàn toàn với oxi thu được m2 gam oxit. Giá trị m1 - m2 có giá trị là
PTHH:
\(M+H_2SO_4\rightarrow M_2\left(SO_4\right)_x+H_2\left(1\right)\)
\(M+O_2\rightarrow M_2O_x\left(2\right)\)
Phần 1:
\(n_{SO_4}=n_{H_2SO_4}=n_{H_2}=0,2\left(mol\right)\)
Ta có: \(m_{M_2\left(SO_4\right)_x}=m_M+m_{SO_4}\Leftrightarrow m_1=\dfrac{m}{2}+0,2.96=\dfrac{m}{2}+19,2\left(3\right)\)
Phần 2:
Ta có: \(m_O=m_{M_2O_x}-m_M=m_2-\dfrac{m}{2}\Rightarrow n_O=\dfrac{m_2}{16}-\dfrac{m}{32}\left(mol\right)\)
Lại có: \(n_{SO_4\left(1\right)}=x.n_{M_2\left(SO_4\right)_n}=\dfrac{x}{2}.n_M=x.n_{M_2O_x}=n_{O\left(2\right)}\)
\(\Leftrightarrow0,2=\dfrac{m_2}{16}-\dfrac{m}{32}\)
\(\Leftrightarrow3,2=m_2-\dfrac{m}{2}\)
\(\Leftrightarrow m_2=\dfrac{m}{2}+3,2\left(4\right)\)
Từ \(\left(3\right)\) và \(\left(4\right)\Rightarrow m_1-m_2=16\)
Đúng 1
Bình luận (0)



















