Tính toán và trình bày phương xác định nồng độ % và nồng độ mol của 1 mẫu dd CuSO4 trong phòng thí nghiệm

Những câu hỏi liên quan
Trình bày phương pháp thực nghiệm để xác định nồng độ phần trăm và nồng độ ml của mẫu dung dịch C u S O 4 có sẵn trong phòng thí nghiệm.
* Phương pháp xác định nồng độ phần trăm dung dịch C u S O 4
- Cân một lượng dung dịch C u S O 4 xác định.
- Cô cạn dung dịch cho đến khi thu được chất rắn màu trắng đó là C u S O 4 . Sau đó đem cân lượng muối sau khi cô cạn này ta được số liệu là mct.
- Áp dụng công thức: 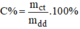 ta sẽ tính C% của dung dịch
C
u
S
O
4
.
ta sẽ tính C% của dung dịch
C
u
S
O
4
.
* Phương pháp xác định nồng độ mol của dung dịch C u S O 4 :
- Đong 1 thể tích dung dịch C u S O 4 xác định, đem cân lượng dung dịch đó.
- Sau đó dùng công thức 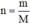 để tính số mol của
C
u
S
O
4
.
để tính số mol của
C
u
S
O
4
.
- Tính nồng độ mol của dung dịch
C
u
S
O
4
bằng công thức: 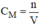
Đúng 0
Bình luận (0)
Bài 1:Thế nào là oxit?Cho 2 ví dụ minh hoạBài 2:Viết công thức tính nồng độ mol của dung dịch.Hãy tính nồng độ mol của 2,5 mol CuSO4 trong 4 lít dung dịchBài 3:Lập phương trình hoá học biễu diễn phản ứng sau và xác định loại phản ứng?a.Đồng(II) oxit+khí hidro- đồng+nướcb.Lưu huỳnh trioxit+nước - axit sunfuricBài 4:a.Hãy gọi tên các hợp chất sau:HNO3;Ca(OH)2b.Viết công thức hoá học của muối có tên sau:-Kali sunfat-Natri hidrocacbonat
Đọc tiếp
Bài 1:Thế nào là oxit?Cho 2 ví dụ minh hoạ
Bài 2:Viết công thức tính nồng độ mol của dung dịch.Hãy tính nồng độ mol của 2,5 mol CuSO4 trong 4 lít dung dịch
Bài 3:Lập phương trình hoá học biễu diễn phản ứng sau và xác định loại phản ứng?
a.Đồng(II) oxit+khí hidro-> đồng+nước
b.Lưu huỳnh trioxit+nước -> axit sunfuric
Bài 4:
a.Hãy gọi tên các hợp chất sau:HNO3;Ca(OH)2
b.Viết công thức hoá học của muối có tên sau:
-Kali sunfat
-Natri hidrocacbonat
Bài 1: Bạn tự học nhé
Bài 2:
\(C_M=\dfrac{n}{V}=\dfrac{2,5}{4}=0,625M\)
Bài 3:
\(a,CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\\ b,SO_3+H_2O\rightarrow H_2SO_4\)
Bài 4:
a, HNO3 - axit nitric
Ca(OH)2 - canxi hiđroxit
b, K2SO4
NaHCO3
Đúng 7
Bình luận (0)
mình làm nốt bài 1 :)))
oxit là 1 hợp chất trong đó có 1 hay nhiều nguyên tử Oxi liên kết với 1 đơn chất
VD : CO2 , FeO
Đúng 1
Bình luận (0)
Hoà tan hoàn toàn 11,2g bột sắt vào một lượng vừa đủ dd CuSO4 có nồng độ 0,1M
a. Tính thể tích dd CuSO4
b. Nếu cho 11,2g bột sắt vào 2,5 lít dd CuSO4 có nồng độ 0,1M. Xác định nồng độ mol các chất có trong dd sau có phản ứng kết thúc. (Giả thiết rằng thể tích của dd sau phản ứng thấy đổi không đáng kể)
Xem chi tiết
a)
\(Fe + CuSO_4 \to FeSO_4 + Cu\)
Theo PTHH :
\(n_{CuSO_4} = n_{Fe} = \dfrac{11,2}{56} = 0,2(mol)\\ \Rightarrow V_{dd\ CuSO_4} = \dfrac{0,2}{0,1} = 2(lít)\)
b)
\(n_{CuSO_4} = 0,1.2,5 = 0,25(mol) > n_{Fe}= 0,2\) nên \(CuSO_4\) dư.
Ta có :
\(n_{CuSO_4\ pư} = n_{FeSO_4} = n_{Fe} = 0,2(mol)\\ \Rightarrow n_{CuSO_4\ dư} = 0,25 - 0,2 = 0,05(mol)\)
Vậy :
\(C_{M_{CuSO_4}} = \dfrac{0,05}{2,5} = 0,02M\\ C_{M_{FeSO_4}} = \dfrac{0,2}{2,5} = 0,08M\)
Đúng 1
Bình luận (0)
trình bày phương pháp thực nghiệm để xác định nồng độ % và nồng độ mol của một mẫu thử dung dịch CuSO4
trình bày phương pháp thực nghiệm để xác định nồng độ % và nồng độ mol của một mẫu thử dung dịch CuSO4
Trả lời
a) Phương pháp xác định nồng độ phần trăm của dung dịch CuSO4 .
– Cân lấy một lượng dung dịch CuSO4 tuỳ ý, ví dụ 100 g.
– Cô cạn dung dịch cho đến khi thu được chất rắn màu trắng là CuSO4.
– Cân muối CuSO4 thu được sau khi cô cạn, thí dụ được 8 g.
– Tính nồng độ phần trăm của dung dịch CuSO4 ban đầu :
C%=100%×8100=8%
b) Phương pháp xác định nồng độ mol của dung dịch CuSO4 :
– Cân lấy một lượng dung dịch CuSO4 tuỳ ý rồi đo thể tích. Thí dụ, cân lấy 100 g dung dịch CuSO4 như trong thí nghiệm trên, đo thể tích được 90 ml.
– Tính số mol CuSO4 có trong 90 ml (hoặc 100 g) dung dịch là :
nCuSO4=8160=0,05(mol)
– Tính nồng độ mol của dung dịch CuSO4 :
Đúng 0
Bình luận (0)
a) Phương pháp xác định nồng độ phần trăm của dung dịch CuSO4 .
– Cân lấy một lượng dung dịch CuSO4 tuỳ ý, ví dụ 100 g.
– Cô cạn dung dịch cho đến khi thu được chất rắn màu trắng là CuSO4.
– Cân muối CuSO4 thu được sau khi cô cạn, thí dụ được 8 g.
– Tính nồng độ phần trăm của dung dịch CuSO4 ban đầu :
C% = (100%×8):100=8%
b) Phương pháp xác định nồng độ mol của dung dịch CuSO4 :
– Cân lấy một lượng dung dịch CuSO4 tuỳ ý rồi đo thể tích. Thí dụ, cân lấy 100 g dung dịch CuSO4 như trong thí nghiệm trên, đo thể tích được 90 ml.
– Tính số mol CuSO4 có trong 90 ml (hoặc 100 g) dung dịch là :
\(_{n_{CuSO4}}\) = 8:160=0,05(mol)
– Tính nồng độ mol của dung dịch CuSO4 :
\(_{C_M}\)= (1000×0,05) : 90 ≈ 0,56(mol/l)
Đúng 0
Bình luận (0)
Ở nhiệt độ phòng, người ta xác định tốc độ đầu của phản ứng hoá học xảy ra giữa hai chất A và B thu được kết quả sau:
Thí nghiệm
Nồng độ đầu A (M)
Nồng độ đầu của B (M)
Tốc độ đầu của phản ứng (mol-1J. S-1)
1
0,01
0,02
0,014
2
0,01
0,01
0,007
3
0,04
0,02
0,224
Biểu thức mô tả sự phụ thuộc tốc độ phản ứng vào nồng độ A và B là: A. v k. CA. CB ...
Đọc tiếp
Ở nhiệt độ phòng, người ta xác định tốc độ đầu của phản ứng hoá học xảy ra giữa hai chất A và B thu được kết quả sau:
| Thí nghiệm |
Nồng độ đầu A (M) |
Nồng độ đầu của B (M) |
Tốc độ đầu của phản ứng (mol-1J. S-1) |
| 1 |
0,01 |
0,02 |
0,014 |
| 2 |
0,01 |
0,01 |
0,007 |
| 3 |
0,04 |
0,02 |
0,224 |
Biểu thức mô tả sự phụ thuộc tốc độ phản ứng vào nồng độ A và B là:
A. v = k. CA. CB
B. v = k. CA2.Cb2
C. v = k. CA2. CB
D. v = k. CA .CB2
Đáp án C
So với TN1, TN2 có nồng độ chất B giảm 2 lần, nồng độ chất A giữ nguyên, làm cho tốc độ phản ứng giảm 2 lần. Kết luận tốc độ phản ứng tỉ lệ thuận với nồng độ chất B.
So với TN1, TN3 có nồng độ chất A tăng 4 lần, nồng độ chất B giữ nguyên, làm cho tốc độ phản ứng tăng 16 lần. Kết luận tốc độ phản ứng tỉ lệ thuận với bình phương nồng độ chất A
Đúng 0
Bình luận (0)
Cho 0,6 mol CuSO4 trong 500ml dung dịch CuSO4 . Tính nồng độ mol của dd CuSO4
Đổi 500ml = 0,5l
\(C_{M\left(C\text{uS}O_4\right)}=\dfrac{n}{V_{\text{dd}}}=\dfrac{0,6}{0,5}=1,2M\)
Đúng 0
Bình luận (0)
hãy tính nồng độ mol của dd khi cho 400g CuSO4 trong 400ml dd CuSO4
\(n_{CuSO_4}=\dfrac{400}{160}=2,5\left(mol\right)\)
\(400ml=0,4\left(l\right)\)
\(C_{M_{CuSO_4}}=\dfrac{2,5}{0,4}=6,25\left(M\right)\)
Đúng 6
Bình luận (19)
\(n_{CuSO_4}=\dfrac{400}{160}=2,5\left(mol\right)\\ C_M=\dfrac{2,5}{0,4}=6,25M\)
Đúng 3
Bình luận (2)
\(400ml=0,4l\)
\(C_{M_{CuSO_4}}=\dfrac{400:160}{0,4}=6,25\left(M\right)\)
Đúng 4
Bình luận (0)
Hãy nêu phương pháp thực nghiệm xác định nồng độ mol của mỗi chất trong dung dịch hỗn hợp gồm Na2CO3 và NaHCO3
Hãy nêu phương pháp thực nghiệm xác định nồng độ mol của mỗi chất trong dung dịch hỗn hợp gồm Na2CO3 và NaHCO3





















