Tính khối lượng CaF2 cần dùng để điều chế 200g ddịch axit flohidric nồng độ 5%. Biết hiệu suất phản ứng 70%.
Cho biết H = 1, O = 16, F=19, Al = 27, Cl = 35,5 ; K = 39, Ca = 40 , Mn = 55, Zn = 65,
Br = 80, Ag = 108, I = 127; Cu=64
Tính khối lượng CaF2 cần dùng để điều chế 2,5kg dung dịch axit flohidric nồng độ 40%. Biết hiệu suất phản ứng là 80 %.
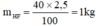
Phương trình hóa học của phản ứng:
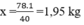
mCaF2 cần dùng: 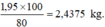
Khối lượng C a F 2 cần dùng để điều chế 200 gam dung dịch axit flohidric nồng độ 40% (hiệu suất phản ứng bằng 80%) là
A. 312 gam.
B. 156 gam.
C. 195 gam.
D. 390 gam.
Chọn đáp án C
m H F = 200 . 40 100 = 80 (gam) => n H F = 80 20 = 4 (mol)
m C a F 2 = 4 . 1 2 . 78 . 100 80 = 195 (gam)
Khối lượng CaF2 cần dung để điều chế 400 gam dung dịch axit flohidric nồng độ 40% (hiệu suất phản ứng bằng 80%) là
A. 624 gam
B. 312 gam
C. 780 gam
D. 390 gam
Đáp án D
![]() .100 = 40% => mHF =160 (g) => n HF = 8 (mol)
.100 = 40% => mHF =160 (g) => n HF = 8 (mol)
CaF2 + H2SO4 → CaSO4 + 2HF
4 ← 8 (mol)
Do H% = 60%=> ![]() = 5 mol
= 5 mol
m = 5. (40+19.2) = 390 (g)
Khối lượng C a F 2 cần dùng để điều chế 400 gam dung dịch axit flohiđric nồng độ 40% (hiệu suất phản ứng bằng 80%) là
A. 624 gam
B. 312 gam
C. 780 gam
D. 390 gam
Chọn đáp án D
m H F = 400 . 40 100 = 160 (gam) → n H F = 160 20 = 8 (mol)
Bảo toàn F có: n H F = 2. n C a F 2 → n C a F 2 = 4 mol.
m C a F 2 = 4 , 78 80 % = 390 (gam)
Khối lượng CaF 2 cần dùng để điều chế 2,5kg dung dịch HF 40% (Biết hiệu suất phản ứng là 80%)
A. 1,95 kg.
B. 2,4375 kg.
C. 1,56 kg.
D. 4,88 kg.
1. Tính khối lượng CaF2 cần dùng để điều chế 2,5 kg dung dịch axit Flohidric nồng độ 40%.
2. Hòa tan 11 gam hỗn hợp bột sắt và nhôm trong dung dịch HCl thu được 8,96 lit khí (điều kiện tiêu chuẩn).
a. Xác định thành phần phần trăm về khối lượng của mỗi kim loại trong hỗn hợp.
b. Tính thể tích dung dịch HCl 2M đã dùng.
![]()
(Cho Ca = 40; F = 19; H =1; Fe = 56; Al = 27)
\(1,n_{HF}=\dfrac{2,5.40\%}{100\%.20}=0,05(kmol)\\ PTHH:CaF_2+H_2SO_4\to CaSO_4+2HF\\ \Rightarrow n_{CaF_2}=0,025(kmol)\\ \Rightarrow m_{CaF_2}=0,025.78=1,95(kg)\\ 2,\text {Đặt }\begin{cases} n_{Fe}=x(mol)\\ n_{Al}=y(mol) \end{cases} \Rightarrow 56x+27y=11(1)\\ n_{H_2}=\dfrac{8,96}{22,4}=0,4(mol)\\ PTHH:Fe+2HCl\to FeCl_2+H_2\\ 2Al+6HCl\to 2AlCl_3+3H_2\\ \Rightarrow x+1,5y=0,4(2)\\ (1)(2)\Rightarrow \begin{cases} x=0,1(mol)\\ y=0,2(mol) \end{cases} \Rightarrow \begin{cases} \%_{Fe}=\dfrac{0,1.56}{11}.100\%=50,91\%\\ \%_{Al}=100\%-50,91\%=49,09\% \end{cases}\)
\(b,\Sigma n_{HCl}=2n_{Fe}+3n_{Al}=0,2+0,6=0,8(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,8}{2}=0,4(l)\)
tính khối lượng CaF2 cần dùng để điều chế 2,5 kg dung dịch axit flohiđric nồng độ 40% . Biết hiệu suất phản ứng là 80% .
mHF =\(\frac{40.2,5}{100}\) = 1kg
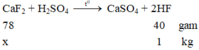
Phương trình phản ứng hóa học:
CaF2 + H2SO4 ---> CaSO4 + 2HF
78kg 40kg
X kg 1 kg
mCaF2 cần dùng: \(\frac{1.78}{40}.\frac{100}{80}\) = 2,4375 kg
mHF = = 1kg
Phương trình phản ứng hóa học:
CaF2 + H2SO4 CaSO4 + 2HF
78kg 40kg
X kg 1 kg
cần dùng:
= 2,4375 kg
ở đâu ra mà bạn tính được 78kg và 40kg vậy?
Cho sơ đồ phản ứng sau : KClO3——-> KCl + O2 a, hãy hoàn thành phương trình phản ứng b, Tính số mol và khối lượng Kaliclorat (KClO3) cần dùng để điều chế 11,2 lít khí oxi(O2) (đktc) ( biết : K = 39, Cl= 35,5 ,O=16)
\(n_{O_2\left(dktc\right)}=\dfrac{V}{22,4}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\\ PTHH:2KClO_3-^{t^o}>2KCl+3O_2\)
tỉ lệ 2 : 2 : 3
n(mol) `1/3`<------------`1/3`<-----`0,5`
\(m_{KClO_3}=n\cdot M=\dfrac{1}{3}\cdot\left(39+35,5+16\cdot3\right)\approx40,83\left(g\right)\)
Câu 11: (2,0 điểm) Đế oxi hóa 6,75 gam nhôm người ta dùng 3,36 lít khí oxi (đktc).
a. Tính khối lượng chất dư.
b. Tính khối lượng KMNO4 cần dùng để điều chế lượng oxi dùng trong phản ứng trên.
(Biết NTK: CI = 35,5; K = 39; Cu = 64; 0= 16, Al-27; Mn= 55)
\(n_{Al}=\dfrac{6,75}{27}=0,25mol\)
\(n_{O_2}=\dfrac{3,36}{22,4}=0,15mol\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
0,25 0,15 0
0,2 0,15 0,1
0,05 0 0,1
\(m_{dư}=m_{Aldư}=0,05\cdot27=1,35g\)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
0,3 0,15
\(m_{KMnO_4}=0,3\cdot158=47,4g\)