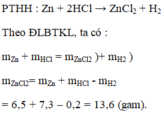Hòa tan 6,5 gam kẽm vừa đủ trong 100 gam dung dịch axit clohidric.(Biết: Zn = 65; H =1; Cl = 35,5).Nồng độ phần trăm của dung dịch muối tạo thành bằng bao nhiêu?

Những câu hỏi liên quan
Hòa tan hoàn toàn 6,5 gam kẽm vào dung dịch axit clohidric HCl có chứa 7,3 gam HCl (vừa đủ). Sau phản ứng thu được dung dịch muối kẽm clorua và 0,2 gam khí hidro.
a) Lập công thức hóa học của muối kẽm clorua. Biết kẽm clorua do hai nguyên tố là Zn và Cl tạo ra.
b) Tính khối lượng muối kẽm clorua tạo thành.
a) Lập công thức hóa học của muối kẽm clorua: Z n C l 2
b) Khối lượng muối Z n C l 2 = 6,5 + 7,3 – 0,2 = 13,6 (gam)
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn 6,5 gam kẽm vào dung dịch axit clohidric HCl có chứa 7,3 gam HCl (vừa đủ). Sau phản ứng thu được dung dịch muối kẽm clorua và 0,2 gam khí hidro,
Viết phản ứng hóa học xảy ra.
Tính khối lượng kẽm clorua Z n C l 2 tào thành.
hoà tan hoàn toàn 6,5 kim loại kẽm zn vào dung dịch axit clohidric HCL 10%(vừa đủ) tính thể tích hidro thoát ra(đktc)
nZn = 6.5/65 = 0.1 (mol)
Zn + 2HCl =>ZnCl2 + H2
0.1..............................0.1
VH2 = 0.1 * 22.4 = 2.24 (l)
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn 6,5 gam kim loại kẽm bằng 1 lượng vừa đủ dung dịch axit clohidric (HCl), sau phản ứng thu được khí Hidro và muối kẽm clorua (ZnCl2).
a) Viết phương trình hóa học xảy ra?
b) Tính thể tích khí hidro thu được sau phản ứng ở đktc?
c) Tính khối lượng HCl đã phản ứng?
a. \(n_{Zn}=\dfrac{6.5}{65}=0,1\left(mol\right)\)
PTHH : Zn + 2HCl -> ZnCl2 + H2
0,1 0,2 0,1
b. \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
c. \(m_{HCl}=0,2.36,5=7,3\left(g\right)\)
Đúng 4
Bình luận (0)
\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
\(m_{HCl}=0,2\cdot36,5=7,3g\)
Đúng 2
Bình luận (0)
Để hòa tan hết m gam Zn cần vừa đủ 200 ml dung dịch H₂SO₄ 1M. Giá trị của m là bao nhiêu? Biết H = 1 ; O = 16 ; S = 32 ; Zn = 65.A.26,0 gam.B.19,5 gam.C.13,0 gam.D.6,5 gam.
Xem chi tiết
\(n_{H_2SO_4}=0.2\left(mol\right)\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(0.2..........0.2\)
\(m_{Zn}=0.2\cdot65=13\left(g\right)\)
Đúng 1
Bình luận (0)
Hòa tan 6,5 gam Zn trong dung dịch axit HCl dư, sau phản ứng cô cạn dung dịch thì số gam muối khan thu được là (Cho H = 1, Zn = 65, Cl = 35,5) ?
ADĐLBTKL ta có:
mZn+mHCl=mMuoi+mH2
=>mMuoi=6.5+0.2*36.5-0.1*2=13.6
OK
Đúng 0
Bình luận (0)
Để hòa tan m gam kẽm cần vừa đủ 50 gam dung dịch HCl 7,3 %
a/ Viết PTPƯ
b/ Tính m
c/ Tính thể tích khí thu được ở đktc?
d/ Tính khối lượng muối tạo thành sau phản ứng ?
( Biết Zn = 65 , H = 1, Cl = 35,5 )
\(m_{HCl}=50.7,3\%=3,65\left(g\right)\\ n_{HCl}=\dfrac{3,65}{36,5}=0,1\left(mol\right)\\ PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{Zn}=n_{H_2}=n_{ZnCl_2}=\dfrac{1}{2}n_{HCl}=\dfrac{1}{2}.0,1=0,05\left(mol\right)\\ m_{Zn}=0,05.65=3,25\left(g\right)\\ V_{H_2\left(ĐKTC\right)}=0,05.22,4=1,12\left(l\right)\\ m_{ZnCl_2}=0,05.136=6,8\left(g\right)\)
Đúng 4
Bình luận (0)
mHCl=50.7,3%=3,65(g) -> nHCl=0,1(mol)
a) PTHH: Zn + 2 HCl -> ZnCl2 + H2
nH2=nZnCl2=nZn=nHCl/2= 0,1/2=0,05(mol)
b) m=mZn=0,05.65=3,25(g)
c) V(H2,đktc)=0,05.22,4=1,12(l)
d) mZnCl2= 136.0,05= 7,8(g)
Đúng 2
Bình luận (1)
cho 65 gam kẽm tác dụng vừa đủ với dung dịch axit clohidric cho 136 (g) muối clorua và giải phóng 22,4 (l) khí hidro (đktc). Tính khối lượng axit clohidric cần dùng
Ptpư Zn + 2HCl ---> ZnCl2 + H2
nH2 = 1 mol
mH2 = 2(g)
Áp dụg ĐLBTKL
mHCl = mZnCl2 +mH2 - mZn = 136 +2-65= 73(g)
Đúng 0
Bình luận (0)
ko hjeu đề bài.........bn sửa lại đj,mk lm cho
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 6,5 gam kẽm Zn vào 200 ml dung dịch axit clohidric.
a.Viết phương trình phản ứng hóa học xảy ra
b.Tính nồng độ mol của dung dịch axit clohiđric đã dùng
c.tính khối lượng O2 cần để đốt cháy hoàn toàn lượng khí vừa sinh ra ở trên
Dùm trả lời ạ! Xin cảm ơn ạ
a) \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b) \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,1-->0,2------------->0,1
=> \(C_{M\left(HCl\right)}=\dfrac{0,2}{0,2}=1M\)
c)
PTHH: 2H2 + O2 --to--> 2H2O
0,1-->0,05
=> \(m_{O_2}=0,05.32=1,6\left(g\right)\)
Đúng 3
Bình luận (0)