hoà tan 8g NaOH vào 50ml nước. tính số phần trăm của dung dịch
hoà tan 8g NaOH vào 50ml nước. tính số phần trăm của dung dịch
hoà tan 8g NaOH vào 50ml nước. tính số phần trăm của dung dịch là
Khối lượng nước (50ml) = 50g (giả định rằng mật độ nước là 1g/ml).
Tổng khối lượng dung dịch = khối lượng NaOH + khối lượng nước = 8g + 50g = 58g.
Phần trăm khối lượng NaOH = (khối lượng NaOH / tổng khối lượng dung dịch) × 100%.
Phần trăm khối lượng NaOH = (8g / 58g) × 100% ≈ 13.79%.
Đúng 0
Bình luận (0)
Câu 3: Phát biểu nào sau đây về diễn biến của phản ứng hóa học là đúng?A. Các biến đổi hóa học xảy ra chỉ có sự thay đổi trạng thái chất.B. Trong phản ứng hóa học, chỉ có liên kết giữa các nguyên tử thay đổi.C. Trong phản ứng hóa học, chỉ có khối lượng các chất trước và sau phản ứng thay đổi.D. Số lượng nguyên tử của mỗi nguyên tố trước và sau phản ứng thay đổi.
Đọc tiếp
Câu 3: Phát biểu nào sau đây về diễn biến của phản ứng hóa học là đúng?
A. Các biến đổi hóa học xảy ra chỉ có sự thay đổi trạng thái chất.
B. Trong phản ứng hóa học, chỉ có liên kết giữa các nguyên tử thay đổi.
C. Trong phản ứng hóa học, chỉ có khối lượng các chất trước và sau phản ứng thay đổi.
D. Số lượng nguyên tử của mỗi nguyên tố trước và sau phản ứng thay đổi.
Câu B đúng (Trong phản ứng hóa học, chỉ có liên kết giữa các nguyên tử thay đổi) \(\rightarrow\) Các nguyên tử kết hợp với nhau theo một cách khác để tạo thành các phân tử mới
Câu A Sai vì sự thay đổi trạng thái chất (từ rắn sang lỏng, từ lỏng sang khí) không phải là đặc trưng của phản ứng hóa học
Câu C Sai vì trong phản ứng hóa học, tổng khối lượng các chất trước và sau phản ứng luôn bằng nhau (định luật bảo toàn khối lượng)
Câu D Sai vì Số lượng nguyên tử của mỗi nguyên tố trước và sau phản ứng luôn bằng nhau (định luật bảo toàn nguyên tố)
Đúng 0
Bình luận (0)
phải lấy bao nhiêu g mỗi chất khí sau để chúng có cùng thể tích là 6,1975(L)ở điều kiện chuẩn a)CO2 b)CH4 c)O2 d) N2 e)Cl2
Số mol mỗi chất khí : \(n=\dfrac{6,1975}{24,79}=0,25\left(mol\right)\)
\(m\left(CO_2\right)=0,25.44=11\left(g\right)\)
\(m\left(CH_4\right)=0,25.16=4\left(g\right)\)
\(m\left(O_2\right)=0,25.32=8\left(g\right)\)
\(m\left(N_2\right)=0,25.28=7\left(g\right)\)
\(m\left(Cl_2\right)=0,25.71=17,75\left(g\right)\)
Đúng 1
Bình luận (0)
Bài 1: Viết phương trình phản sứng xảy ra nếu có khi cho các kim loại Mg , Al , Fe vào dung dịch ZnSO4
Bài 2: Cho 2,4g Mg tác dụng với dung dịch HCL . Tính khối lượng các chất thu được sau phản ứng .
Do 2 bài trùng lặp nên mình làm tiện thể nhé.
`Mg+ZnSO_4->MgSO_4+Zn`
`2Al+3ZnSO_4->Al_2(SO_4)_3+3Zn`
Bài 2
PTHH:
`Mg+2HCl->MgCl_2+H_2`
0,1------------0,1---------0,1 mol
`n Mg=(2,4)/24=0,1 mol
=>`m_(MgCl_2)=0,1.95=9,5g`
=>`m_(H_2)=0,1.2=0,2g`
Đúng 4
Bình luận (0)
Viết phương trình phản ứng xảy ra nếu có khi cho các kim loại Mg , Al , Fe vào dung dịch ZnSO4
+, Trong 3 kim loại Mg, Al, Fe chỉ có duy nhất Fe không phản ứng với dung dịch ZnSO4.
+, PTPU: Mg + ZnSO4 -> MgSO4 + Zn
2Al + 3ZnSO4 -> Al2(SO4)3 + 3Zn
Đúng 2
Bình luận (0)
viết phương trình phản ứng xảy ra nếu có khi cho các kim loại sau : Ba , K , Mg , Fe , Al , Cu , Ag :
a) tác dụng với O2 ;
b) tác dụng với Cl2 ;
c) tác dụng với H2SO4 ;
d) tác dụng với H2O
a)
`2Ba+O_2->2BaO`
`4K+O_2->2K_2O`
`2Mg+O_2->2MgO`
`3Fe+2O_2->Fe_3O_4` (to)
`4Al+3O_2->2Al2_O3`
`2Cu+O_2->2CuO`(to)
b)
`Ba+Cl_2->BaCl_2`
`2K+Cl_2->2KCl`
`Mg+Cl_2->MgCl_2`
`Fe+Cl_2->FeCl_3`(to)
`Al+Cl_2->AlCl_3`(to)
c)
`Ba+H_2SO_4->BaSO_4+H_2`
`K+H_2SO_4->K_2SO_4+H_2`
`Mg+H_2SO_4->MgSO_4+H_2`
`Fe+H_2SO_4->FeSO_4+H_2`
`2Al+3H_2SO_4->Al2(SO_4)_3+3H_2`
d)
`Ba+2H_2O->Ba(OH)_2+H_2`
`2K+2H_2O->2KOH+H_2`
Tham khảo.
Đúng 2
Bình luận (1)
cứ 1 mol 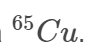 thì sẽ có bao nhiêu
thì sẽ có bao nhiêu 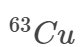
giúp mk vs ạ
Xét 1 mol Cu có x mol 65Cu và (1 – x) mol 63Cu
⟹ MCu = 65x + 63.(1 – x) = 63,546
⟹ x = 27,3%
Bạn tham khảo
Đúng 1
Bình luận (0)
đọ tan của CUSO4 ở nhiệt độ t1 laaf 20g t2 là 34.2g người ta lấy 134.2 dd bh ở nhiệt đọ t2 hạ xuống nhiết độ t1 tách ra 25g tinh thể CUSO4.nH2Otìm ct
Độ tan của CUSO4 ở nhiệt độ t1 (20°C) là 20g / 100g nước.Độ tan của CUSO4 ở nhiệt độ t2 (34.2°C) là 34.2g / 100g nước.Ta có 134.2g dung dịch ở nhiệt độ t2.
Từ độ tan ở nhiệt độ 34.2°C:34.2100=yx ⟹ y=34.2100x10034.2=xy⟹y=10034.2xGiải hệ phương trình:
Thay y vào phương trình đầu tiên:x+34.2100x=134.2gx+10034.2x=134.2g134.2100x=134.2g ⟹ x=100g100134.2x=134.2g⟹x=100g
Khi đã xác định n, ta có:CUSO4 kết tinh với n phân tử nước, với khối lượng tổng:25g=159.61g/mol⋅0.156+n⋅18g/mol25g=159.61g/mol⋅0.156+n⋅18g/mol
Tính khối lượng nước trong 134.2g dung dịch:
Đặt khối lượng nước là x, khối lượng CUSO4 là y. Ta có:
Từ độ tan ở nhiệt độ 34.2°C:34.2100=yx ⟹ y=34.2100x10034.2=xy⟹y=10034.2xGiải hệ phương trình:
Thay y vào phương trình đầu tiên:x+34.2100x=134.2gx+10034.2x=134.2g134.2100x=134.2g ⟹ x=100g100134.2x=134.2g⟹x=100g
Khi đó:
y=134.2g−100g=34.2gy=134.2g−100g=34.2gTính khối lượng nước trong 25g tinh thể CUSO4·nH2O:
Khi hạ nhiệt độ xuống t1, CUSO4 sẽ kết tinh:
Tính số mol CUSO4:
Khối lượng mol CUSO4 = 159.61g/mol.
Khi đã xác định n, ta có:CUSO4 kết tinh với n phân tử nước, với khối lượng tổng:25g=159.61g/mol⋅0.156+n⋅18g/mol25g=159.61g/mol⋅0.156+n⋅18g/mol
Ta tính ra được n:
25g=25g+n⋅18g/mol ⟹ n≈525g=25g+n⋅18g/mol⟹n≈5Vậy, công thức phân tử của CUSO4·nH2O là CUSO4·5H2O.
Đúng 0
Bình luận (1)

















