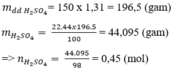Tính số mol H2SO4 có trong 400g dung dịch H2SO4 19,6%?

Những câu hỏi liên quan
Tính số mol của 300 gam dung dịch H2SO4 19,6%
Trong 400 ml dung dịch có chứa 19,6 gam H2SO4. Nồng độ mol của dung dịch thu được là ?
Mấy bài dạng này em cứ tính số mol chất đó, sau đó áp dụng công thức là ra nhé! Nhớ đổi ml ra lít
\(n_{H_2SO_4}=\dfrac{19,6}{98}=0,2\left(mol\right)\\ C_{M_{H_2SO_4}}=\dfrac{0,2}{0,4}=0,5\left(M\right)\)
Đúng 2
Bình luận (2)
Ta có: \(n_{H_2SO_4}=\dfrac{19,6}{98}=0,2\left(mol\right)\) \(\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,2}{0,4}=0,5\left(M\right)\)
Đúng 1
Bình luận (0)
3/ Cho 100g dung dịch NaOH 20% tác dụng vừa đủ với dung dịch H2SO4 19,6%.
a. Viết phương trình hóa học.
b. Tính số gam dung dịch H2SO4 19,6% cần dùng.
c. Tính nồng độ phần trăm dung dịch thu được sau phản ứng.
a) 2NaOH + H2SO4 -- Na2SO4 + 2H2O
b) \(n_{NaOH}=\dfrac{100.20}{100.40}=0,5\left(mol\right)\)
PTHH: 2NaOH + H2SO4 -- Na2SO4 + 2H2O
______0,5----->0,25------>0,25
=> mH2SO4 = 0,25.98 = 24,5 (g)
=> \(m_{ddH_2SO_4}=\dfrac{24,5.100}{19,6}=125\left(g\right)\)
c) mNa2SO4 = 0,25.142 = 35,5 (g)
mdd sau pư = 100 + 125 = 225 (g)
=> \(C\%\left(Na_2SO_4\right)=\dfrac{35,5}{225}.100\%=15,778\%\)
Đúng 1
Bình luận (0)
cho dung dịch H2SO4 98% với những dụng cụ có sẵn trong phòng thí nghiệm em hay tính toán và pha chế 200g dung dịch H2SO4 19,6%
CỨU EM VỚI Ạ
\(m_{H_2SO_4}=200.19,6\%=39,2\left(g\right)\\ m_{ddH_2SO_4\left(98\%\right)}=\dfrac{39,2}{98\%}=40\left(g\right)\\ m_{H_2O\left(bđ\right)}=40-39,2=0,8\left(g\right)\\ m_{H_2O\cdot\left(thêm\right)}=200-40=160\left(g\right)\)
pp: lấy 40 g ddH2SO4 đặc (98%), đong lấy 160 g nước, cho nước vào bình nghiệm rồi rót từ từ ddH2SO4 vào rồi khuấy đều
Đúng 4
Bình luận (0)
mH2SO4 =\(\dfrac{200.19,6}{100}=58,8\) (g)
=>mdd H2SO4 98% =\(\dfrac{39,2.100}{98}=40g\)(g)
Đúng 1
Bình luận (0)
Trộn 300 gam dung dịch H2SO4 19,6 % với 200 gam dung dịch NaOH 4% . Tính C% các chất tan có trong dung dịch ?
dung dịch H2SO4 có nồng độ 24% tính khối lượng và số mol của H2SO4 có trong 183,75g dung dịch
\(C_{\%_{H_2SO_4}}=\dfrac{m_{H_2SO_{\text{4}}}}{m_{dd}}.100\%\Rightarrow m_{H_2SO_4}=\dfrac{m_{dd}.C_{\%_{H_2SO_4}}}{100\%}=\dfrac{183,75.24\%}{100\%}=44,1\left(g\right)\)
\(n_{H_2SO_4}=\dfrac{44,1}{98}=0,45\left(mol\right)\)
Đúng 3
Bình luận (0)
Cho 150ml dung dịch H 2 SO 4 22,44% (D = 1,31g/ml). Tính số mol của H 2 SO 4 có trong dung dịch trên.
Cho 11,2g Fe vào 200g dung dịch H2SO4 19,6%. Biết rằng Fe phản ứng hết
a) Tính khối lượng H2 sinh ra sau phản ứng
b) Tính nồng độ% dung dịch H2SO4 còn lại trong dung dịch sau phản ứng
a) Số mol của 11,2 gam Fe:
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
PTHH:
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
1 : 1 : 1 : 1
0,2-> 0,2 : 0,2 : 0,2 (mol)
Khối lượng của 0,2 mol H2:
\(m_{H_2}=n.M=0,2.2=0,4\left(g\right)\)
b) khồi lượng của 0,2 mol H2SO4:
\(m_{H_2SO_4}=n.M=0,2.98=19,6\left(g\right)\)
Nồng độ phần trăm của dd:
\(C\%_{H_2SO_4}=\dfrac{m_{ct}}{m_{dd}}.100\%=\dfrac{19,6}{200}.100\%=9,8\%\)
Đúng 1
Bình luận (0)
a,tính khối lượng NaOH có trong 200ml dung dịch NaOh 1M b,tính số mol H2SO4 có trong 100ml dung dịch H2SO4 2M c,hoà tan 6g NaCl vào nước thu được 200g dung dịch tính nồng độ phần trăm của dung dịch d,tính khối lượng NaCl có trong 200g dung dịch NaCl 8%
a, \(n_{NaOH}=0,2.1=0,2\left(mol\right)\)
\(m_{NaOH}=0,2.40=8\left(g\right)\)
b, \(n_{H_2SO_4}=2.0,1=0,2\left(mol\right)\)
\(c,C\%=\dfrac{6}{200}.100\%=3\%\)
\(m_{NaCl}=\dfrac{200.8}{100}=16\left(g\right)\)
Đúng 1
Bình luận (0)