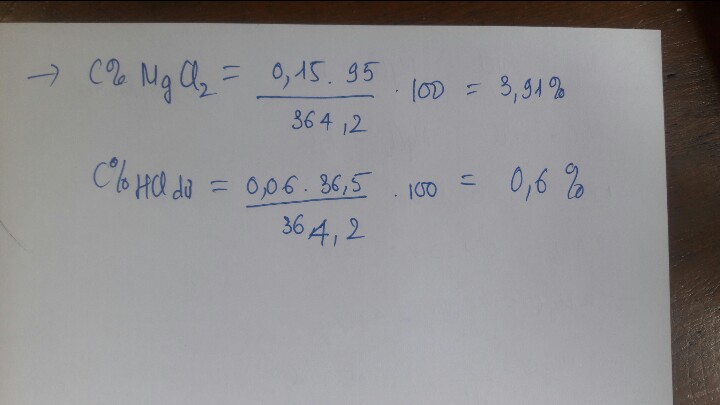Cho 5,2 g hỗn hợp x gồm MgO và MgCO³ phản ứng kết hợp với dung dịch HCl sau phản ứng thu đc 1,12 lít khi cacbonic ( đktc) a) Viết phương trình phản ứng xảy ra b) Tính khối lượng mỗi chất trong hỗn hợp x

Những câu hỏi liên quan
Cho 4,4 g hỗn hợp gồm Mg và MgO tác dụng vừa đủ với dung dịch HCl 7,3% thu được 2,24 lít khí (đkc) A) viết các phương trình phản ứng xảy ra b) tính khối lượng mỗi chất trong hỗn hợp ban đầu C) tính khối lượng dung dịch HCl phản ứng D) tính c% của dung dịch muối thu được sau phản ứng Ghi rõ ra để mình biết các câu để mình ghi nha
Hòa tan hoàn toàn 4,4 gam hỗn hợp gồm Mg và MgO bằng dung dịch axit HCl 7,3%(vừa đủ) Sau phản ứng thu được 2,24 lít khí (ở đktc).
a) viết phương trình phản ứng hóa học xảy ra
b) tính khối lượng mỗi chất trong hỗn hợp ban đầu.
C) tính khối lượng dung dịch axit HCl cần dùng
nH2=0,1(mol)
PTHH: Mg + 2 HCl -> MgCl2 + H2
0,1__________0,2___________0,1(mol)
MgO + 2 HCl -> MgCl2 + H2O
0,05____0,1___0,05(mol)
mMg=0,1. 24= 2,4(g) -> mMgO=4,4-2,4= 2(g) -> nMgO=0,05((mol)
b) %mMg= (2,4/4,4).100=54,545%
=> %mMgO=45,455%
c) nHCl=0,3(mol) -> mHCl=0,3.36,5=10,95(g)
=> mddHCl=(10,95.100)/7,3=150(g)
Đúng 3
Bình luận (0)
Cho 8,8 gam hỗn hợp X gồm Mg và MgO tác dụng với dung dịch HCl dư, phản ứng thu được 4,38 lít khí H2 (đktc)a/ Viết phương trình phản ứng hóa học b/ tính thành phần % về khối lượng mỗi chất trong hỗn hợp Xc/ tính khối lượng muối thu được sau phản ứng
Xem chi tiết
nH2 \(\approx\)0,2 (mol)
Mg + 2HCl \(\rightarrow\) MgCl2 + H2 (1)
0,2 <------------ 0,2 <----- 0,2 (mol)
MgO + 2HCl \(\rightarrow\) MgCl2 + H2O (2)
b) %mMg = \(\frac{0,2.24}{8,8}\) . 100% =54,55%
%mMgO = 45,45%
c) mMgO = 8,8 - 0,2 . 24 = 4(g)
=> nMgO=0,1 (mol)
Theo pt(2) nMgCl2 = nMg = 0,1 (mol)
=> \(\Sigma n_{MgCl_2}\) = 0,2 + 0,1 = 0,3 (mol)
mmuối = 0,3 . 95 = 28,5 (g)
Đúng 0
Bình luận (0)
Cho 12 gam hỗn hợp X gồm Fe và FeO tác dụng vừa đủ với dung dịch HCl. Sau phản ứng thu được 3,36 lít khí H2 (đktc).
a. Viết các phương trình phản ứng xảy ra.
b. Tính khối lượng của mỗi chất trong hỗn hợp X và thể tích dung dịch HCl 2M đã dùng.
c. Cho lượng hỗn hợp X nói trên vào dung dịch CuSO4 dư thì sau phản ứng thu được bao nhiêu gam chất rắn.
a)
$Fe + 2HCl \to FeCl_2 + H_2$
$FeO + 2HCl \to FeCl_2 + H_2O$
b)
Theo PTHH : $n_{Fe} = n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)$
$m_{Fe} = 0,15.56 = 8,4(gam)$
$m_{FeO} = 12 - 8,4 = 3,6(gam)$
$n_{FeO} =0,05(mol)$
Theo PTHH : $n_{HCl} = 2n_{Fe} + 2n_{FeO} = 0,4(mol)$
$V_{dd\ HCl} = \dfrac{0,4}{2} = 0,2(lít)$
c) $Fe + CuSO_4 \to FeSO_4 + Cu$
$n_{Cu} = n_{Fe} = 0,15(mol) \Rightarrow m_{chất\ rắn} = m_{FeO} + m_{Cu}$
$= 3,6 + 0,15.64 = 13,2(gam)$
Đúng 0
Bình luận (0)
Hòa tan 9,2g hỗn hợp gồm Mg và MgO vào dung dịch HCl vừa đủ. Sau phản ứng thu được 1,12 lít khí ở đktc
a, Viết các phương trình hóa học xảy ra
b, Tính khối lượng mỗi chất có trong hỗn hợp ban đầu
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
\(n_{Mg}=n_{H_2}=\dfrac{1.12}{22.4}=0.05\left(mol\right)\)
\(m_{Mg}=0.05\cdot24=1.2g\)
\(m_{MgO}=9.2-1.2=8\left(g\right)\)
Đúng 2
Bình luận (0)
a)
$Mg + 2HCl \to MgCl_2 + H_2$
$MgO + 2HCl \to MgCl_2 + H_2O$
b)
Theo PTHH :
$n_{Mg} = n_{H_2} = \dfrac{1,12}{22,4} = 0,05(mol)$
$m_{Mg} = 0,05.24 = 1,2(gam)$
$m_{MgO} = 9,2 - 1,2 = 8(gam)$
Đúng 1
Bình luận (0)
Câu 5: Cho 8,4 gam hỗn hợp X gồm Mg và MgO phản ứng vừa đủ với m gam dung dịch HCl 3,65 %, sau phản ứng thu được dung dịch Y và 2,24 lít khí H2 (ở đktc). a.Viết PTPƯ xảy ra và tính phần trăm khối lượng mỗi chất trong hỗn hợp đầu. b. Tính m và nồng độ phần trăm các chất trong dung dịch Y.
Câu 5 :
\(n_{H2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
a) Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,1 0,2 0,1 0,1
\(MgO+2HCl\rightarrow MgCl_2+H_2O|\)
1 2 1 1
0,15 0,3 0,15
a) \(n_{Mg}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(m_{Mg}=0,1.24=2,4\left(g\right)\)
\(m_{MgO}=8,4-2,4=6\left(g\right)\)
0/0Mg = \(\dfrac{2,4.100}{8,4}=28,57\)0/0
0/0MgO = \(\dfrac{6.100}{8,4}=71,43\)0/0
b) Có : \(m_{MgO}=6\left(g\right)\)
\(n_{MgO}=\dfrac{6}{40}=0,15\left(mol\right)\)
\(n_{HCl\left(tổng\right)}=0,2+0,3=0,5\left(mol\right)\)
\(m_{HCl}=0,5.36,5=18,25\left(g\right)\)
\(m_{ddHCl}=\dfrac{18,25.100}{3,65}=500\left(g\right)\)
\(n_{MgCl2\left(tổng\right)}=0,1+0,15=0,25\left(mol\right)\)
⇒ \(m_{MgCl2}=0,15.95=14,25\left(g\right)\)
\(m_{ddspu}=8,4+500-\left(0,1.2\right)=508,2\left(g\right)\)
\(C_{MgCl2}=\dfrac{14,25.100}{508,2}=2,8\)0/0
Chúc bạn học tốt
Đúng 1
Bình luận (1)
1) Cho 4,4 gam hỗn hợp gồm Mg và MgO tác dụng với dung dịch HCl (dư) thu được 2,24 lít khí (đktc).
1. Viết các phương trình phản ứng xảy ra.
2. Tính khối lượng của mỗi chất trong hỗn hợp.
3. Phải dùng bao nhiêu ml dung dịch HCl 2M đủ để hoà tan 4,4 gam hỗn hợp
1)
$MgO + 2HCl to MgCl_2 + H_2O$
$Mg + 2HCl \to MgCl_2 + H_2$
2)
$n_{Mg} = n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol)$
$m_{Mg} = 0,1.24 = 2,4(gam)$
$m_{MgO} = 4,4 - 2,4 = 2(gam)$
3)
$n_{HCl} = 2n_{Mg} + 2n_{MgO} = 0,1.2 + \dfrac{2}{40}.2 = 0,3(mol)$
$V_{dd\ HCl} = \dfrac{0,3}{2} = 0,15(lít) = 150(ml)$
Đúng 2
Bình luận (0)
Cho 4,4 gam hỗn hợp X gồm Mg và MgO tác dụng với dung dịch HCl 3,65% (dư 20% so với lượng phản ứng) thu được dung dịch Y và 2,24 lít khí H2 (đktc). (a) Viết PTHH xảy ra và tính phần trăm khối lượng mỗi chất trong hỗn hợp X. (b) Tính nồng độ phần trăm các chất có trong dung dịch Y.
Bài tập 3: Hoà tan 9,2 gam hỗn hợp gồm Mg, MgO cần vừa đủ dung dịch HCl . Sau phản ứng thu được 1,12 lít khí (đktc). - Tính % khối lượng mỗi chất trong hỗn hợp ban đầu? Theo các bước sau: + Viết các PTHH xảy ra. + Tính của khí thu được (H2). +Dựa vào PTHH tính => =>%MgO.
Ta có: \(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
PTHH:
Mg + 2HCl ---> MgCl2 + H2 (1)
MgO + 2HCl ---> MgCl2 + H2O (2)
Theo PT(1): \(n_{Mg}=n_{H_2}=0,05\left(mol\right)\)
=> \(m_{Mg}=0,05.24=1,2\left(g\right)\)
=> \(\%_{m_{Mg}}=\dfrac{1,2}{9,2}.100\%=13,04\%\)
\(\%_{m_{MgO}}=100\%-13,04\%=86,96\%\)
Đúng 1
Bình luận (0)