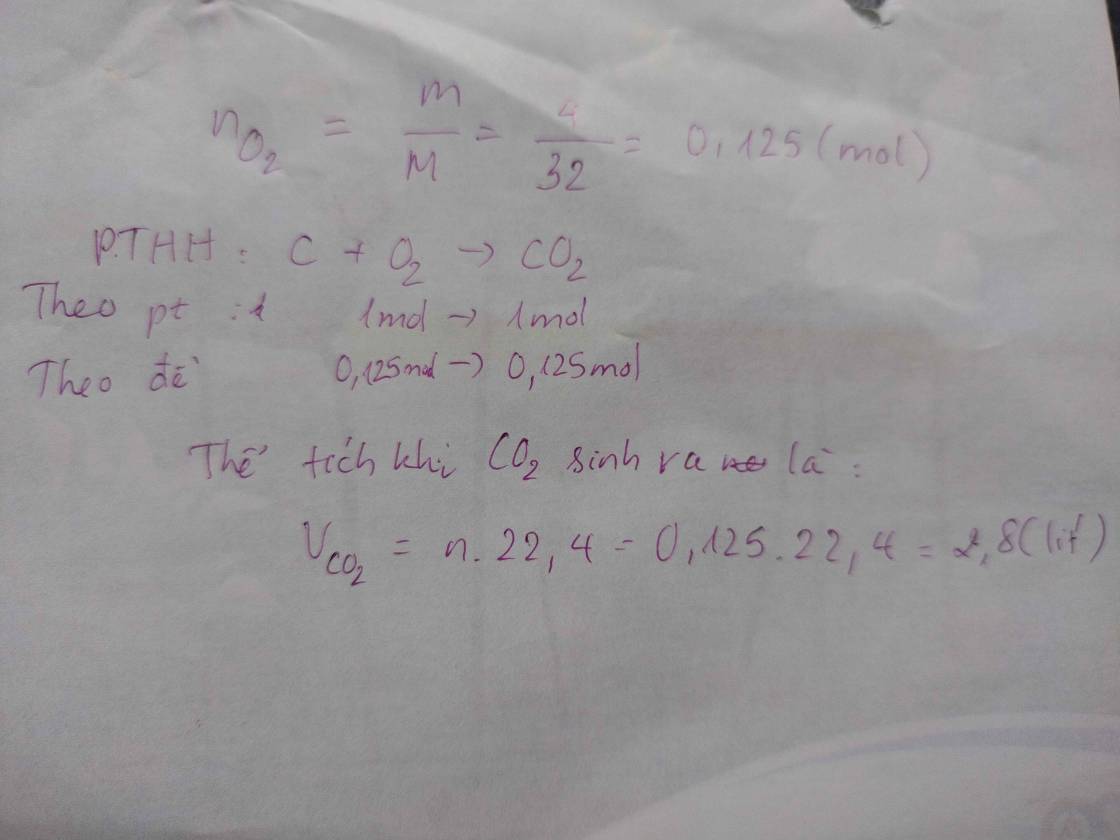Sulfur cháy trong oxygen sinh ra khí sulfur dioxide SO2. Hãy tính thể tích khí sinh ra (đkc), nếu có 4 gam khí O2 tham gia

Những câu hỏi liên quan
Carbon cháy trong khí oxygen hoặc trong không khí sinh ra khí carbon dioxxide: C + O2 → CO2 Hãy tìm thể tích khí carbon dioxide (đktc) sinh ra nếu có 4 gam khí oxi tham gia phản ứng
Xin mn giúp ạ.Thanks
Đốt cháy 3,2 gam sulfur trong bình đựng khí oxygen ( O2 )thì thấy sulfur cháy có ngọn lửa màu xanh thu được 6,4 gam sulfur dioxide SO2.
a) Hãy cho biết dấu hiệu nhận biết có phản ứng hóa học xảy ra.
b) Tính khối lượng khí oxygen phản ứng.
c) Khí oxygengen nặng hay nhẹ hơn không khí bằng bao nhiêu lần ?
a) Có chất mới sinh ra
b) Theo ĐLBTKL: mS + mO2 = mSO2
=> mO2 = 6,4 - 3,2 = 3,2 (g)
c) Xét \(d_{O_2/kk}=\dfrac{32}{29}=1,1\)
=> Khí O2 nặng hơn không khí 1,1 lần
Đúng 0
Bình luận (0)
Lưu huỳnh cháy trong oxi hoặc trong không khí sinh ra lưu huỳnh đioxit SO2. Hãy tính thể tích (đktc) sinh ra, nếu có 4 gam khí O2 tham gia phản ứng
\(n_{O_2}=\dfrac{4}{32}=0,125\left(mol\right)\\ S+O_2\rightarrow\left(t^o\right)SO_2\\ n_{SO_2}=n_{O_2}=0,125\left(mol\right)\\ \Rightarrow V_{SO_2\left(đktc\right)}=0,125.22,4=2,8\left(l\right)\)
Đúng 3
Bình luận (0)
\(n_{O_2}=\dfrac{4}{32}=0,125\left(mol\right)\)
PTHH : S + O2 -to> SO2
0,125 0,125 0,125
\(V_{SO_2}=0,125.22,4=2,8\left(l\right)\)
Đúng 2
Bình luận (0)
\(n_{O_2}=\dfrac{4}{32}=0,125\left(mol\right)\)
PTHH : S + O2 -to-> SO2
0,125 0,125 0,125
\(V_{O_2}=0,125.22,4=2,8\left(l\right)\)
Đúng 0
Bình luận (1)
9) Sulfur (S) cháy theo sơ đồ phản ứng sau: S + O2
t
o
→ SO2
Đốt cháy 48 (g) S trong khí Oxygen thì thu được 96(g) khí Sulfur dioxide (SO2).
Tính khối lượng Oxygen đã tham gia phản ứng:
A.40(g)
B.44(g)
C.48(g)
D.52(g)
Bảo toàn KL: \(m_S+m_{O_2}=m_{SO_2}\)
\(\Rightarrow m_{O_2}=96-48=48\left(g\right)\\ \Rightarrow C\)
Đúng 3
Bình luận (0)
Đáp án là C: 48g đấy bạn
Áp dụng định luật bảo toàn khối lượng :
mS+mO2=mSO2
⇒mO2=96−48=48(g).
chúc bạn học tốt !
Đúng 0
Bình luận (0)
Lưu huỳnh cháy trong oxi hoặc trong không khí sinh ra lưu huỳnh đioxit SO2. Hãy tính thể tích (đktc) sinh ra, nếu có 4 gam khí O2
tham gia phản ứng
Bước 1: Viết phương trình hóa học
Bước 2: Tìm số mol khí
Bước 3: thông qua phương trình hóa học, tìm số mol chất cần tính
Bước 4: Tìm thể tích khí
b1:
PTHH: \(S+O_2\Rightarrow SO_2\)
b2:
nSO2=\(\dfrac{m}{M}=\dfrac{4}{64}=0,0625mol\)
b4:
VSO2=22,4.n=22,4.0,0625=1,4 (lít)
Đúng 1
Bình luận (0)
4. Carbon cháy trong khí oxygen hoặc trong không khí sinh ra khí carbon dioxxide: C + O2 → CO2 Hãy tính thể tích khí oxygen O2 (đktc) cần dùng để đốt cháy hoàn toàn 24 gam carbon C
Đốt cháy S trong bình chứa khí O2 sau phản ứng người ta thu được 4,958 lít khí SO2 biết các khí ở đkc a) Khối lượng S đã tham gia phản ứng là bao nhiêu gam? b) thể tích khí oxygen (O2) ở đkc
\(S+O_2\underrightarrow{t^o}SO_2\)
\(1:1:1:1\)
\(0,2:0,2:0,2:0,2\left(mol\right)\)
\(n_{SO_2}=\dfrac{V}{24,79}=\dfrac{4,958}{24,79}=0,2\left(mol\right)\)
\(a,m_S=n.M=0,2.32=6,4\left(g\right)\)
\(b,V_{O_2}=n.24,79=0,2.24,79=4,958\left(l\right)\)
Đúng 3
Bình luận (0)
làm lại ko để ý có điều kiện=))))
\(n_{SO_2\left(dkc\right)}=\dfrac{V}{24,79}=\dfrac{4,958}{24,79}=0,2\left(mol\right)\)
\(PTHH:S+O_2-^{t^o}>SO_2\)
tỉ lệ 1 : 1 : 1
n(mol) 0,2<--0,2<---0,2
\(m_S=n\cdot M=0,2\cdot32=6,4\left(g\right)\\ V_{O_2\left(dkc\right)}=n\cdot24,79=0,2\cdot24,79=4,958\left(l\right)\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 6,4g Sulfur trong không khí thu được 12,8g khí Sulfur dioxide
a) Viết phương trình hóa học phản ứng xảy ra
b) Cho biết tỉ lệ số nguyên tử , phân tử giữa các chất trong phản ứng
c) Áp dụng DLBTKL , hãy tính khối lượng khí Oxygen đã phản ứng
\(a.S+O_2\xrightarrow[]{t^0}SO_2 \)
b. Tỉ lệ 1 : 1 : 1
\(c:BTKL:m_S+m_{O_2}=m_{SO_2}\\ \Rightarrow m_{O_2}=m_{SO_2}-m_S\\ =12,8-6,4\\ =6,4g\)
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 1 lượng sulfur trong khí oxygen thu được 6,4 gam sulfur dioxide.
a. Lập PTHH.
b. Tính khối lượng của sulfur và thể tích khí oxygen cần cho phản ứng.
S=32, O=16
a) \(n_{SO_2}=\dfrac{6,4}{64}=0,1\left(mol\right)\)
PTHH : S + O2 - to---> SO2
0,1 0,1 0,1 ( mol )
b) \(m_S=0,1.32=3,2\left(g\right)\)
\(V_{O_2}=0,1.22,4=2,24\left(l\right)\)
Đúng 2
Bình luận (1)