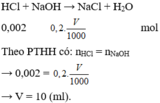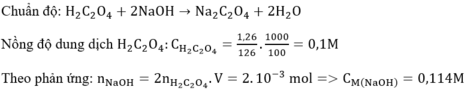Trung hòa hoàn toàn 400ml dung dịch axit axetic bằng 400 ml dung dịch NaOH. Tính nồng độ mol/l dung dịch NaOH cần dùng.

Những câu hỏi liên quan
Để trung hòa 480 gam dung dịch axit axetic cần dùng 200 ml dung dịch NaOH 2M . Tính nồng độ % của axit axetic trong dung dịch ban đầu.
nNaOH = 0,2.2 = 0,4 (mol)
PTHH: NaOH + CH3COOH --> CH3COONa + H2O
0,4------>0,4
=> \(C\%_{ddCH_3COOH}=\dfrac{0,4.60}{480}.100\%=5\%\)
Đúng 2
Bình luận (0)
Cho 500ml dung dịch axit axetic tác dụng hoàn toàn với Mg, thu được 14,2g muối (CH3COO)2Mg
a/ Tính nồng độ mol của dung dịch axit
b/ Tính thể tích khí hidro sinh ra ở đktc
c/ Tính thể tích dung dịch NaOH 0,5M cần dùng để trung hòa 500ml dung dịch axit trên
đổi 500ml = 0,5l
n(CH\(_3\)COOH)\(_2\)Mg= \(\dfrac{14,2}{142}\)= 0,1mol
2CH3COOH + Mg \(\rightarrow\) (CH3COO)2Mg + H2
0,2mol 0,1mol 0,1mol
a/ CCH3COOH= \(\dfrac{0,2}{0,5}\)=0,4M
b/ VH\(_2\) 0,1 . 22,4 = 2,24l
c/ nCH\(_3\)COOH= 0,2mol
CH3COOH + NaOH \(\rightarrow\) CH3COONa + H2
0,2mol 0,2mol
V\(_{dd_{NaOH}}\)= \(\dfrac{0,2}{0,5}\)= 0,4l
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn một lượng Zn bằng 400 ml dung dịch axit axetic vừa đủ, thấy thoát ra 4.48lit khí ( ở đktc). a/ Viết PTHH của phản ứng xảy ra. b/ Tính nồng độ mol của dung dịch axit đã dùng c/ Nếu cho một lượng axit như trên tác dụng với 400ml dung dịch KOH Tính nồng độ mol/l của dung dịch muối tạo thành sau phản ứng ?
\(a,Zn+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Zn+H_2\\ n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ b,n_{CH_3COOH}=2.0,2=0,4\left(mol\right)\\ C_{MddCH_3COOH}=\dfrac{0,4}{0,4}=1\left(M\right)\\ c,CH_3COOH+KOH\rightarrow CH_3COOK+H_2O\\ n_{CH_3COOK}=n_{CH_3COOH}=0,4\left(mol\right)\\ V_{ddCH_3COOK}=400+400=800\left(ml\right)=0,8\left(l\right)\\ C_{MddCH_3COOK}=\dfrac{0,4}{0,8}=0,5\left(M\right)\)
Đúng 3
Bình luận (0)
\(Zn+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Zn+H_2\uparrow\)
0,4 0,2
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(b,C_{M_{CH_3COOH}}=\dfrac{0,4}{0,4}=1M\)
\(c,CH_3COOH+KOH\rightarrow CH_3COOK+H_2O\)
0,4 0,4 0,4
\(C_{M_{CH_3COOK}}=\dfrac{0,4}{0,4}=1M\)
Đúng 0
Bình luận (0)
Cho 40ml dung dịch axit axetic tác dụng hết với bột magie thu được 1,42g muối.
a) Tính nồng độ mol cảu dung dịch axetic đã dùng.
b) Tính thể tích khí bay ra (đktc).
c) Để trung hòa hết lượng dung dịch axit trên cần phải dùng bao nhiêu ml dung dịch NaOH 0,75M.
"Câu cuối r "
2CH3COOH+Mg->(CH3COO)2Mg+H2
0,02---------------0,01-------0,01----------0,01
n muối=0,01mol
=>CM=\(\dfrac{0,02}{0,04}=0,5M\)
=>VH2=0,01.22,4=0,224l
CH3COOH+NaOH->CH3COONa+H2O
0,02--------------0,02
=>VNaOH=\(\dfrac{0,02}{0,75}=0,03l\)
Đúng 2
Bình luận (3)
a) \(n_{\left(CH_3COO\right)_2Mg}=\dfrac{1,42}{142}=0,01\left(mol\right)\)
PTHH: Mg + 2CH3COOH --> (CH3COO)2Mg + H2
0,01<-------0,02<------------0,01------->0,01
=> \(C_{M\left(dd.CH_3COOH\right)}=\dfrac{0,02}{0,04}=0,5M\)
b) VH2 = 0,01.22,4 = 0,224 (l)
c)
PTHH: NaOH + CH3COOH --> CH3COONa + H2O
0,02<------0,02
=> \(V_{dd.NaOH}=\dfrac{0,02}{0,75}=\dfrac{2}{75}\left(l\right)=\dfrac{80}{3}\left(ml\right)\)
Đúng 1
Bình luận (2)
\(a.2CH_3COOH+Mg\rightarrow\left(CH_3COO\right)_2Mg+H_2\\ n_{\left(CH_3COO\right)_2Mg}=0,01\left(mol\right)\\ n_{CH_3COOH}=2n_{\left(CH_3COO\right)_2Mg}=0,02\left(mol\right)\\ \Rightarrow CM_{CH_3COOH}=\dfrac{0,02}{0,04}=0,5M\\ b.n_{H_2}=n_{\left(CH_3COO\right)_2Mg}=0,01\left(mol\right)\\ \Rightarrow V_{H_2}=0,01.22,4=0,224\left(l\right)\\ c.CH_3COOH+NaOH\rightarrow CH_3COONa+H_2O\\ n_{CH_3COOH}=n_{NaOH}=0,02\left(mol\right)\\ \Rightarrow V_{NaOH}=\dfrac{0,02}{0,75}=0,02667\left(l\right)=26,67ml\)
Đúng 2
Bình luận (1)
a: hòa tan hoàn toàn 0,3 mol NaOH vào nước thu được 0,5 lít dung dịch NaOH. tính nồng độ mol của dung dịch?
b: hòa tan hoàn tàn 24 gam NaOH vào nước thu được 400ml dung dịch NaOH. tính nồng độ mol của dung dịch?
\(a,C_{M\left(NaOH\right)}=\dfrac{0,3}{0,5}=0,6M\\ b,n_{NaOH}=\dfrac{24}{40}=0,6\left(mol\right)\\ C_{M\left(NaOH\right)}=\dfrac{0,6}{0,4}=1,5M\)
Đúng 1
Bình luận (0)
Để trung hòa hoàn toàn 20 ml dung dịch HCl 0,1M cần V ml dung dịch NaOH nồng độ 0,2 mol/l. Giá trị của V là
A. 40
B. 20
C. 10
D. 30
Trung hòa 400ml dung dịch H2SO4 1M bằng dung dịch NaOH 0,5M.
a/ Viết phương trình phản ứng hóa học xảy ra?
b/ Tính thể tích dung dịch NaOH 0,5M đã dùng?
c/Tính nồng độ mol/l dung dịch thu được phản ứng sau?
\(n_{H_2SO_4}=0,4\cdot1=0,4mol\)
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+H_2O\)
0,8 0,4
\(V_{NaOH}=\dfrac{0,8}{0,5}=1,6l\)
Đúng 2
Bình luận (1)
\(n_{H_2SO_4}=0.4\cdot1=0.4\left(mol\right)\)
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
\(0.8.............0.4..............0.4\)
\(V_{dd_{NaOH}}=\dfrac{0.8}{0.5}=1.6\left(l\right)\)
\(V_{dd}=0.4+1.6=2\left(l\right)\)
\(C_{M_{Na_2SO_4}}=\dfrac{0.4}{2}=0.2\left(M\right)\)
Đúng 1
Bình luận (0)
Để trung hòa 10 ml dung dịch hỗn hợp axit gồm HCl và
H
2
S
O
4
cần dùng 40ml dung dịch NaOH 0,5M. Mặt khác lấy 100 ml dung dịch hỗn hợp axit trên đem trung hòa bằng một lượng NaOH vừa đủ rồi cô cạn thì thu được 13,2 gam muối khan. Nồng độ mol của mỗi axit trong dung dịch ban đầu lần lượt là A. 0,8M và 0,6M B. 1M và 0,5M C. 0,6M và 0,7M D. 0,2M và 0,9M
Đọc tiếp
Để trung hòa 10 ml dung dịch hỗn hợp axit gồm HCl và H 2 S O 4 cần dùng 40ml dung dịch NaOH 0,5M. Mặt khác lấy 100 ml dung dịch hỗn hợp axit trên đem trung hòa bằng một lượng NaOH vừa đủ rồi cô cạn thì thu được 13,2 gam muối khan. Nồng độ mol của mỗi axit trong dung dịch ban đầu lần lượt là
A. 0,8M và 0,6M
B. 1M và 0,5M
C. 0,6M và 0,7M
D. 0,2M và 0,9M
Chọn A
Gọi nồng độ mol ban đầu của HCl và H 2 S O 4 lần lượt là x và y (M)


Đúng 0
Bình luận (0)
Để xác định nồng đội dung dịch NaOH người ta tiến hành như sau: cân 1,26 gam axit oxalic ngậm nước (H2C2O4.2H2O) hòa tan hoàn toàn vào nước, định mức thành 100 ml. lấy 10 ml dung dịch này thêm vào đó vài giọt phenolphthalein, đem chuẩn độ bằng dung dịch NaOH đến xuất hiện màu hồng (ở pH 9) thì hết 17,5 ml dung dịch NaOH. Tính nồng độ dung dịch NaOH đã dùng. A. 0,114M B. 0,26M C. 0,124M D. 0,16M
Đọc tiếp
Để xác định nồng đội dung dịch NaOH người ta tiến hành như sau: cân 1,26 gam axit oxalic ngậm nước (H2C2O4.2H2O) hòa tan hoàn toàn vào nước, định mức thành 100 ml. lấy 10 ml dung dịch này thêm vào đó vài giọt phenolphthalein, đem chuẩn độ bằng dung dịch NaOH đến xuất hiện màu hồng (ở pH = 9) thì hết 17,5 ml dung dịch NaOH. Tính nồng độ dung dịch NaOH đã dùng.
A. 0,114M
B. 0,26M
C. 0,124M
D. 0,16M