tính khối lượng nước bay hơi khi làm bay hơi 500g dung dịch NaOH 3% để thu được dung dịch NaOH 10%. MÌnh cảm ơn trước nha!!

Những câu hỏi liên quan
Có 200g dung dịch NaOH 5% (dung dịch A). Làm bay hơi nước dung dịch A, người ta cũng thu được dung dịch NaOH 8%. Tính khối lượng nước đã bay hơi.
Gọi x(g) là khối lượng của nước bay hơi khỏi dung dịch để có dung dịch NaOH 8%.
Ta có công thức:
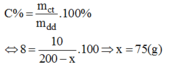
Vậy cho 75g nước bay hơi ra khỏi 200g dung dịch NaOH ban đầu, ta có: 200 – 75 = 125(g) dung dịch NaOH 8%.
Đúng 0
Bình luận (0)
bài 1 : Làm bay hơi 500g dung dịch NAOH 3% người ta thu được dung dịch NAOH 10% . Tính khối lượng nước thoát ra?
bài 2 : Cần thêm bao nhiêu gam SO3 vào dung dịch H2SO4 10% để được 100g dung dịch H2SO4 20% ?
giúp mk vs ... thanks mn trước nha
Bài 1 :
Ta có :
Khối lượng nước có trong dung dịch NaOH 3% là :
mH2O = mdm = mdd- mct = 500 - \(\dfrac{500.3\%}{100}=485\left(g\right)\)
Gọi x là số gam nước thoát ra :
ta có : \(\dfrac{10}{485-x}=\dfrac{10}{100}\)
<=> \(\dfrac{10}{485-x}=0,1\)
<=> 10 = 0,1(485- x)
<=> 0,1x = 38,5
=> x = 385 (g)
Vậy...
Đúng 0
Bình luận (0)
Chữa bài 2
Số gam SO3 cần cho vào là x (gam); số gam dung dịch H2SO4 10% ban đầu là y (gam). Suy ra \(x+y=100\left(1\right)\)
SO3 + H2O \(\rightarrow\) H2SO4
\(\dfrac{x}{80}\)...................... \(\dfrac{x}{80}\)
Sau khi thêm SO3 vào dung dịch H2SO4 10% thì thu được 100gam dd H2SO4 20%.
\(\Rightarrow\dfrac{\dfrac{x}{80}.98+10\%.y}{100}=20\%\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x\approx8,88gam\\y\approx91,11gam\end{matrix}\right.\)
Đúng 0
Bình luận (2)
Gọi số mol của SO3 cần thêm là x mol => mSO3 cần thêm = 80x (g)
Ta có PTHH :
SO3 + H2O \(\rightarrow\) H2SO4.
x(mol)..............x(mol)
số gam H2SO4 có thêm là mH2SO4 = 98x
Khối lượng chất tan có trong dung dịch ban đầu là :
mH2SO4 = 10g
=> khối lượng chất tan sau p/ư là
mH2SO4=98x+10g
Theo ĐLBTKL thì m ddH2SO4 sau pứ là 80x + 100
DD sau pứ có nồng độ 20%
=>\(\dfrac{98x+10}{80x+10}.100\%=20\%\)
giả ra ta đc x \(\approx\) 0,122 mol
=>\(mSO3_{\left(c\text{ần}-th\text{ê}m\right)}=0,122.80=9,76\left(g\right)\)
Vậy....
Đúng 0
Bình luận (3)
Có 200g dung dịch NaOH 5% (dung dịch A) 1)cần hòa tan bao nhiêu g NaOH vào dung dich A để được dung dịnh NaOH 8% 2)Làm bay hơi nước dung dịch A,người ta thu được dung dịch NaOH 8% .tính khối lượng...
Đọc tiếp
Có 200g dung dịch NaOH 5% (dung dịch A) 1)cần hòa tan bao nhiêu g NaOH vào dung dich A để được dung dịnh NaOH 8% 2)Làm bay hơi nước dung dịch A,người ta thu được dung dịch NaOH 8% .tính khối lượng nước bay hơi 3) cần trộn thêm vào dung dịch A bao nhiêu gam dung dịch NaOH 10% để được dung dịch NaOH 8%
a/ Gọi khối lượng NaOH cần thêm vào là a.
Khối lượng NaOH có trong dung dịch NaOH 5% là:
\(200.5\%=10\left(g\right)\)
Khối lượng NaOH sau khi thêm là:
\(m_{NaOH}=a+10\left(g\right)\)
\(\Rightarrow\dfrac{10+a}{200+a}=0,08\)
\(\Leftrightarrow a\approx6,522\left(g\right)\)
b/ Gọi khối lượng nước cần làm bay hơi là x. Ta có
\(\dfrac{10}{200-x}=0,08\)
\(\Rightarrow x=75\left(g\right)\)
c/ Gọi khối lượng dung dịch NaOH cần thêm vào là y.
\(\Rightarrow m_{NaOH\left(t\right)}=0,1y\left(g\right)\)
\(\Rightarrow m_{NaOH}=10+0,1y\left(g\right)\)
\(\Rightarrow\dfrac{10+0,1y}{200+y}=0,08\)
\(\Rightarrow y=300\left(g\right)\)
Đúng 0
Bình luận (0)
Câu 14: Có 100g dung dịch NaOH 5% (dung dịch A). a) Làm bay hơi nước dung dịch A, người ta cũng thu được dung dịch NaOH 8%. Tính khối lượng nước đã bay hơi. b) Cần hòa tan bao nhiêu gam NaOH vào dung dịch A để có dung dịch A để có dung dịch NaOH 8%?
a. \(n_{NaOH\left(5\%\right)}=\frac{100.5}{100.40}=0,125mol\)
\(m_{ddNaOH\left(8\%\right)}=\frac{0,125.100.40}{8}=62,5g\)
\(m_{H_2O}\) bay hơi \(=100-62,5=37,5g\)
b. \(m_{NaOH\left(A\right)}=40.0,125=5g\)
\(m_{NaOH\left(8\%\right)}=\frac{100.8}{100}=8g\)
\(m_{NaOH}\) thêm vào \(=8-5=3g\)
Có 250 g dung dịch NaOH 6% ( dung dịch A)
a, Cần hoà tan bao nhiêu gam NaOH vào dung dịch A để có dung dịch NaOH 8%
b, Làm bay hơi nước dung dịch A , người ta cũng thu được dung dịch NaOH 8% . Tính khối lượng nước bay hơi
có 250 gam dung dịch NaOH 6% (dung dịch A)
a) cần phải trộn thêm vào dung dịch A bao nhiêu gam dung dịch NaOH 10% để được dung dịch NaOH 8%?
b) cần hòa tan bao nhiêu gam NaOH vào dung dịch A để có dung dịch NaOH 8%?
c) làm bay hơi nước dung dịch A, người ta cũng thu được dung dịch NaOH 8%. Tính khối lượng nước bay hơi?
giúp em với ạ, e đg cần kq gấp ! T^T
Áp dụng phương pháp đường chéo ta có
250g dd A ,C%=6%------------8%-----------10-8
Xg dd NaOh , C% =10%-------8%-----------8-6
=> \(\dfrac{250}{X}\)= 1
=> X = 250 (g)
b) mA=\(\dfrac{250.6}{100}\)=15(g)
Gọi a là số gam NaOH thêm vào
Ta có :
C%=\(\dfrac{\left(15+a\right).100\%}{250+a}\)= 8%
=> 1500 + 100a = 2000 + 8a
=> 92a = 500
=> a=\(\dfrac{500}{92}\)= 5,4(g)
c) Gọi b là khối lượng nước bay hơi
Ta có :
C% =\(\dfrac{15.100\%}{250-b}\)= 8%
=> 1500 =2000 - 8b
=> 8b = 500
=> b = \(\dfrac{500}{8}\)= 62,5(g)
250g dd A ,C%=6%------------8%-----------10-8
Xg dd NaOh , C% =10%-------8%-----------8-6
=> \(\dfrac{250}{X}\)= 1
=> X = 250 (g)
b) mA=\(\dfrac{250.6}{100}\)=15(g)
Gọi a là số gam NaOH thêm vào
Ta có :
C%=\(\dfrac{\left(15+a\right).100\%}{250+a}\)= 8%
=> 1500 + 100a = 2000 + 8a
=> 92a = 500
=> a=\(\dfrac{500}{92}\)= 5,4(g)
c) Gọi b là khối lượng nước bay hơi
Ta có :
C% =\(\dfrac{15.100\%}{250-b}\)= 8%
=> 1500 =2000 - 8b
=> 8b = 500
=> b = \(\dfrac{500}{8}\)= 62,5(g)
Đúng 0
Bình luận (0)
theo giả thiết, mNaOH = 250 0,06 = 15 (g)
a)
gọi khối lượng NaOH thêm vào là a (g) => khối lượng dung dịch NaOH 10% là 10a (g)
để được dung dịch như đề bài thì: \(\dfrac{15+a}{250+10a}=0,08\Rightarrow a=25\left(g\right)\)
Vậy cần trộn thêm 250 g dung dịch NaOH 10% để được dung dịch NaOH 8%
b)
gọi khối lượng NaOH thêm vào là a (g)
để được dung dịch như đề bài thì: \(\dfrac{15+a}{250}=0,08\Rightarrow a=5\left(g\right)\)
Vậy cần trộn thêm 5 g NaOH để được dung dịch NaOH 8%
c)
gọi khối lượng nước bay hơi là a (g)
để được dung dịch như đề bài thì: \(\dfrac{15}{250-a}=0,08\Rightarrow a=62,5\left(g\right)\)
Vậy cần làm bay hơi 62,5 g nước để được dung dịch NaOH 8%
Đúng 0
Bình luận (0)
Có 200g dung dịch NaOH 5% ( dung dịch A ).
a,cần phải trộn thêm vào dung dịch A bao nhiêu gam dung dịch NaOH 10% để thu được dung dịch có nồng độ 8%.
b, cần hoà tan bao nhiêu gam NaOH vào dung dịch A để có dung dịch 8%.
c, làm bay hơi nước từ dung dịch A người ta thu được dung dịch có nồng độ 8%. Tính khối lượng nước đã bay hơi.
Cho 22,9 gam hỗn hợp Na và Ba tác dụng với nước (dư), thu được dung dịch X và 1,8.1023 phân tử H2 và dung dịch A chứa NaOH, Ba(OH)2.
a/ Viết PTHH.
b/ Tính khối lượng nước đã phản ứng
c/ Cô cạn dung dịch A để nước bay hơi. Tính tổng khối lượng NaOH và Ba(OH)2 thu được.
d/ Tính khối lượng từng kim loại trong hỗn hợp.
Cho 11,6 gam hỗn hợp Na và K tác dụng với nước (dư), thu được 4,48 lít H2 (đktc) và dung dịch A chứa NaOH, KOH.
a/ Viết PTHH.
b/ Tính khối lượng nước đã phản ứng.
c/ Cô cạn dung dịch A để nước bay hơi. Tính tổng khối lượng NaOH và KOH thu được.
d/ Tính khối lượng từng kim loại trong hỗn hợp.
2Na+2H2O->2NaOH+H2
x-------------------x---------0,5x
2K+2H2O->2KOH+H2
y-----------------y-----------0,5y
nH2O=2n H2
=>mH2O=\(\dfrac{4,48}{22,4}2.18\)=7,2g
Ta có :\(\left\{{}\begin{matrix}23x+39y=11,6\\0,5x+0,5y=0,2\end{matrix}\right.\)
=>x=0,25 mol, y=0,15 mol
=>m bazo=0,25.40+0,15.56=18,4g
d) m Na=0,25.23=5,75g
=>m K=0,15.39=5,85g
Đúng 2
Bình luận (0)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
gọi nNa :a , nk :b (a,b>0)
=> 23a+39b=11,6(g)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
a \(\dfrac{1}{2}a\)
\(2K+2H_2O\rightarrow2KOH+H_2\)
b \(\dfrac{1}{2}b\)
=> \(\left\{{}\begin{matrix}23a+39b=11,6\\\dfrac{1}{2}a+\dfrac{1}{2}b=0,2\end{matrix}\right.\)
=> a= 0,25 , b = 0,15(mol)
theo pt nH2O = 0,4+0,4=0,8(mol)
=> mH2O = 0,8.18=14,4(g)
theo pthh : nKOH = 0,15 , nNaOH = 0,25
=> \(\left\{{}\begin{matrix}m_{KOH}=0,15.56=8,4\left(g\right)\\m_{NaOH}=0,25.40=10\left(g\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}m_K=0,15.39=5,85\left(g\right)\\m_{Na}=0,25.23=5,75\left(g\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)























