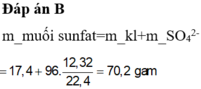Hỗn hợp X gồm có 3 kim loại Al, Mg, Cu. Lấy 6,7 g hhX tác dụng hết với dd H2SO4 đặc nóng dư thu được 4,48 lit SO2 ở đktc và dd A. Cô cạn dd A thu được m (g) muối khan . Giá trị của m là :

Những câu hỏi liên quan
Hỗn hợp X gồm có 3 oxit kim loại Al, Mg, Zn. Lấy 6,4 g hhX tác dụng vừa hết 200ml dung dịch H2SO4 19,6% ( d = 1,12 g/ml)dd A. Cô cạn dd A thu được m (g) muối khan . Giá trị của m là :
\(m_{ddH_2SO_4}=D\cdot V=1,12\cdot200=224g\)
\(\Rightarrow m_{H_2SO_4}=\dfrac{19,6\%\cdot224}{100\%}=4,3904g\)
\(\Rightarrow n_{H_2SO_4}=0,0448mol\Rightarrow n_{SO_4^{2-}}=n_{H_2SO_4}=0,0488mol\)
\(\Rightarrow m_{SO_4^{2-}}=0,0488\cdot96=4,3008g\)
\(m=m_{SO_4^{2-}}+m_{hhX}=4,3008+6,4=10,7008g\)
Đúng 2
Bình luận (0)
1) Cho 6g hỗn hợp gồm Cu và Fe tác dụng hoàn toàn với dung dịch H2SO4 đặc,nóng dư thu được 2,8 lít khí SO2 đktc. Khối lượng Cu và Fe trong hỗn hợp ban đầu lần lượt là bao nhiêu?
2) Cho 10g hỗn hợp Cu và CuO vào dung dịch H2SO4 đặc nóng thu được 2,24 lít SO2 sản phẩm khử duy nhất ở đktc. Tính % khối lượng của Cu trong hỗn hợp ban đầu
3) Hỗn hợp X gồm 3 kim loại Al, Mg,Fe. Lấy 6,7g hỗn hợp X tác dụng hết với dd H2SO4 thu được 5,6 lit H2 ở đktc và dd A. Cô cạn dd A thu được m(g) muối khan. Giá tr...
Đọc tiếp
1) Cho 6g hỗn hợp gồm Cu và Fe tác dụng hoàn toàn với dung dịch H2SO4 đặc,nóng dư thu được 2,8 lít khí SO2 đktc. Khối lượng Cu và Fe trong hỗn hợp ban đầu lần lượt là bao nhiêu?
2) Cho 10g hỗn hợp Cu và CuO vào dung dịch H2SO4 đặc nóng thu được 2,24 lít SO2 sản phẩm khử duy nhất ở đktc. Tính % khối lượng của Cu trong hỗn hợp ban đầu
3) Hỗn hợp X gồm 3 kim loại Al, Mg,Fe. Lấy 6,7g hỗn hợp X tác dụng hết với dd H2SO4 thu được 5,6 lit H2 ở đktc và dd A. Cô cạn dd A thu được m(g) muối khan. Giá trị m là
1>
n SO2=2,8/22,4=0,125(mol)
Cu +2H2SO4-->CuSO4 +2H2O+SO2
x------------------------------------x(mol)
2Fe +6H2SO4-->Fe2(SO4)3+3SO2+6H2O
y-----------------------------------1,5y(mol)
ta có hpt
64x+56y=6
x+3y=0,125
=>x=0,05,y=0,05
=m Cu=0,05.64=3,2(g)
m Fe =6-3,2=2,8(g)
2>
Cu +2H2SO4-->CUSO4+2H2O+SO2
n SO2=2,24/22,4=0,1mol)
n Cu=n SO2=0,1(mol)
%m Cu=0,1.64/10.100%=64%
%m CUO=100-64=36%
3>
nH2=nH2SO4=5,6\22,4=0,25mol
=> nSO4=nH2SO4=0,25mol
Coi A gồm kim loại và nhóm SO4
=> m=mX+mSO4=6,7+0,25.96=30,7g
Đúng 0
Bình luận (0)
Câu 10: Cho m(g) hh Na2CO3 và Na2SO4 tác dụng hết với dd H2SO4 2M dư thu được 2,24 lít hh khí (ở đktc) có tỷ khối so với H2 bằng 27. Giá trị của m làB. 11,6 gam A. 1,16 g C. 6,11g D. 61,1 gam.Câu 11: Hỗn hợp X gồm có 3 kim loại Al, Mg, Fe. Lấy 6,7 g hhX tác dụng hết với dd H2SO4 thu được 5,6 lít H2 đktc và dd A. Cô cạn dd A thu được m (g) muối khan . Giá trị của m là :C. 30,7g B. 7,2 gam A. 6,2g D. 31,7 gam.Câu 12 : Thêm 100ml dd H,SO, vào 200ml dd NaOH 0,1M ta thu được dd X . Cho X tác dụng vừ...
Đọc tiếp
Câu 10: Cho m(g) hh Na2CO3 và Na2SO4 tác dụng hết với dd H2SO4 2M dư thu được 2,24 lít hh khí (ở đktc) có tỷ khối so với H2 bằng 27. Giá trị của m là
B. 11,6 gam A. 1,16 g C. 6,11g D. 61,1 gam.
Câu 11: Hỗn hợp X gồm có 3 kim loại Al, Mg, Fe. Lấy 6,7 g hhX tác dụng hết với dd H2SO4 thu được 5,6 lít H2 đktc và dd A. Cô cạn dd A thu được m (g) muối khan . Giá trị của m là :
C. 30,7g B. 7,2 gam A. 6,2g D. 31,7 gam.
Câu 12 : Thêm 100ml dd H,SO, vào 200ml dd NaOH 0,1M ta thu được dd X . Cho X tác dụng vừa đủ với 0,25g BaCl2 . Nồng độ của dd H2SO4 ban đầu là.
A. 1,6M B. 0,8M C. 2,6M D. 1,8M
Hỗn hợp X gồm 3 kim loại Al, Mg, Fe. Cho 6,7 gam hỗn hợp X tác dụng hết với dung dịch H2SO4 loãng thu được 5,6 lít H2 (đktc) và dung dịch Y. Cô cạn dung dịch Y thu được m gam muối khan. Giá trị của m là A. 6,2. B. 7,2. C. 30,7. D. 31,7.
Đọc tiếp
Hỗn hợp X gồm 3 kim loại Al, Mg, Fe. Cho 6,7 gam hỗn hợp X tác dụng hết với dung dịch H2SO4 loãng thu được 5,6 lít H2 (đktc) và dung dịch Y. Cô cạn dung dịch Y thu được m gam muối khan. Giá trị của m là
A. 6,2.
B. 7,2.
C. 30,7.
D. 31,7.
Hỗn hợp X gồm các kim loại Mg, Al, Zn. Lấy m gam hỗn hợp X tác dụng hết với dung dịch HCl dư thu được 6,72 lít khí (đktc). Cũng lấy m gam X tác dụng hết với dung dịch
H
2
S
O
4
đặc, nóng, dư thu được V lít khí
S
O
2
(sản phẩm khử duy nhất, ở đktc) và (m+a) gam muối. Giá trị của V và a lần lượt là A. 3,36 và 28,8 B. 6,72 và 28,8 C. 6,72 và 57,6 D. 3,36 và...
Đọc tiếp
Hỗn hợp X gồm các kim loại Mg, Al, Zn. Lấy m gam hỗn hợp X tác dụng hết với dung dịch HCl dư thu được 6,72 lít khí (đktc). Cũng lấy m gam X tác dụng hết với dung dịch H 2 S O 4 đặc, nóng, dư thu được V lít khí S O 2 (sản phẩm khử duy nhất, ở đktc) và (m+a) gam muối. Giá trị của V và a lần lượt là
A. 3,36 và 28,8
B. 6,72 và 28,8
C. 6,72 và 57,6
D. 3,36 và 14,4
Hoà tan 23,7 hỗn hợp kim loại gồm Mg , Al , Ag bằng dd HCl (lấy dư) thu được dd X ; 14,56 lít khí H2 (đktc) và 10,8g chất rắn Y . Cô cạn dd X thu được m gam muối . Giá trị của m là
10,8 g chất rắn đó là Ag không tan trong dd HCl
=> mMg + mAl = 23,7 - 10,8 = 12,9 (g)
nH2 = 14,56/22,4 = 0,65 (mol)
PTHH:
Mg + 2HCl -> MgCl2 + H2
2Al + 6HCl -> 2AlCl3 + 3H2
Theo 2 PTHH trên: nHCl = 2nH2 = 2 . 0,65 = 1,3 (mol)
Áp dụng ĐLBTKL, ta có:
mAl + mMg + mHCl = m(muối) + mH2
=> m(muối) = 12,9 + 36,5 . 1,3 - 0,65 . 2 = 59,05 (g)
Đúng 1
Bình luận (1)
41. Hoà tan 24,8g hh X gồm Fe, Mg, Cu trong dd H2SO4 đặc, nóng dư thu được dd A. Cô cạn dd A thu được 132 g muối khan. Nếu cho 24,8 g X tác dụng với dd HCl dư thu được 11,2 lít khí (đkc).
a. Viết phương trình phản ứng b. Tính % khối lượng mỗi kim loại trong hh X.
Gọi x, y, z là số mol Fe, Mg, Cu
=> \(56x+24y+64z=24,8\) (1)
X+ H2SO4 đặc nóng
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2↑ + 6H2O
Mg + 2H2SO4→ MgSO4 + SO2↑ + 2H2O.
Cu + 2H2SO4→ CuSO4 + SO2↑ + 2H2O.
Các muối là \(Fe_2\left(SO_4\right)_3,MgSO_4,CuSO_4\)
=> \(n_{Fe_2\left(SO_4\right)_3}=\dfrac{n_{Fe}}{2}=\dfrac{x.}{2};n_{MgCl_2}=n_{Mg}=y;n_{CuCl_2}=n_{Cu}=z\)
=> \(\dfrac{400x}{2}+120y+160z=132\) (2)
X + HCl dư thu được khí là H2
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
=> x+y=0,5 (mol) (3)
Từ (1), (2), (3) => x, y ,z
Xem lại đề vì hệ vô nghiệm
Đúng 2
Bình luận (1)
Hoà tan hoàn toàn 17,4 gam hỗn hợp kim loại X gồm Mg, Al, Cu bằng dung dịch H2SO4 đặc nóng thu được dung dịch Y và thoát ra 12,32 lit khí SO2 (đktc), sản phẩm khử duy nhất. Cô cạn cẩn thận dung dịch Y thu được m gam muối sunfat khan. Gía trị của m là: A. 52,6 gam B. 70,2 gam C. 71,3 gam D. 67,4 gam
Đọc tiếp
Hoà tan hoàn toàn 17,4 gam hỗn hợp kim loại X gồm Mg, Al, Cu bằng dung dịch H2SO4 đặc nóng thu được dung dịch Y và thoát ra 12,32 lit khí SO2 (đktc), sản phẩm khử duy nhất. Cô cạn cẩn thận dung dịch Y thu được m gam muối sunfat khan. Gía trị của m là:
A. 52,6 gam
B. 70,2 gam
C. 71,3 gam
D. 67,4 gam
Hòa tan hết m gam hỗn hợp gồm Mg, Al, Al2O3 và MgO cần 800ml dd hỗn hợp gồm HCl 0,5M và H2SO4 0,75M. Sau phản ứng thu được dd X và 4,48l khí H2 (đktc) . Cô cạn dd thu được X thu được 88,7 g muối khan. Tính m.
$n_{HCl} = 0,8.0,5 = 0,4(mol) ; n_{H_2SO_4} = 0,6(mol) ;n_{H_2} = 0,2(mol)$
$n_{H(trong\ axit)} = 0,4 + 0,6.2 = 1,6(mol)$
Bảo toàn H : $n_{H_2O} = \dfrac{n_{H(trong\ axit)} - 2n_{H_2} }{2} = 0,6(mol)$
Bảo toàn khối lượng :
$m = 88,7 + 0,6.18 + 0,2.2 - 0,4.36,5 - 0,6.98 = 26,5(gam)$
Đúng 2
Bình luận (0)