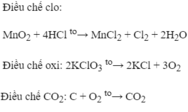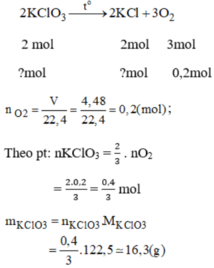viết phương trình hóa học điều chế khí oxi từ kali cloric và thuốc tím

Những câu hỏi liên quan
Hãy viết phương trình bằng chữ biểu diễn hiện tượng được mô tả sau đâyĐể điều chế oxi người ta tiến hành nung thuốc tím ( kali pemanganat
K
M
n
O
4
), thu được kali manganat
K
2
M
n
O
4
; mangan ddioxxit
(
M
n
O
2
)
và khí oxi.
Đọc tiếp
Hãy viết phương trình bằng chữ biểu diễn hiện tượng được mô tả sau đây
Để điều chế oxi người ta tiến hành nung thuốc tím ( kali pemanganat K M n O 4 ), thu được kali manganat K 2 M n O 4 ; mangan ddioxxit ( M n O 2 ) và khí oxi.
kali clorat được sử dụng để làm thuốc pháo, ngòi nổ, thuốc đầu diêm và là thuốc giúp nhãn ra hoa... cũng như thuốc tím, ở nhiệt độ cao (có mặt MnO2 làm xúc tác) kali clorat bị phân hủy giải phóng khí oxia, hãy viết pthh điều chế oxi từ thuốc tím và từ kali cloratb, nếu muốn thu được cùng một lượng khí oxi thì dùng hóa chất nào sẽ tiết kiệm được hóa chất hơn? giải thích?
Đọc tiếp
kali clorat được sử dụng để làm thuốc pháo, ngòi nổ, thuốc đầu diêm và là thuốc giúp nhãn ra hoa... cũng như thuốc tím, ở nhiệt độ cao (có mặt MnO2 làm xúc tác) kali clorat bị phân hủy giải phóng khí oxi
a, hãy viết pthh điều chế oxi từ thuốc tím và từ kali clorat
b, nếu muốn thu được cùng một lượng khí oxi thì dùng hóa chất nào sẽ tiết kiệm được hóa chất hơn? giải thích?
a)
$2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2$
$2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2$
b)
Coi n O2 = 1(mol)
Theo PTHH :
n KMnO4 = 2n O2 = 2(mol)
n KClO3 = 3/2 n O2 = 1,5(mol)
Ta thấy :
m KMnO4 = 2.158 =316 > m KClO3 = 122,5.1,5 = 183,75
Nên dùng KClO3 tiết kiệm được hóa chất hơn
Đúng 2
Bình luận (0)
a)
2KMnO4->K2MnO4+MnO2+O2
2KClO3->2KCl+3O2
b)
gọi a là số mol O2
=>nKMnO4=2a mol
nKClO3=2a/3 mol
mKMnO4=158x2a=316a g
mKClO3=122,5x2a/3=81,67a g
=> KClO3 tiết kiệm hơn
Đúng 0
Bình luận (1)
Để điều chế Oxi trong phòng thí nghiệm, một em học sinh nhiệt phân 24,5g kali clorat ( KClO3) thu được 9,6g khí Oxi và muối kali clorua ( KCl). a) Viết phương trình hóa học của phản ứng trên b) Viết công thức về khối lượng của phản ứng xảy ra c) Tính khối lượng muối kali clorua tạo ra.d) Cho biết lệ số phân tử Oxi với các chất còn lại trong phản ứngMọi người giúp mình.Cẻm ơn!
Đọc tiếp
Để điều chế Oxi trong phòng thí nghiệm, một em học sinh nhiệt phân 24,5g kali clorat ( KClO3) thu được 9,6g khí Oxi và muối kali clorua ( KCl).
a) Viết phương trình hóa học của phản ứng trên
b) Viết công thức về khối lượng của phản ứng xảy ra
c) Tính khối lượng muối kali clorua tạo ra.
d) Cho biết lệ số phân tử Oxi với các chất còn lại trong phản ứng
Mọi người giúp mình.Cẻm ơn!
\(a,PTHH:2KClO_3\rightarrow\left(^{t^o}_{MnO_2}\right)2KCl+3O_2\\ b,m_{KClO_3}=m_{KCl}+m_{O_2}\\ c,m_{KCl}=m_{KClO_3}-m_{O_2}=14,9\left(g\right)\\ d,\text{Số phân tử }O_2:\text{Số phân tử }KCl=3:2\\ \text{Số phân tử }O_2:\text{Số phân tử }KClO_3=3:2\)
Đúng 3
Bình luận (0)
Hãy viết các phương trình hóa học sau đây:
a/ Nhiệt phân thuốc tím KMnO4
b/ Điều chế khí hydrogen (hidro) từ kim loại sắt và hydrochloride acid (axit clohidric) HCl
c/ Điện phân nước
d/ Phản ứng giữa P2O5. và nước
e/ Đốt cháy kim loại kẽm trong khí oxigen (oxi)
Hãy viết các phương trình hóa học sau đây:
a/ Nhiệt phân thuốc tím KMnO4
2KMNO4-to>K2MnO4+MnO2+O2
b/ Điều chế khí hydrogen (hidro) từ kim loại sắt và hydrochloride acid (axit clohidric) HCl
Fe+2HCl->FeCl2+H2
c/ Điện phân nước
2H2O-đp->2H2+O2
d/ Phản ứng giữa P2O5. và nước
P2O5+3H2O->2H3PO4
e/ Đốt cháy kim loại kẽm trong khí oxigen (oxi)
2Zn+O2-to>2ZnO
Đúng 2
Bình luận (0)
`a)` `2KMnO_4` $\xrightarrow[]{t^o}$ `K_2MnO_4 + MnO_2 + O_2`
`b) Fe + 2HCl -> FeCl_2 + H_2`
`c)` `2H_2O` $\xrightarrow[]{đpnc}$ `2H_2 + O_2`
`d) P_2O_5 + 3H_2O -> 2H_3PO_4`
`e) 2Zn + O_2` $\xrightarrow[]{t^o}$ `2ZnO`
Đúng 0
Bình luận (1)
Từ M n O 2 , dung dịch H C l , K C l O 3 và cacbon, viết phương trình hóa học để điều chế các khí: clo, oxi, cacbon đioxit.
1. khí oxi tác dụng được với:A. CO2, Fe, C B. Na2O, CH4, H2C. CaCO3, P, CH4D. C2H4, C, K2.Dãy chất dùng để điều chế oxi trong phòng thí nghiệm:A. Nước, thuốc tímB. Không khí, nướcC. thuốc tím, kali cloratD. kali nitrat, nước3.có thể thu khí hidro bằng cách đẩy nước vì:A. khí hidro nhẹ hơn ko khíB. khí hidro tan rất ít trong nướcC. khí hidro tan nhiều trong nướcD. thu khí hidro bằng cách đặt úp ống nghiệm4.kim loại nào sau đây tác dụng với nước ở nhiệt dộ thường tạo thành dd bazo và khí hidro?A....
Đọc tiếp
1. khí oxi tác dụng được với:
A. CO2, Fe, C
B. Na2O, CH4, H2
C. CaCO3, P, CH4
D. C2H4, C, K
2.Dãy chất dùng để điều chế oxi trong phòng thí nghiệm:
A. Nước, thuốc tím
B. Không khí, nước
C. thuốc tím, kali clorat
D. kali nitrat, nước
3.có thể thu khí hidro bằng cách đẩy nước vì:
A. khí hidro nhẹ hơn ko khí
B. khí hidro tan rất ít trong nước
C. khí hidro tan nhiều trong nước
D. thu khí hidro bằng cách đặt úp ống nghiệm
4.kim loại nào sau đây tác dụng với nước ở nhiệt dộ thường tạo thành dd bazo và khí hidro?
A. Fe B.Mg C. Ba D. Zn
5. đốt cháy chất nào sau đây tạo ra sản phẩm là CO2 và H20?
A. H2 B. P C. Mg D. C3H8
6. chất nào sau đây phản ứng với nước tạo thành bazo?
A.SO3 B. P2O5 C.FeO D. K2O
7. chất nào sau đây phản ứng với nước tạo thành axit?
A. CO2 B. CaO C. FeO D. Na
8.rót nước vào ống nghiệm có chứa một ít vôi sống CaO, cho mẫu quì tím vào dd tạo thành. Hiện tượng quan sát được là:
A. quì tím chuyển sang màu đỏ
B. quì tím chuyển sang màu xanh
C. quì tím bị mất màu
D. quì tím ko bị mất màu
9.dãy kim loại tác dụng được với nước ở điều kiện thường:
A. K, Na, Cu B. Zn, Ca,K C. Ca, Li, Fe D. Li, Ba, K
10. dãy oxit tác dụng được với nước tạo thành dd bazo:
A. PbO, Na2O, CuO
B. ZnO, CaO, K2O
C. BaO, K2O, Fe2O3
D. Na2O, BaO, K2O
1. khí oxi tác dụng được với:
A. CO2, Fe, C
B. Na2O, CH4, H2
C. CaCO3, P, CH4
D. C2H4, C, K
2.Dãy chất dùng để điều chế oxi trong phòng thí nghiệm:
A. Nước, thuốc tím
B. Không khí, nước
C. thuốc tím, kali clorat
D. kali nitrat, nước
3.có thể thu khí hidro bằng cách đẩy nước vì:
A. khí hidro nhẹ hơn ko khí
B. khí hidro tan rất ít trong nước
C. khí hidro tan nhiều trong nước
D. thu khí hidro bằng cách đặt úp ống nghiệm
4.kim loại nào sau đây tác dụng với nước ở nhiệt dộ thường tạo thành dd bazo và khí hidro?
A. Fe B.Mg C. Ba D. Zn
5. đốt cháy chất nào sau đây tạo ra sản phẩm là CO2 và H20?
A. H2 B. P C. Mg D. C3H8
6. chất nào sau đây phản ứng với nước tạo thành bazo?
A.SO3 B. P2O5 C.FeO D. K2O
7. chất nào sau đây phản ứng với nước tạo thành axit?
A. CO2 B. CaO C. FeO D. Na
8.rót nước vào ống nghiệm có chứa một ít vôi sống CaO, cho mẫu quì tím vào dd tạo thành. Hiện tượng quan sát được là:
A. quì tím chuyển sang màu đỏ
B. quì tím chuyển sang màu xanh
C. quì tím bị mất màu
D. quì tím ko bị mất màu
9.dãy kim loại tác dụng được với nước ở điều kiện thường:
A. K, Na, Cu B. Zn, Ca,K C. Ca, Li, Fe D. Li, Ba, K
10. dãy oxit tác dụng được với nước tạo thành dd bazo:
A. PbO, Na2O, CuO
B. ZnO, CaO, K2O
C. BaO, K2O, Fe2O3
D. Na2O, BaO, K2O
Đúng 6
Bình luận (0)
1. khí oxi tác dụng được với:
A. CO2, Fe, C
B. Na2O, CH4, H2
C. CaCO3, P, CH4
D. C2H4, C, K
2.Dãy chất dùng để điều chế oxi trong phòng thí nghiệm:
A. Nước, thuốc tím
B. Không khí, nước
C. thuốc tím, kali clorat
D. kali nitrat, nước
3.có thể thu khí hidro bằng cách đẩy nước vì:
A. khí hidro nhẹ hơn ko khí
B. khí hidro tan rất ít trong nước
C. khí hidro tan nhiều trong nước
D. thu khí hidro bằng cách đặt úp ống nghiệm
4.kim loại nào sau đây tác dụng với nước ở nhiệt dộ thường tạo thành dd bazo và khí hidro?
A. Fe B.Mg C. Ba D. Zn
5. đốt cháy chất nào sau đây tạo ra sản phẩm là CO2 và H20?
A. H2 B. P C. Mg D. C3H8
6. chất nào sau đây phản ứng với nước tạo thành bazo?
A.SO3 B. P2O5 C.FeO D. K2O
7. chất nào sau đây phản ứng với nước tạo thành axit?
A. CO2 B. CaO C. FeO D. Na
8.rót nước vào ống nghiệm có chứa một ít vôi sống CaO, cho mẫu quì tím vào dd tạo thành. Hiện tượng quan sát được là:
A. quì tím chuyển sang màu đỏ
B. quì tím chuyển sang màu xanh
C. quì tím bị mất màu
D. quì tím ko bị mất màu
9.dãy kim loại tác dụng được với nước ở điều kiện thường:
A. K, Na, Cu B. Zn, Ca,K C. Ca, Li, Fe D. Li, Ba, K
10. dãy oxit tác dụng được với nước tạo thành dd bazo:
A. PbO, Na2O, CuO
B. ZnO, CaO, K2O
C. BaO, K2O, Fe2O3
D. Na2O, BaO, K2O
Đúng 5
Bình luận (0)
Trong phòng thí nghiệm người ta có thể điều chế oxi bằng cách đốt nóng kali clorat:
2
K
C
l
O
3
(
r
ắ
n
)
→
t
0
2
K
C...
Đọc tiếp
Trong phòng thí nghiệm người ta có thể điều chế oxi bằng cách đốt nóng kali clorat:
2 K C l O 3 ( r ắ n ) → t 0 2 K C l ( r ắ n ) + 3 O 2 ( k h í )
Hãy dùng phương trình hóa học trên nên trả lời những câu hỏi sau:
Muốn điều chế được 4,48 lit khí oxi (đktc) cần dùng bao nhiêu gam K C l O 3 ?
Đốt cháy 7,8 g kim loại Kali trong khí Oxi sinh ra Kali oxit. Viết phương trình hóa học của phản ứng. Tính khối lượng Kali oxit sinh ra. Tính thể tích của khí Oxi đã phản ứng ở điều kiện tiêu chuẩn. Tính thể tích không khí cần dùng biết khí oxi chiếm...
Xem chi tiết
nK=0,2(mol)
PTHH: 4K + O2 -to-> 2 K2O
nK2O= 0,1(mol) => mK2O=0,1.94=9,4(g)
nO2=0,05(mol) -> V(O2,đktc)=0,05.22,4=1,12(l)
V(kk,dktc)=5.V(O2,dktc)=5.1,12=5,6(l)
Đúng 1
Bình luận (0)
(giúp mình với nha)Lấy cùng 1 lượng KClO3 và KMnO4 để điều chế khí oxi, chất nào cho nhiều khí oxi hơn? Viết phương trình hóa học và giải thích
\(2KClO_3\rightarrow\left(t^o,MnO_2\right)2KCl+3O_2\)
\(\dfrac{m}{122,5}\) \(\dfrac{3m}{245}\) ( mol )
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
\(\dfrac{m}{158}\) \(\dfrac{m}{316}\) ( mol )
So sánh:
\(\dfrac{3m}{245}\) > \(\dfrac{m}{316}\)
=> \(KClO_3\) cho nhiều O2 hơn
Đúng 1
Bình luận (7)