Số gam KMnO4 cần phân hủy để điều chế được 2,24 lít khí oxi (đktc) là:
A. 20,7g
B. 42,8g
C. 14,3g
D. 31,6g
để điều chế được 6,72 lít khí oxi cần phân hủy bao nhiêu gam KMnO4 biết hiệu suất phân hủy là 90%
2KMnO4-to>K2MnO4+MnO2+O2
0,6------------------------------------0,3 mol
n O2=\(\dfrac{6,72}{22,4}\)=0,3 mol
=>m KMnO4pứ=0,6.158.\(\dfrac{100}{90}\)=105,33g
Số gam KMnO4 cần dùng để điều chế được 2,24 lít khí oxi (đktc) là (K = 39, Mn = 55, O = 16) A. 20,7g B. 42,8g C. 14,3g D. 31,6g
Ko cần giải thích học ngu lắm :))
\(pthh:2KMnO_4\overset{t^o}{--->}K_2MnO_4+MnO_2+O_2\uparrow\)
\(n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo pt: \(n_{KMnO_4}=0,2\left(mol\right)\)
\(\Rightarrow m_{KMnO_4}=0,2.158=31,6\left(g\right)\)
Chọn D
Nhiệt phân hoàn toàn 31,6 gam KMnO4 để điều chế oxi. Thể tích khí O2 thu được ở đktc là:
(K = 39; Mn = 55; O = 16)
A.8,96 lít
B.4,48 lít
C.1,12 lít
D.2,24 lít
Nhiệt phân hoàn toàn 31,6 gam KMnO4 để điều chế oxi. Thể tích khí O2 thu được ở đktc là:
(K = 39; Mn = 55; O = 16)
A.
8,96 lít
B.
4,48 lít
C.
1,12 lít
D.
2,24 lít
Tham khảo:
= 31,6/158 = 0,2 (mol)
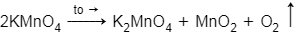
⇒ V = 0,1.22,4 = 2,24 (lít)
Tính khối lượng KMnO4 cần dùng để điều chế được lượng oxi là 11,2 lít , biết hiệu suất phản ứng phân hủy đạt 80% (các chất khí đo ở đktc)
\(n_{O_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
1<------------------------------------0,5
=> \(m_{KMnO_4\left(pthh\right)}=1.158=158\left(g\right)\)
=> \(m_{KMnO_4\left(tt\right)}=\dfrac{158.100}{80}=197,5\left(g\right)\)
Câu 3: Tính số mol và số gam thuốc tím cần để điều chế được:
1. 48 gam khí oxi.
2,24 lít khí oxi ở đktc
1) nO2= 48/32=1,5(mol)
PTHH: 2 KMnO4 -to-> K2MnO4 + MnO2 + O2
nKMnO4=2.1,5=3(mol)
=>mKMnO4=158.3= 474(g)
2) nO2=2,24/22,4=0,1(mol)
nKMnO4=2.0,1=0,2(mol)
-> mKMnO4=158.0,2= 31,6(g)
Bài 6: Nung nóng Kali pemanganat KMnO4 thu được K2MnO4, MnO2 và khí O2. Hãy tính khối lượng KMnO4 cần thiết để điều chế 16,8 lít khí oxi (đktc).
Bài 7: a, Tính số gam sắt và oxi cần dung để điều chế 4,64g oxit sắt từ Fe3O4. b, Tính số gam Kali clorat KClO3 cần dùng để có lượng oxi dùng cho phản ứng trên.
Câu 6.
\(n_{O_2}=\dfrac{16,8}{22,4}=0,75mol\)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
1,5 0,75
\(m_{KMnO_4}=1,5\cdot158=237g\)
Câu 7.
\(n_{Fe_3O_4}=\dfrac{4,64}{232}=0,02mol\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
0,04 0,02
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
\(\dfrac{2}{75}\) 0,04
\(m_{KClO_3}=\dfrac{2}{75}\cdot122,5=\dfrac{49}{15}\approx3,27g\)
Bài 6 :
\(n_{O_2}=\dfrac{16.8}{22,4}=0,75\left(mol\right)\)
PTHH : 2KMnO4 ----t0-----> K2MnO4 + MnO2 + O2
1,5 0,75
\(m_{KMnO_4}=1,5.158=237\left(g\right)\)
Phân hủy KMnO4,thu được K2Mn04;MnO2 và 2,24 lít khí oxi ở đktc. a)Viết phương trình hóa học xảy ra ? b)Tính khối lượng KMnO4 cần đem đi phân hủy? c)Nếu dùng hết lượng oxi trên tác dụng với thể tích của H2 là bao nhiêu lít để tạo ra hỗn hợp nổ mạnh.
nO2 = 2,24/22,4 = 0,1 (mol)
PTHH: 2KMnO4 -> (t°) K2MnO4 + MnO2 + O2
nKMnO4 = 0,1 . 2 = 0,2 (mol)
mKMnO4 = 0,2 . 158 = 31,6 (g(
Để tạo hh nổ mạnh nhất thì VH2 : VO2 = 2 : 1
=> VH2 = VO2 . 2 = 2,24 . 2 = 4,48 (l)
14.Khối lượng Kali pemanganat KMnO 4 cần thiết để điều chế được 13,95 lít khí oxi (ở 25 o C và 1 bar) là:
A. 15,8g B. 31,6g C. 15g D. 31g
15. Đốt 12,8 gam đồng trong bình chứa 8,37 lit khí oxi (ở 25 o C và 1 bar). Lượng đồng(II)
oxit thu được là:
A. 48 gam B. 8 gam C. 32 gam D. 16 gam
nCH4 = 11.2/22.4 = 0.5 Mol
CH4 + 2O2 -to-> CO2 + 2H2O
0.5____1
2KMnO4 -to-> K2MnO4 + MnO2 + O2
2_____________________________1
mKMnO4 = 2 *158 = 316 (g)