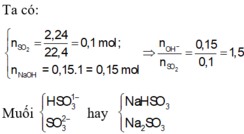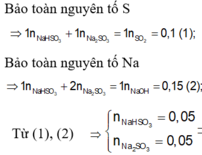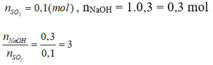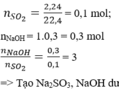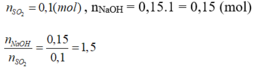cho 2,24 l khí SO2 hấp thụ vào 150 ml NaOH 1M Tính m muối sau pứ

Những câu hỏi liên quan
Cho 2,24 lít SO2 (đktc) hấp thụ hết vào 150 ml dung dịch NaOH 1M thu được dung dịch Y. Khối lượng muối có trong dung dịch Y là: A. 11,5 gam B. 12,6 gam C. 10,4 gam D. 9,64 gam
Đọc tiếp
Cho 2,24 lít SO2 (đktc) hấp thụ hết vào 150 ml dung dịch NaOH 1M thu được dung dịch Y. Khối lượng muối có trong dung dịch Y là:
A. 11,5 gam
B. 12,6 gam
C. 10,4 gam
D. 9,64 gam
1. Cho 2240 ml khí H2S (ở đktc) hấp thụ hết vào 200 ml dung dịch NaOH 1M. Sau phản ứng thu được ?
2. Cho 2240 ml khí SO2 (ở đktc) hấp thụ hết vào 200 ml dung dịch NaOH 1M. Sau phản ứng thu được ?
1) \(n_{H_2S}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{NaOH}=0,2.1=0,2\left(mol\right)\)
Xét \(\dfrac{n_{NaOH}}{n_{H_2S}}=\dfrac{0,2}{0,1}=2\) => Tạo muối Na2S
PTHH: 2NaOH + H2S --> Na2S + 2H2O
0,2------------>0,1
=> mNa2S = 0,1.78 = 7,8 (g)
2)
\(n_{SO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{NaOH}=0,2.1=0,2\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{n_{NaOH}}{n_{SO_2}}=\dfrac{0,2}{0,1}=2\) => Tạo muối Na2SO3
PTHH: 2NaOH + SO2 --> Na2SO3 + H2O
0,2-------------->0,1
=> mNa2SO3 = 0,1.126 = 12,6 (g)
Đúng 1
Bình luận (0)
2. \(\left\{{}\begin{matrix}n_{SO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\n_{NaOH}=0,2.1=0,2\left(mol\right)\end{matrix}\right.\)
Ta có: \(T=\dfrac{0,2}{0,1}=2\) ⇒ tạo ra muối Na2SO3
SO2 + 2NaOH -----> Na2SO3 + H2O
Đúng 0
Bình luận (0)
Hấp thụ 2,24 lít khí SO2 (đktc) vào 300 ml dung dịch NaOH 1M, thu được dung dịch X. Chất tan trong X là A. Na2SO3 B. NaHSO3 C. Na2SO3, NaOH D. Na2SO3, NaHSO3
Đọc tiếp
Hấp thụ 2,24 lít khí SO2 (đktc) vào 300 ml dung dịch NaOH 1M, thu được dung dịch X. Chất tan trong X là
A. Na2SO3
B. NaHSO3
C. Na2SO3, NaOH
D. Na2SO3, NaHSO3
Hấp thụ 2,24 lít khí
S
O
2
(đktc) vào 300 ml dung dịch NaOH 1M, thu được dung dịch X. Chất tan trong X là A.
N
a
2
S
O
3
B.
N
a
H
S
O
3
C.
N
a
2
S
O
3
, NaOH D.
N...
Đọc tiếp
Hấp thụ 2,24 lít khí S O 2 (đktc) vào 300 ml dung dịch NaOH 1M, thu được dung dịch X. Chất tan trong X là
A. N a 2 S O 3
B. N a H S O 3
C. N a 2 S O 3 , NaOH
D. N a 2 S O 3 , N a H S O 3
Hấp thụ 2,24 lít
S
O
2
(đktc) vào 150 ml dung dịch NaOH 1M thu được dung dịch A. Chất tan có trong dung dịch A là A.
N
a
2
S
O
3
và NaOH dư. B.
N
a
2
S
O
3
. C.
N
a
H
S
O
3
. ...
Đọc tiếp
Hấp thụ 2,24 lít S O 2 (đktc) vào 150 ml dung dịch NaOH 1M thu được dung dịch A. Chất tan có trong dung dịch A là
A. N a 2 S O 3 và NaOH dư.
B. N a 2 S O 3 .
C. N a H S O 3 .
D. N a H S O 3 và N a 2 S O 3
Hấp thụ 2,24 lít SO2 (đktc) vào 150 ml dung dịch NaOH 1M thu được dung dịch A. Chất tan có trong dung dịch A là. A. Na2SO3 và NaOH dư B. Na2SO3 C. NaHSO3 D. NaHSO3 và Na2SO3
Đọc tiếp
Hấp thụ 2,24 lít SO2 (đktc) vào 150 ml dung dịch NaOH 1M thu được dung dịch A. Chất tan có trong dung dịch A là.
A. Na2SO3 và NaOH dư
B. Na2SO3
C. NaHSO3
D. NaHSO3 và Na2SO3
Câu 6: Hấp thụ 4,48 lít SO2 (đktc) vào 150 ml dung dịch NaOH 2M, thu được dung dịch chứa m gam muối. Tính giá trị của m
nSO2 = 4.48/22.4 = 0.2 (mol)
nNaOH = 0.15*2 = 0.3 (mol)
nNaOH / nSO2 = 0.3 / 0.2 = 1.5
=> Tạo ra 2 muối
Đặt :
nNa2SO3 = x mol
nNaHSO3 = y mol
=> 2x + y = 0.3
x + y = 0.2
=> x = y = 0.1
mNa2SO3 = 0.1*126 = 12.6 (g)
mNaHSO3 = 0.1*104 = 10.4 (g)
Đúng 2
Bình luận (0)
nNaOH= 0,3(mol); nSO2=0,2(mol)
Ta có: 2>nOH-/nSO2=0,3/0,2=1,5>1
=> Sản phẩm là hỗn hợp 2 muối: Na2SO3 và NaHSO3
PTHH: 2 NaOH + SO2 -> Na2SO3 + H2O
2x____________x_____x(mol)
NaOH + SO2 -> NaHSO3
y_______y______y(mol)
Ta có hpt: \(\left\{{}\begin{matrix}x+y=0,2\\2x+y=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
=> m(muối)=mNa2SO3+ mNaHSO3= 126x+104y=126.0,1+104.0,1=23(g)
Đúng 2
Bình luận (0)
cho 3,2 g so2 hấp thụ hoàn toàn bởi V ml dd naoh 1M. sau phản ứng đem cô cạn dd 5,75g muối. Tính V NaOH tối thiểu phải dùng.
SO2+NaOH->NaHSO3
n So2=0,05 mol
Giả sử phản ứng tạo 1 muối NaHSO3
BTNT S: nNaHSO3 = nSO2 = 0,05 => m muối = 5,2 gam < 5,75 gam
Giả sử phản ứng tạo 1 muối Na2SO3
BTNT S: nNa2SO3 = nSO2 = 0,05 => m muối = 6,3 gam > 5,75 gam
Chứng tỏ phản ứng tạo hỗn hợp 2 muối NaHSO3 (a mol) và Na2SO3 (b mol)
\(\left\{{}\begin{matrix}a+b=0,05\\\text{104 a + 126 b = 5,75 }\end{matrix}\right.\)
a=0,025, b=0,025 mol
BTNT Na => n NaOH = 2n Na2SO3 + n NaHSO3 = 0,075 mol
VNaOH = 0,075 :1 = 0,075 lít = 75ml
Đúng 4
Bình luận (0)
SO2 + NaOH ---> \(\left[{}\begin{matrix}Na2SO3+H2O\\NaHSO3\end{matrix}\right.\)
nSO2 = \(\dfrac{3,2}{64}=0,05\left(mol\right)\)
Bảo toàn nguyên tố : nSO2 = nS (muối) = 0,05 (mol)
M (muối) = \(\dfrac{5,75}{0,05}=115\left(đvC\right)\)
Nhận thấy MNaHSO3 < M(muối) < MNa2SO3
=> Phản ứng tạo 2 muối
Gọi muối NaHSO3 là x , Na2SO3 là y
Ta có : \(\left\{{}\begin{matrix}x+y=0,05\\104x+126y=5,75\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,025\\y=0,025\end{matrix}\right.\)
Bảo toàn Na : 0,025.1 + 0,025.2 = 0,075 ( mol )
=> V NaOH = n/Cm = 75 ( ml )
Đúng 2
Bình luận (0)
Cho 2,24 lít (đktc) SO2 hấp thụ hoàn toàn vào 200 ml dung dịch NaOH 1,5 M. Dung dịch thu được sau phản ứng chứa chất nào?
n SO2=0,1 mol, n NaOH=0,3 mol
=>\(\dfrac{nNaOH}{nSO2}\)=3
Tạo Na2SO3
SO2 + 2NaOH → Na2SO3 + H2O
=> thu đc Na2CO3, NaOH dư
Đúng 3
Bình luận (1)