Người ta dùng 120 tấn quặng pirit có chứa 10% tạp chất để sản xuất Fe ta thu được 48. tấn sắt. Tính hiệu suất phản ứng trên

Những câu hỏi liên quan
Người ta dùng 120 tấn quặng sắt pirit có chứa 10% tạp chất để sản xuất Fe ta thu được 48 tấn sắt. Tính hiệu suất phản ứng
mtạp chất=120.10%=12(tấn)
mFeS2=120-12=108(tấn)
mFe lý thuyết=\(\dfrac{108}{120}.56=50,4\left(tấn\right)\)
H=\(\dfrac{48}{50,4}.100\%=95,238\%\)
Đúng 0
Bình luận (0)
tính khối lượng quặng pirit sắt chứa 90% FeS2 còn lại là tạp chất trơ cần dùng để sản xuất 5000 tấn Fe . giả sử hiệu suất phản ứng đạt 89,6%
\(n_{Fe} = \dfrac{5000.1000}{56} = \dfrac{625000}{7}\ kmol\\ n_{FeS_2\ đã\ dùng} = \dfrac{n_{Fe}}{H\%} = \dfrac{\dfrac{625000}{7}}{89,6\%} = 99649,23\ kmol\\ m_{quăng\ pirit} = \dfrac{m_{FeS_2}}{90\%} = \dfrac{99649,23.120}{90\%} = 13259897,33 (kg) = 13259,89(tấn)\)
Đúng 1
Bình luận (0)
\(n_{Fe}=\dfrac{5000\cdot10^6}{56}=\dfrac{625}{7}\cdot10^6\left(mol\right)\)
\(BTFe:\)
\(n_{FeS_2}=n_{Fe}=\dfrac{625}{7}\cdot10^6\left(mol\right)\)
\(n_{FeS_2\left(tt\right)}=\dfrac{\dfrac{625}{7}\cdot10^6}{89.6}=\dfrac{56000\cdot10^6}{7}\left(mol\right)\)
\(\Rightarrow m_{FeS_2}=\dfrac{56000\cdot10^6\cdot120}{7}=960000\cdot10^6\left(g\right)=960000\left(tấn\right)\)
\(m_{quặng}=\dfrac{960000\cdot100}{90}=1066666.67\left(tấn\right)\)
Đúng 0
Bình luận (0)
Để sản xuất được 16,9 tấn oleum H2SO4.3SO3 phải dùng m tấn quặng pirit sắt chứa 10% tạp chất trơ, hiệu suất của quá trình sản xuất là 80%. Giá trị của m là: A. 16,67 tấn B. 8,64 tấn C. 14,33 tấn D. 12 tấn
Đọc tiếp
Để sản xuất được 16,9 tấn oleum H2SO4.3SO3 phải dùng m tấn quặng pirit sắt chứa 10% tạp chất trơ, hiệu suất của quá trình sản xuất là 80%. Giá trị của m là:
A. 16,67 tấn
B. 8,64 tấn
C. 14,33 tấn
D. 12 tấn
Đáp án A
Để đơn giản về tính toán thì ta xem đơn vị tấn như gam.

Quặng này chứa 10% tạp chất trơ tức
FeS2 chiếm 90%.
Vậy khối lượng quặng pirit sắt cần:
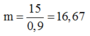
Đúng 0
Bình luận (0)
Để sản xuất được 16,9 tấn oleum H2SO4.3SO3 phải dùng m tấn quặng pirit sắt chứa 10% tạp chất trơ, hiệu suất của quá trình sản xuất là 80%. Giá trị của m là:
A. 16,67 tấn
B. 8,64 tấn
C. 14,33 tấn
D. 12 tấn
Đáp án A
Để đơn giản về tính toán thì ta xem đơn vị tấn như gam.

Đúng 0
Bình luận (0)
Để sản xuất sắt, người ta đưa vào lò 250 tấn quặng hematit có chứa 60% Fe2O3, còn lại là tạp chất rắn không phản ứng rồi khử bằng khí CO. Tính khối lượng sắt thu được biết hiệu suất của nó chỉ đạt 90%.
Mình cần gấp lắm, giúp mình với
K/lượng của Fe2O3 nguyên chất trong 250 tấn quặng hematit là :
250.60%=150(tấn)
=150000000(g)
Fe2O3+3CO-->2Fe+3CO2
Số mol của Fe2O3 là:
n=m/M=150000000:160
=937500(mol)
Số mol của Fe là:
nFe=2nFe2O3=2.937500
=1875000(mol)
K/lượng của Fe là:
m=n.M=1875000.56
=105000000(g)
K/lượng của Fe nếu hiệu suất chỉ đạt 90% là:
105000000.90%
=94500000(g)
=94,5 tấn
Mình không biết là đúng hay sai nha
Đúng 0
Bình luận (1)
Để thu được 89,03 tấn H2SO4 người ta sử dụng 68 tấn quặng pirit chứa 50%S,còn lại là tạp chất. Hỏi hiệu suất của quá trình sản xuất axit là bao nhiêu?
mS = 68*50/100=34 tấn
Sơ đồ sản xuất :
S ---------------------> H2SO4
32_________________98
34_________________x
x = 34*98/32=104.125 tấn
H = 89.03/104.125*100% = 85.5%
Đúng 0
Bình luận (0)
Trong công nghiệp người ta sản xuất axít sunfuric theo sơ đồ sau: FeS2
→
SO2
→
SO3
→
H2SO4 . Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axít sunfuric từ quặng trên là: A. 40% B. 60% C. 80% D. 62,5%
Đọc tiếp
Trong công nghiệp người ta sản xuất axít sunfuric theo sơ đồ sau: FeS2 → SO2 → SO3 → H2SO4 . Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axít sunfuric từ quặng trên là:
A. 40%
B. 60%
C. 80%
D. 62,5%
Trong công nghiệp người ta sản xuất axit sunfuric theo sơ đồ sau: FeS2 → SO2 → SO3 → H2SO4. Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axit sunfuric từ quặng trên là: A. 40%. B. 60%. C. 80%. D. 62,5%
Đọc tiếp
Trong công nghiệp người ta sản xuất axit sunfuric theo sơ đồ sau:
FeS2 → SO2 → SO3 → H2SO4.
Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axit sunfuric từ quặng trên là:
A. 40%.
B. 60%.
C. 80%.
D. 62,5%
Đáp án C.
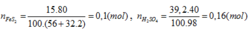
FeS2→ 2H2SO4
0,08 ← 0,16 (mol)
H% = 0,08.100/0,1= 80%
Đúng 0
Bình luận (0)
từ 150 kg quặng pirit sắt có chứa 10% tạp chất người ta sản xuất được 250 kg dd H2SO4 80%. Tính hiệu suất của quá trình sản xuất


















