Phân biệt và viết phương trình tổng quát cho mỗi loại phản ứng: hóa hợp, phân hủy, phản ứng thế, sự oxi hóa

Những câu hỏi liên quan
nêu các khái niệm sự oxi hóa phản ứng hóa hợp, phản ứng phân hủy, sự cháy, sự oxi hóa chậm, phản ứng thế
Các khái niệm sự oxi hóa phản ứng hóa hợp, phản ứng phân hủy, sự cháy, sự oxi hóa chậm, phản ứng:
- Sự oxi hóa là sự tác dụng của oxi với một chất (chất đó có thể là đơn chất hoặc hợp chất).
- Phản ứng hóa hợp là phản ứng hóa học trong đó có một chất mới được tạo thành từ hai hay nhiều chất ban đầu.
- Phản ứng phân hủy là một phản ứng hóa học mà trong đó một chất tham gia có thể tạo thành hai hay nhiều chất mới.
- Sự cháy là phản ứng oxy hóa khử nhiệt độ cao giữa chất đốt và chất oxy hóa, có sinh ra ngọn lửa sáng
- Sự oxi hóa chậm là sự oxi hóa có tỏa nhiệt nhưng không phát sáng.
- Phản ứng thế là phản ứng hóa học, trong đó một nguyên tố có độ hoạt động hóa học mạnh sẽ thay thế cho nguyên tố có độ hoạt động hóa học yếu hơn trong hợp chất của nguyên tố này
Đúng 0
Bình luận (0)
Câu 1: Hoàn thành các phương trình hoa học sau và cho biết đâu là phản ứng hóa hợp, phản ứng phân hủy, đâu là phản ứng có xảy ra sự oxi hóa?1) KClO3 ---to, MnO2--? + ? 6) Ca + ? --to-- CaO2) KMnO4 --to--? + ? + ? 7) ? + ? --to-- P2O53) K + O2 --to-- ? 8) ? + O2 --to-- H2O4) ? + O2 --to-- ? 9) H2 + ? --to-- Fe + ?5) C2H2 + ? --to-- ...
Đọc tiếp
Câu 1: Hoàn thành các phương trình hoa học sau và cho biết đâu là phản ứng hóa hợp, phản ứng phân hủy, đâu là phản ứng có xảy ra sự oxi hóa?
1) KClO3 ---to, MnO2-->? + ? 6) Ca + ? --to--> CaO
2) KMnO4 --to-->? + ? + ? 7) ? + ? --to--> P2O5
3) K + O2 --to--> ? 8) ? + O2 --to--> H2O
4) ? + O2 --to--> ? 9) H2 + ? --to--> Fe + ?
5) C2H2 + ? --to--> ? + H2O 10) Fe + ? --to--> Fe3O4
1) 2 KClO3 ---to, MnO2-->2KCl+3O2 (phân hủy )
6) 2Ca + O2 --to-->2 CaO hóa hợp
2) 2 KMnO4 --to-->K2MnO4+MnO2+O2 (phân hủy )
7) 4P+5O2 --to--> 2P2O5 hóa hợp
3) 4 K + O2 --to-->2 K2O hóa hợp
8)2 H2 + O2 --to--> 2H2O hóa hợp
4) C + O2 --to--> CO2 hóa hợp
9) H2 + FeO --to--> Fe + H2O (oxi hóa)
5) C2H2 + \(\dfrac{5}{2}\)O2 --to--> 2CO2 + H2O (oxi hóa)
10) 3Fe +2O2 --to--> Fe3O4 hóa hợp
Đúng 2
Bình luận (0)
câu 2.so sánh sự giống nhau và khác nhau và phản ứng phân hủy? lấy ví dụ mỗi loại phản ứng phương trình hóa học?
Giống nhau:
Đều là phản ứng hóa học
Khác nhau:
-Phản ứng hóa hợp là từ 2 hay nhiều chất tham gia tạo thành 1 sản phẩm
-Phản ứng phân hủy là từ 1 chất tham gia tạo thành 2 hay nhiều sản phẩm
VD:
\(S+O_2\rightarrow\left(t^o\right)SO_2\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
\(CaCO_3\rightarrow\left(t^o\right)CaO+CO_2\)
Đúng 0
Bình luận (0)
Loại phản ứng hóa học nào sau đây luôn luôn là phản ứng oxi hóa
A. phản ứng hóa hợp
B. phản ứng phân hủy
C. phản ứng thế
D. phản ứng trao đổi
Loại phản ứng nào sau đây luôn luôn không là loại phản ứng oxi hóa – khử?
A. Phản ứng hóa hợp.
B. Phản ứng phân hủy.
C. Phản ứng thế trong hóa vô cơ
D. Phản ứng trao đổi.
Loại phản ứng hóa học nào sau đây luôn luôn không phải là phản ứng oxi hóa - khử
A. phản ứng hóa hợp
B. phản ứng phân hủy
C. phản ứng thế
D. phản ứng trung hòa
Loại phản ứng nào sau đây luôn luôn là phản ứng oxi hóa – khử?
A. Phản ứng hóa hợp.
B. Phản ứng phân hủy.
C. Phản ứng thế trong hóa vô cơ.
D. Phản ứng trao đổi.
Lấy ba thí dụ phản ứng phân hủy là loại phản ứng oxi hóa – khử và ba thí dụ phản ứng phân hủy không là loại phản ứng oxi hóa – khử.
- Ba thí dụ phản ứng phân hủy là phản ứng oxi hóa – khử:
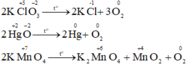
- Ba thí dụ phản ứng phân hủy không phải là phản ứng oxi hóa – khử:
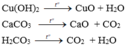
Đúng 0
Bình luận (0)
Nêu khái niệm phản ứng hóa hợp , phản ứng phân hủy, phản ứng thế ? Mỗi loại cho 1 vd
- Phản ứng hoá hợp là phản ứng chỉ có một chất sản phẩm tạo thành từ 2 hay nhiều chất ban đầu:
\(4Fe_3O_4+O_2\underrightarrow{t^o}6Fe_2O_3\)
- Phản ứng phân huỷ là có 2 hay nhiều chất tạo thành từ một chất ban đầu:
\(2Fe\left(OH\right)_3\underrightarrow{t^o}Fe_2O_3+3H_2O\)
- Phản ứng thế là phản ứng xảy ra giữa đơn chất với hợp chất, trong đó nguyên tử của đơn chất thay thế cho nguyên tử của 1 nguyên tố trong hợp chất:
\(2NaBr+Cl_2\rightarrow2NaCl+Br_2\uparrow\)
Đúng 3
Bình luận (0)















