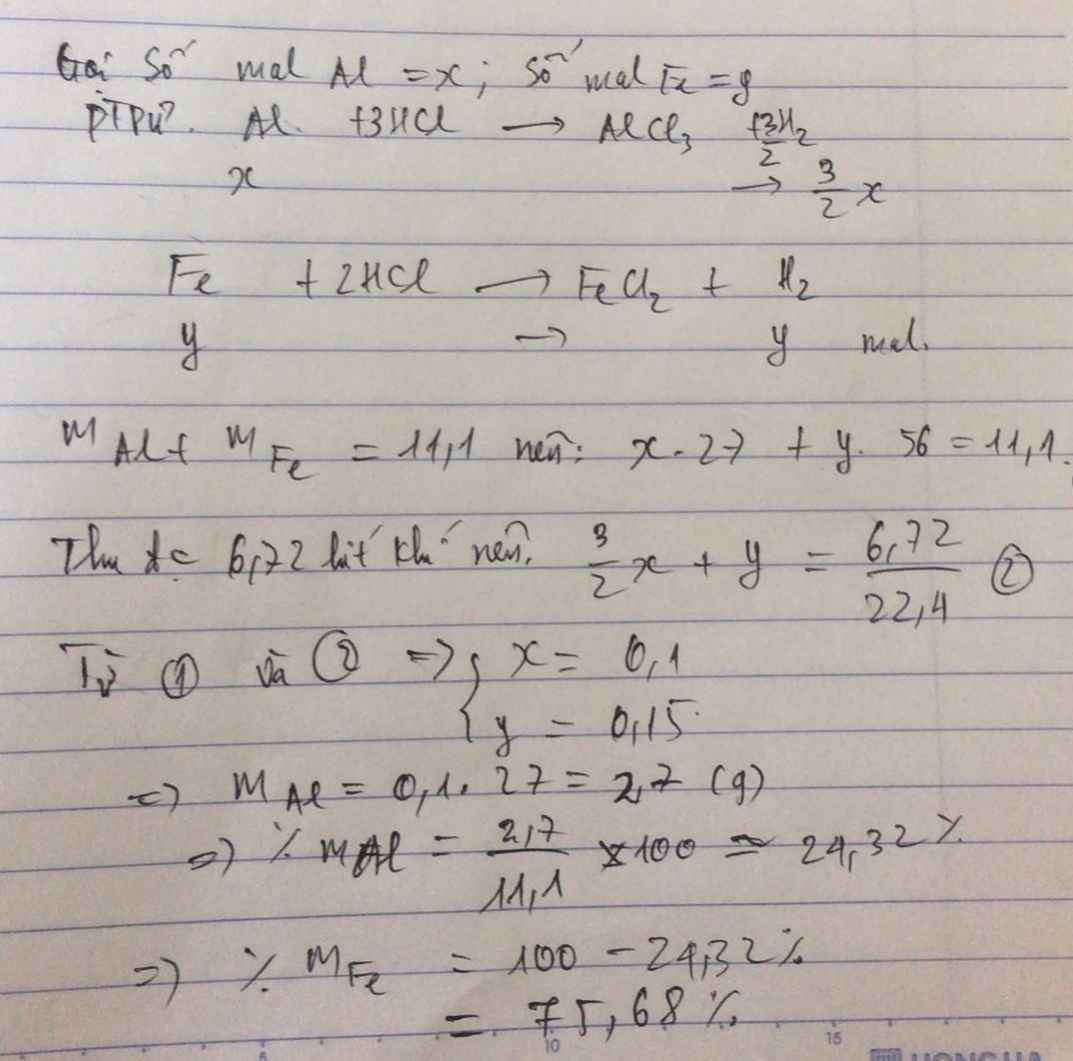Bài 14: Cho a gam hỗn hợp A gồm Mg, CuO tác dụng vừa đủ với 500 ml dung dịch HCl 1M thu được 3,36 lít khí H2 ở đktc. Tính a=?

Những câu hỏi liên quan
Bài 1: Cho 1,4 gam hỗn hợp gồm Mg và Fe tác dụng vừa đủ với với 160 ml dung dịch HCl 2M, sau phản ứng ta thu được 3,584 lít H2 ở đktc. Tính khối lượng muối khan thu được.
Bài 2: Cho 11,9g hỗn hợp gồm Zn, Mg, Al tác dụng với khí oxi thu được 18,3g hỗn hợp chất rắn. Tính thể tích khí oxi đã phản ứng (đktc)?
Bài 1:
\(n_{HCl}=2.0,16=0,32\left(mol\right);n_{H_2}=\dfrac{3,584}{22,4}=0,16\left(mol\right)\)
PTHH: Mg + 2HCl → MgCl2 + H2
PTHH: Fe + 2HCl → FeCl2 + H2
\(m_{H_2}=0,16.2=0,32\left(g\right)\)
\(m_{HCl}=0,32.36,5=11,68\left(g\right)\)
Theo ĐLBTKL ta có: \(m_{MgCl_2+FeCl_2}=1,4+11,68-0,32=12,76\left(g\right)\)
Đúng 1
Bình luận (0)
Bài 12:
Theo ĐLBTKL, ta có:
\(m_{hhkl}+m_{O_2}=m_{hh.oxit}\\ \Leftrightarrow11,9+m_{O_2}=18,3\\ \Leftrightarrow m_{O_2}=18,3-11,9=6,4\left(g\right)\\ n_{O_2}=\dfrac{6,4}{32}=0,2\left(mol\right)\\ V_{O_2\left(đktc\right)}=0,2.22,4=4,48\left(l\right)\)
Đúng 1
Bình luận (0)
Cho m gam hỗn hợp A gồm: Al, Na, Mg tác dụng với nước dư thu được 2,24 lít khí H2. Nếu lấy 2m gam hỗn hợp A tác dụng với dung dịch NaOH dư thu được 8,96 lít khí H2. Nếu lấy 3m gam hỗn hợp A tác dụng với dung dịch HCl vừa đủ thu được 22,4 lít khí H2. Biết các thể tích khí đo ở đktc, tính m và phần trăm về khối lượng của từng kim loại trong A
Đặt x,y, z lần lượt là số mol của Na,Al,Mg trong m gam hỗn hợp A
m gam A + H2O dư
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
x--------------------x--------->0,5x
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
x<------x-------------------------------------->1,5x
=> \(0,5x+1,5x=\dfrac{2,24}{22,4}=0,1\left(mol\right)\) (1)
2m gam A + NaOH
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
2x------------------------------->x
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
2y---------------------------------------------->3y
=> \(x+3y=\dfrac{8,96}{22,4}=0,4\left(mol\right)\) (2)
3m gam A + HCl
\(Na+HCl\rightarrow NaCl+\dfrac{1}{2}H_2\)
3x--------------------------->1,5x
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
3y----------------------------->4,5y
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
3z----------------------------->3z
=> \(1,5x+4,5y+3z=\dfrac{22,4}{22,4}=1\left(mol\right)\) (3)
Từ (1), (2), (3) =>\(\left\{{}\begin{matrix}x=0,05\\y=\dfrac{7}{60}\\z=\dfrac{2}{15}\end{matrix}\right.\)
=> \(m_{Na}=0,05.23=1,15\left(g\right)\)
\(m_{Al}=\dfrac{7}{60}.27=3,15\left(g\right)\)
\(m_{Mg}=\dfrac{2}{15}.24=3,2\left(g\right)\)
=> \(m=1,15+3,15+3,2=7,5\left(g\right)\)
=> \(\%m_{Na}=\dfrac{1,15}{7,5}.100=15,33\%\)
\(\%m_{Al}=\dfrac{3,15}{7,5}.100=42\%\)
\(\%m_{Mg}=\dfrac{3,2}{7,5}.100=42,67\%\)
Đúng 2
Bình luận (0)
: Cho m gam hỗn hợp A gồm: Al, Na, Mg tác dụng với nước dư thu được 2,24 lít khí H2. Nếu lấy 2m gam hỗn hợp A tác dụng với dung dịch NaOH dư thu được 8,96 lít khí H2. Nếu lấy 3m gam hỗn hợp A tác dụng với dung dịch HCl vừa đủ thu được 22,4 lít khí H2. Biết các thể tích khí đo ở đktc, tính m và phần trăm về khối lượng của từng kim loại trong A
\(2Na+2H2O\rightarrow2NaOH+H2\left(1\right)\)
\(2Al+2NaOH+2H2O\rightarrow2NaAlO2+3H2\left(2\right)\)
\(2Al+6HCl\rightarrow2AlCl3+3H2\left(3\right)\)
\(2Na+2HCl\rightarrow2NaCl+H2\left(4\right)\)
\(Mg+2HCl\rightarrow MgCl2+H2\left(5\right)\)
\(n_{H2\left(1\right)}=0,1\left(mol\right)\rightarrow n_{Na}=0,2\left(mol\right)\rightarrow m_{Na}=4,6\left(g\right)\)
\(n_{H2\left(2\right)}=0,4\left(mol\right)\Rightarrow n_{Al}=\dfrac{4}{15}\left(mol\right)\Rightarrow m_{Al}=7,2\left(g\right)\)
\(\Rightarrow n_{H2\left(3\right)}=\dfrac{3}{2}n_{Al}=0,4\left(mol\right)\)
\(n_{H2\left(4\right)}=\dfrac{1}{2}n_{Na}=0,1\left(mol\right)\)
\(\Rightarrow n_{H2\left(5\right)}=1-0,4-0,1=0,5\left(mol\right)\)
\(\Rightarrow n_{Mg}=0,5\left(mol\right)\Rightarrow m_{Mg}=12\left(g\right)\)
\(\Rightarrow m=12+4,6+7,2=23,8\left(g\right)\)
\(\%m_{Na}=\dfrac{4,6}{23,8}.100\%=19,33\%\)
\(\%m_{Al}=\dfrac{7,2}{23,8}.100\%=30,25\%\)
\(\%m_{Mg}=100-19,33-30,25=50,42\%\)
Chúc bạn học tốt
Đúng 2
Bình luận (1)
Na vàHoà tan hoàn toàn 13,200 gam hỗn hợp K vào nước thu được dung dịch X và 4,48 lít khí H2 (đktc). Cho 5,200 gam hỗn hợp gồm Mg và Fe tác dụng với dung dịch HCl vừa đủ thu được dung dịch Y chứa m gam muối và 3,36 lít khí H2 (đktc). Cho X tác dụng với Y đến khi phản ứng hoàn toàn thu được x gam kết tủa. Giá trị của x là: A.12,000. B. 10,300. C. 14,875. D. 22,235.
Đọc tiếp
Na vàHoà tan hoàn toàn 13,200 gam hỗn hợp K vào nước thu được dung dịch X và 4,48 lít khí H2 (đktc). Cho 5,200 gam hỗn hợp gồm Mg và Fe tác dụng với dung dịch HCl vừa đủ thu được dung dịch Y chứa m gam muối và 3,36 lít khí H2 (đktc). Cho X tác dụng với Y đến khi phản ứng hoàn toàn thu được x gam kết tủa. Giá trị của x là:
A.12,000.
B. 10,300.
C. 14,875.
D. 22,235.
Đáp án B
Các phản ứng tạo kết tủa:
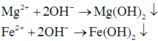
Dung dich X có ![]()
Dung dịch Y có ![]()
Mà ![]() nên OH-dư và
nên OH-dư và ![]()
Vậy ![]()
Đúng 0
Bình luận (0)
Hoà tan hoàn toàn 13,200 gam hỗn hợp Na và K vào nước thu được dung dịch X và 4,48 lít khí H2 (đktc). Cho 5,200 gam hỗn hợp gồm Mg và Fe tác dụng với dung dịch HCl vừa đủ thu được dung dịch Y chứa m gam muối và 3,36 lít khí H2 (đktc). Cho X tác dụng với Y đến khi phản ứng hoàn toàn thu được x gam kết tủa. Giá trị của m là: A. 10,525. B. 9,580. C. 15,850. D. 25,167.
Đọc tiếp
Hoà tan hoàn toàn 13,200 gam hỗn hợp Na và K vào nước thu được dung dịch X và 4,48 lít khí H2 (đktc). Cho 5,200 gam hỗn hợp gồm Mg và Fe tác dụng với dung dịch HCl vừa đủ thu được dung dịch Y chứa m gam muối và 3,36 lít khí H2 (đktc). Cho X tác dụng với Y đến khi phản ứng hoàn toàn thu được x gam kết tủa. Giá trị của m là:
A. 10,525.
B. 9,580.
C. 15,850.
D. 25,167.
cho 11,1 gam hỗn hợp gồm Al và Fe tác dụng vừa đủ với dung dịch V(ml) dung dịch HCl 1M thu được 6,72 lít khí H2 (đktc). phần trăm khối lượng mỗi kim loại tròn mỗi hỗn hợp trên
Gọi số mol Al, Fe là a, b (mol)
=> 27a + 56b = 11,1 (1)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
a----------------------->1,5a
Fe + 2HCl --> FeCl2 + H2
b------------------------>b
=> 1,5a + b = 0,3 (2)
(1)(2) => a = 0,1; b = 0,15
=> \(\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,1.27}{11,1}.100\%=24,32\%\\\%m_{Fe}=\dfrac{0,15.56}{11,1}.100\%=75,68\end{matrix}\right.\)
Đúng 4
Bình luận (0)
Cho 5g hỗn hợp X gồm Mg và Cu tác dụng với dung dịch HCl 14,6% (phản ứng vừa đủ), thu được dung dịch Y và 3,36 lít khí H2 (ở đktc)
a) Viết PTHH của phản ứng xảy ra
b) Tính % theo khối lượng của mỗi kim loại trong hhX?
c) Tính Khối lượng dung dịch HCl đã dùng
d) Tính nồng độ % của dung dịch Y
a. PTHH : Mg + 2HCl ➝ MgCl2 + H2 (1)
b. theo bài : nH2 = 3,36 : 22,4 = 0,15 (mol)
theo (1) nMg = nH2 = 0,15 (mol)
➞ mMg = 0,15 ✖ 24 = 3,6 (g)
➞ %mMg = (3,6 : 5)✖100 = 72%
➞ %mCu = 100% - 72% = 28%
c. theo (1) nHCl = 2nH2 = 2✖0,15 = 0,3 (mol)
mHCl = 0,3✖36,5 = 10,95(g)
➜mddHCl = (10,95✖100):14,6 = 75(g)
d. dung dịch Y : MgCl2
mdd(spư)= 3,6+75-0,3 = 78,3(g)
theo (1) nMgCl2 = nH2 = 0,15(mol)
mMgCl2 = 0,15✖95 = 14,25(g)
C%MgCl2 = (14,25 : 78,3)✖100 = 18,199%
Đúng 0
Bình luận (0)
Câu 4: Cho m gam Fe vào 500 ml dung dịch HCl, phản ứng xảy ra vừa đủ thu được 3,36 lit khí H2 (Đktc). Tính m g Fe? Và CM của HCl
Câu 5: cho 8,3 gam hỗn hợp kim loại Fe, Al tác dụng với 500ml dung dịch HCl vừa đủ thu được 5,6 lit khí Hidro (Đktc). Xác định thành phần % mỗi kim loại trong hỗn hợp ban đầu
\(4.\)
\(n_{H_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(0.15.....0.3....................0.15\)
\(m_{Fe}=0.15\cdot56=8.4\left(g\right)\)
\(C_{M_{HCl}}=\dfrac{0.3}{0.5}=0.6\left(M\right)\)
\(5.\)
\(Đặt:n_{Fe}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(m_{hh}=56a+27b=8.3\left(g\right)\left(1\right)\)
\(n_{H_2}=\dfrac{5.6}{22.4}=0.25\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(\Rightarrow a+1.5b=0.25\left(2\right)\)
\(\left(1\right),\left(2\right):a=b=0.1\)
\(\%Fe=\dfrac{5.6}{8.3}\cdot100\%=67.47\%\)
\(\%Al=32.53\%\)
Đúng 2
Bình luận (1)
Bài 1: Cho 5,1 gam hỗn hợp gồm Mg và Al tác dụng với 200 ml dung dịch HCI (vừa đủ) sinh ra 5,6 lít khí H2 (đktc).
a) Viết PTHH.
b) Tính nồng độ mol dung dịch HCl và khối lượng của từng kim loại trong hỗn hợp.
a) Mg + 2HCl -> MgCl2 + H2
Al + 3HCl -> AlCl3 + 3/2H2
b) Gọi a, b lần lượt là số mol Mg, Al.
nH2 = 5,6/22,4 = 0,25 (mol)
Mg + 2HCl -> MgCl2 + H2
a 2a a a
Al + 3HCl -> AlCl3 + 3/2H2
b 3b b 3/2b
Ta có hệ pt:
mhh = 24a + 27b = 5,1 (g)
nH2 = a + 3/2b = 0,25 (mol)
=> a = 0,1 (mol)
b = 0,1 (mol)
200 ml = 0,2 l
nHCl = 2a + 3b = 0,2 + 0,3 = 0,5 (mol)
=> CM ddHCl = 0,5/0,2 = 2,5 (M)
%mMg = 24a/5,1*100% = 2,4/5,1*100% = 47,06%
%mAl = 100%-47,06% = 52,94%
Đúng 1
Bình luận (0)