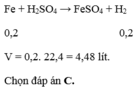Cho 11,2 gam Fe tác dụng với dung dịch H2SO4 loãng có chứa 12,25 gam H2SO4 . Tính thể tích khí H2 thu đc ở đktc.

Những câu hỏi liên quan
Cho 22,4g Fe tác dụng với dung dịch loãng có chứa 24,5 g H2SO4 sau phản ứng hãy cho biết: a, Chất nào dư sau phản ứng và dư bao nhiêu gam? b, Tính thể tích H2 thu được ở đktc. Có đc ghi fe +h2so4--->fe2(so4)3 +h2 đc ko ạ
`Fe + H_2 SO_4 -> FeSO_4 + H_2`
`0,25` `0,25` `0,25` `(mol)`
`a)n_[Fe]=[22,4]/56=0,4(mol)`
`n_[H_2 SO_4]=[24,5]/98=0,25(mol)`
Có: `[0,4]/1 > [0,25]/1=>Fe` hết, `H_2 SO_4`
`=>m_[Fe(dư)]=(0,4-0,25).56=8,4(g)`
`b)V_[H_2]=0,25.22,4=5,6(l)`
Ko được ghi `Fe+H_2 SO_4->Fe_2 (SO_4)_3+H_2` vì đây là `H_2 SO_4` loãng
Đúng 4
Bình luận (2)
Cho 11,2 gam sắt tác dung với dung dịch loãng có chứa 49gam axit sunfuaric H2SO4. Tính thể tích khí hiđro thu được (Ở đktc)
`Fe + H_2 SO_4 -> FeSO_4 + H_2↑`
`0,2` `0,2` `(mol)`
`n_[Fe] = [ 11,2 ] / 56 = 0,2 (mol)`
`n_[H_2 SO_4] = 49 / 98 = 0,5 (mol)`
Ta có: `[ 0,2 ] / 1 < [ 0,5 ] / 1`
`=> Fe` hết, `H_2 SO_4` dư
`-> V_[H_2] = 0,2 . 22,4 = 4,48 (l)`
Đúng 2
Bình luận (0)
Cho 22,4 gam sắt tác dụng với dung dịch loãng có chứa 24,5 gam axit H2SO4 . a. Tính thể tích khí H2 thu được ở (đktc). b. Chất nào dư sau phản ứng và dư bao nhiêu gam?
\(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right);n_{H_2SO_4}=\dfrac{24,5}{98}=0,25\left(mol\right)\\ PTHH:Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ Vì:\dfrac{0,4}{1}>\dfrac{0,25}{1}\Rightarrow Fe.dư\\ n_{H_2}=n_{Fe\left(p.ứ\right)}=n_{H_2SO_4}=0,25\left(mol\right)\\ a,V_{H_2\left(đktc\right)}=0,25.22,4=5,6\left(l\right)\\ b,n_{Fe\left(dư\right)}=0,4-0,25=0,15\left(g\right)\\ m_{Fe\left(dư\right)}=0,14.56=8,4\left(g\right)\)
Đúng 2
Bình luận (0)
cho 11,2 gam sắt tác dụng với dung dịch loãng có chứa 24,5 gam axit sunfuric H2SO4 a, viết phương trình hóa học xảy ra
b, tính thể tích khid hidro thu đc ( ở đktc)
c, dung dịch sau phản ứng có những chất nào . tính nồng độ % của các dung dịch sau phản ứng , biết dung dịch sau phản ứng có khối lượng là 190 gam
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\\
n_{H_2SO_4}=\dfrac{24,5}{98}=0,25\left(mol\right)\\
pthh:Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
\(LTL:\dfrac{0,2}{1}< \dfrac{0,25}{1}\)
=> H2SO4 dư
\(n_{H_2}=n_{H_2SO_4\left(p\text{ư}\right)}=n_{Fe}=0,2\left(mol\right)\\
V_{H_2}=0,2.22,4=4,48l\\
m_{H_2SO_4\left(d\right)}=\left(0,25-0,2\right).98=4,9g\)
Đúng 1
Bình luận (0)
Cho 11,2 gam Fe và 6,4 gam Cu tác dụng với dung dịch
H
2
S
O
4
loãng, dư. Sau phản ứng thu được V lít khí
H
2
(đktc). Giá trị của V là A. 2,24 lít. B. 3,36 lít. C. 4,48 lít. D. 6,72 lít.
Đọc tiếp
Cho 11,2 gam Fe và 6,4 gam Cu tác dụng với dung dịch H 2 S O 4 loãng, dư. Sau phản ứng thu được V lít khí H 2 (đktc). Giá trị của V là
A. 2,24 lít.
B. 3,36 lít.
C. 4,48 lít.
D. 6,72 lít.
Cho 11,2 gam Fe và 6,4 gam Cu tác dụng với dung dịch H2SO4 loãng, dư. Sau phản ứng thu được V lít khí H2 (đktc). Giá trị của V là : A. 2,24 lít B. 3,36 lít C. 4,48 lít D. 6,72 lít
Đọc tiếp
Cho 11,2 gam Fe và 6,4 gam Cu tác dụng với dung dịch H2SO4 loãng, dư. Sau phản ứng thu được V lít khí H2 (đktc). Giá trị của V là :
A. 2,24 lít
B. 3,36 lít
C. 4,48 lít
D. 6,72 lít
Cho 11,2g Fe tác dụng với dung dịch loãng có chứa 24,5 g H2SO4 sau phản ứng hãy cho biết: a, Chất nào dư sau phản ứng và dư bao nhiêu gam? b, Tính thể tích H2 thu được ở đktc.
nFe=11,2/56=0,2 mol
nH2SO4=24,5/98=0,25
PTPƯ: Fe + H2SO4 ---> FeSO4 + H2
0,2 mol ----> 0,2 mol --------------------> 0,2 mol
Ta có Fe:H2SO4=0,2/1<0,25/1 (nên H2SO4 dư)
a, mH2SO4=(0,25-0,2).98=4,9 g
b, VH2=0,2.22,4=4,48 l
Đúng 1
Bình luận (0)
Cho 22,4g Fe tác dụng với dung dịch loãng có chứa 24,5 g H2SO4 sau phản ứng hãy cho biết: a, Chất nào dư sau phản ứng và dư bao nhiêu gam? b, Tính thể tích H2 thu được ở đktc.
PTHH: \(Fe+H_2SO_{4\left(l\right)}\rightarrow FeSO_4+H_2\uparrow\)
Ta có: \(\left\{{}\begin{matrix}n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\\n_{H_2SO_4}=\dfrac{24,5}{98}=0,25\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Sắt còn dư, Axit p/ứ hết
\(\Rightarrow\left\{{}\begin{matrix}n_{H_2}=0,25\left(mol\right)\\n_{Fe\left(dư\right)}=0,15\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=0,25\cdot22,4=5,6\left(l\right)\\m_{Fe\left(dư\right)}=0,15\cdot56=8,4\left(g\right)\end{matrix}\right.\)
Đúng 3
Bình luận (0)
5.Cho 0,83 gam hỗn hợp gồm Al và Fe tác dụng với dung dịch H2SO4 loãng dư
theo phản ứng:
Al + H2SO4 → Al2( SO4)3 + H2 ; Fe + H2SO4 → FeSO4 + H2 ; sau phản
ứng thu được 0,56 lít khí ở đktc. Tính khối lượng mỗi kim loại có trong hỗn
hợp ban đầu?
Gọi x, y lần lượt là số mol Al, Fe
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ n_{H_2}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\\ Tacó:\left\{{}\begin{matrix}27x+56y=0,83\\1,5x+y=0,025\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}x=0,01\\y=0,01\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}m_{Al}=0,27\left(g\right)\\m_{Fe}=0,56\left(g\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)