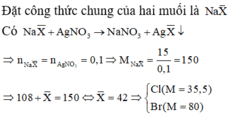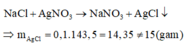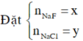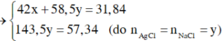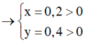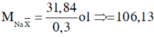Cho 0,03 mol hỗn hợp NaX và NaY ( X, Y là hai halogen thuộc chu kì kế tiếp – đều tạo kết tủa với AgNO3) tác dụng với lượng dư dung dịch AgNO3 thu được 4,75 gam kết tủa. Công thức hai muối trên là
A. NaBr, NaI
B. NaF, NaCl
C. NaCl, NaBr
D. NaF, NaCl hoặc NaBr, NaI