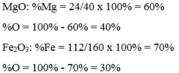Tính thành phần phần trăm theo khối lượng các nguyên tố trong hợp chất sau Mg(HCO3)2

Những câu hỏi liên quan
Tính thành phần phần trăm theo khối lượng các nguyên tố trong hợp chất sau Mg(HCO3)2
\(\%_{Mg}=\dfrac{24}{146}.100\%=16,4\%\)
\(\%_H=\dfrac{1.2}{146}.100\%=1,4\%\)
\(\%_C=\dfrac{12.2}{146}.100\%=16,4\%\)
\(\%_O=100\%-16,4\%-1,4\%-16,4\%=65,8\%\)
Đúng 1
Bình luận (0)
Tính thành phần trăm theo khối lượng của các nguyên tố trong các hợp chất sau: Ca(NO3)2
\(\%m_{Ca}=\dfrac{40}{164}.100=24,39\left(\%\right)\\ \%m_N=\dfrac{28}{164}.100=17,07\left(\%\right)\\ \%m_O=\dfrac{48.2}{164}.100=58,54\left(\%\right)\)
Đúng 2
Bình luận (0)
$M_{Ca(NO_3)_2} = 164$
$\%Ca = \dfrac{40}{164}.100\% = 24,39\%$
$\%N = \dfrac{14.2}{164}.100\% = 17,07\%$
$\%O = 100% -24,39\% -17,07\% = 58,54%%
Đúng 2
Bình luận (0)
BÀI TẬP TỰ LUẬN CHỦ ĐỀ 6Bài 1: Hãy tính thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chấta) CaCO3b) Fe2O3Bài 2: Tìm CTHH của các hợp chất sau, biết thành phần phần trăm các nguyên tố là:a) 52,174%C; 13,043% H và 34,783%O. Biết khối lượng mol của hợp chất A là 46 g/molb) 28,7%Mg, 14,2%C, còn lại là oxygen. Biết khối lượng mol của hợp chất A là 84 g/molBài 3: Hòa tan hoàn toàn 14 gam kim loại Fe, trong dung dịch HCl dư. Phản ứng hóa học được biểu diễn theo sơ đồ...
Đọc tiếp
BÀI TẬP TỰ LUẬN CHỦ ĐỀ 6 Bài 1: Hãy tính thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất a) CaCO3 b) Fe2O3 Bài 2: Tìm CTHH của các hợp chất sau, biết thành phần phần trăm các nguyên tố là: a) 52,174%C; 13,043% H và 34,783%O. Biết khối lượng mol của hợp chất A là 46 g/mol b) 28,7%Mg, 14,2%C, còn lại là oxygen. Biết khối lượng mol của hợp chất A là 84 g/mol Bài 3: Hòa tan hoàn toàn 14 gam kim loại Fe, trong dung dịch HCl dư. Phản ứng hóa học được biểu diễn theo sơ đồ sau: Fe + HCl → FeCl2 + H2 a) Hãy lập phương trình hóa học của phản ứng. b) Tính thể tích (ở đkc) của khí H2 sinh ra. c) Tính khối lượng acid HCl đã tham gia phản ứng. Bài 4: Cho sơ đồ phản ứng: CaCO3 + HCl → CaCl2 + CO2 + H2O. a) Nếu có 9,916 lít khí CO2 (đkc) tạo thành thì cần dùng bao nhiêu gam CaCO3, bao nhiêu gam HCl tham gia phản ứng? b) Nếu có 20 gam CaCO3 tham gia phản ứng, hãy tính khối lượng HCl cần dùng và thể tích khí CO2 sinh ra ở đkc? Bài 5: Cho sơ đồ : Zn + HCl → ZnCl2 + H2. Nếu có 16,25 g Zn tham gia phản ứng, hãy tính: a) Tính khối lượng của HCl? b) Tính thể tích của H2 ở đkc c) Tính khối lượng của ZnCl2 (bằng hai cách). |
tính thành phần phần trăm(theo khối lượng) của các nguyên tố hóa học có trong hợp chất sau;KMnO4
\(M_{KMnO_4}=158(g/mol)\\ \%_{K}=\dfrac{39}{158}.100\%=24,68\%\\ \%_{Mn}=\dfrac{55}{158}.100\%=34,81\%\\ \%_O=100\%-24,68\%-34,81\%=40,51\%\)
Đúng 1
Bình luận (0)
Tính thành phần phần trăm (theo khối lượng) các nguyên tố hóa học có trong các hợp chất sau: MgO và F e 2 O 3 .
Tính thành phần phần trăm theo khối lượng các nguyên tố hóa học có trong hợp chất sau: CaCO3,H2SO4,Fe2O3
\(CaCO_3\\ \%m_{Ca}=\dfrac{40}{40+12+3.16}.100=40\%\\ \%m_C=\dfrac{12}{40+12+16.3}.100=12\%\\ \Rightarrow\%m_O=100\%-\left(40\%+12\%\right)=48\%\\ H_2SO_4\\ \%m_H=\dfrac{2.1}{2.1+32+4.16}.100\approx2,041\%\\ \%m_S=\dfrac{32}{2.1+32+4.16}.100\approx32,653\%\\ \%m_O=\dfrac{4.16}{2.1+32+4.16}.100\approx65,306\%\\ Fe_2O_3\\ \%m_{Fe}=\dfrac{56.2}{56.2+16.3}.100=70\%\\ \Rightarrow\%m_O=100\%-70\%=30\%\)
Đúng 4
Bình luận (0)
CaCO3
\(\%M_{\dfrac{Ca}{CaCO_3}}=\dfrac{40}{100}.100\%=40\%\)
\(\%M_{\dfrac{C}{CaCO_3}}=\dfrac{12}{100}.100\%=12\%\)
\(\%M_{\dfrac{O}{CaCO_3}}=100\%-\left(40\%+12\%\right)=48\%\)
H2SO4
\(\%M_{\dfrac{H_2}{H_2SO_4}}=\dfrac{2}{98}.100\%=2,04\%\)
\(\%M_{\dfrac{S}{H_2SO_4}}=\dfrac{32}{98}.100\%=32,65\%\)
\(\%M_{\dfrac{O}{H_2SO_4}}=100\%-\left(2,04\%+32,65\%\right)=65,31\%\)
Fe2O3
\(\%M_{\dfrac{Fe}{Fe_2O_3}}=\dfrac{112}{160}.100\%=70\%\)
\(\%M_{\dfrac{O}{Fe_2O_3}}=100\%-70\%=30\%\)
Đúng 1
Bình luận (1)
Tính thành phần,phần trăm theo khối lượng các nguyên tố hóa học có trong những hợp chất sau:
a.CaO
b.MgCO3
c.NaOH
Xem chi tiết
\(CaO:\%^MCa=\dfrac{40}{40+16}\cdot100\%=71,43\%\\ \%^MO=100\%-71,43\%=28,57\%\)
\(MgCO_3:\%^MMg=\dfrac{24}{24+12+16\cdot3}\cdot100\%=28,57\%\\ \%^MC=\dfrac{12}{24+12+16\cdot3}\cdot100\%=14,29\%\\ \%^MO=100\%-28,57\%-14,29\%=57,14\%\)
\(NaOH:\%^MNa=\dfrac{23}{23+16+1}\cdot100\%=57,5\%\\ \%^MO=\dfrac{16}{23+16+1}\cdot100\%=40\%\\ \%^MH=100\%-57,5\%-40\%=2,5\%\)
Đúng 3
Bình luận (0)
tính khối lượng phần trăm của các nguyên tố trong các hợp chất sau:
+Tính Mg, O trong hợp chất MgO
+Tính FE trong FE2O3
`@` `\text {MgO}`
\(\text{PTK = 24 + 16 = 40 < amu>}\)
\(\%\text{O}=\dfrac{16\cdot100}{40}=40\%\)
Vậy, khối lượng `%` của `\text {O}` trong `\text {MgO}` là `40%`
`@` `\text {Fe}_2 \text {O}_3`
\(\text{PTK = }56\cdot2+16\cdot3=160\text{ }< \text{amu}\text{ }>\)
\(\%\text{Fe}=\dfrac{56\cdot2\cdot100}{160}=70\%\)
Vậy, khối lượng `%` của `\text {Fe}` trong `\text {Fe}_2 \text {O}_3` là `70%`
Đúng 1
Bình luận (7)
a, Tính thành phần phần trăm theo khối lượng của nguyên tố Canxi và Oxi trong hợp chứa Ca(HCO3)2?
b, 1 hợp chất khi X chứa 27,27% và 72,73℅ Oxi về khối lượng. Tỉ khối của X đối với khí Oxi là 1,375. Tìm công thức của X
b,
Ta có: dX/O2=1,375
=>Mx =1,375.32
=44(g/mol)
Ta lại có:
12.x/27,27=16.y/72,73=44/100
=>x=27,27.44/12.100=1
=> y=72,73.44/16.100=2
Vậy CTHH: CO2
Đúng 2
Bình luận (0)