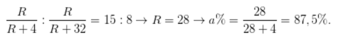. Nguyên tố R có cấu hình e lớp ngoài cùng là ns1. Trong công thức oxit cao nhất của R có 74,19% khối lượng R.
a. Xác định tên kim loại R.
b. Tính giá trị của V trong các trường hợp sau:
Trường hợp 1: Cho 4,6 g kim loại R tác dụng hoàn toàn với H2O thu được V lit khí (đktc).
Trường hợp 2: Cho 4,6 g kim loại R tác dụng vừa đủ với V lit dung dịch HCl 1M.
c. Viết phương trình phản ứng có ghi sự di chuyển e để tạo hợp chất oxit cao nhất của R.