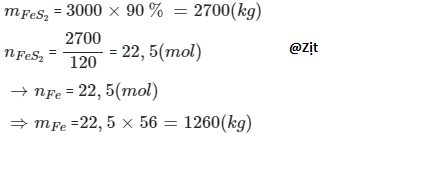1.Tính khối lượng Cu CÓ TRONG 48g CuSO4?
2.Tính lượng sắt có trong 60 tấn quặng sắt chứa 80% Fe2O3

Những câu hỏi liên quan
Cần bao nhiêu tấn quặng hematit chứa 85% Fe2O3 để có một lượng sắt bằng lượng sắt có trong 2,4 tấn muối chứa trong 80% muối sắt (II) sunphat
A là một loại quặng sắt chứa 60% Fe2O3; B là loại quặng sắt khác chứa 69,6% Fe3O4. Hỏi trong một tấn quặng A hoặc B có chứa bao nhiêu kg sắt? 2. Trộn quặng A với quặng B theo tỉ lệ khối lượng mA:mB = 2:5 ta được quặng C có bao nhiêu kg sắt
Có 2 quặng sắt: quặng 1 chứa 70% sắt, quặng 2 chứa 40% sắt. Người ta trộn một lượng quặng loại 1 với một lượng quặng loại 2 thì được hỗn hợp quặng chứa 60% sắt. Nếu lấy giảm đi 8 tấn quặng loại 1 và giảm đi 2 tấn khối lượng loại 2 thì được hỗn hợp quặng chứa 58% sắt. Tính khối lượng mỗi loại quặng đem trộn lúc đầu
Gọi khối lượng mỗi quặng là a và b (tấn)
ta có: \(\frac{70a+40b}{a+b}=60\Leftrightarrow\frac{30a}{a+b}+40=60\Leftrightarrow30a=20\left(a+b\right)\Leftrightarrow10a=20b\Leftrightarrow a=2b\)
lại có\(\frac{70\left(a-8\right)+40\left(b-2\right)}{\left(a-8\right)+\left(b-2\right)}=58\Leftrightarrow\frac{30\left(a-8\right)}{a-8+b-2}+40=58\Leftrightarrow30\left(a-8\right)=18\left(a+b-10\right)\)
\(\Leftrightarrow30a-240=18a+18b-180\Leftrightarrow12a-18b=60\)
thay a=2b vào phương trình trên ta có
\(12\times2b-18b=60\Leftrightarrow24b-18b=60\Leftrightarrow6b=60\Leftrightarrow b=10\Rightarrow a=20\)
Vậy khối lượng quặng 1 là 20 tấn, khối lượng quặng 2 là 10 tấn
Đúng 0
Bình luận (0)
Bài 2. Hãy tính:
a) Khối lượng sắt có trong 10 tấn quặng hematit chứa 60% Fe2O3 (còn lại là tạp chất không chứa sắt).
b) Tổng số nguyên tử của các nguyên tố có trong 36 gam H2O
a) mFe2O3= 60%.10=6(tấn)
=> mFe= (112/160).6= 4,2(tấn)
b) nH2O=36/18=2(mol)
=> Số mol nguyên tử trong 2 mol H2O là: 2.2+ 2.1=6(mol)
Tổng số nguyên tử của các nguyên tố trong 36 gam H2O là:
6.6.1023=3,6.1024 (nguyên tử)
Chúc em học tốt!
Đúng 2
Bình luận (1)
Bài 3. a) Tính khối lượng sắt có trong 100 tấn quặng manhetit chứa 69,6% Fe3O4. b) Tính tổng số nguyên tử của các nguyên tố có trong 4,8 gam CuSO4
a)
$m_{Fe_3O_4} = 100.1000.69,6\% = 69600(kg)$
$n_{Fe_3O_4} = 69600 : 232 = 300(kmol)$
$m_{Fe} = 300.3.56 = 50400(kg)$
b)
$n_{CuSO_4} = \dfrac{4,8}{160} = 0,03(mol)$
Số nguyên tử Cu = Số nguyên tử S = 0,03.6.1023 = 0,18.1023 nguyên tử
Số nguyên tử O = 0,03.4.6.1023 = 0,72.1023 nguyên tử
Đúng 1
Bình luận (0)
a) Khối lượng Fe3O4 có trong quặng là: mFe3O4 = 100* 69,6%= 69,6 (tấn)
-> nFe3O4 = m/M = 69,6 / 232= 0,3 (mol)
-> nFe = 3 nFe3O4 = 0,3*3 = 0,9 (mol)
-> mFe = n*M = 0,9* 56= 50,4 (tấn)
vậy trong 100 tấn quặng manhetit chứa 50,4 tấn Fe
Đúng 1
Bình luận (0)
Tính khối lượng sắt có trong 100 tấn quặng hematit chứa 60% Fe2O3
100 tấn = 100 000kg
khối lượng Fe2O3:
100 000x 60%=60 000kg
Khối lượng Fe:
60 000 : (2+3) x 2 =24 000kg= 24 tấn
Đúng 0
Bình luận (1)
100 tấn=100000kg
mFe2O3=100000.60/100=60000 kg
%Fe trong Fe2O3=(56.2/56.2+16.3).100%=70%
mFe= 60000.70/100=42000kg=42 tấn
Đúng 0
Bình luận (4)
tính khối lượng quặng sắt có trong 3 tấn quặng chứa 90% FeS2
Khối lượng quặng hemantit chứa 60% F e 2 O 3 cần thiết để sản xuất được 1 tấn gang chứa 95% sắt là? Biết hiệu suất của quá trình là 80%.
A. 2,5 tấn
B. 2,2 tấn
C. 2,8 tấn
D. 2,9 tấn
Khử một lượng quặng hemantit chứa 80% (
Fe
2
O
3
) thu được 1,68 tấn sắt, khối lượng quặng cần lấy là: A. 2,4 tấn B. 2,6 tấn C. 2,8 tấn D. 3,0 tấn
Đọc tiếp
Khử một lượng quặng hemantit chứa 80% ( Fe 2 O 3 ) thu được 1,68 tấn sắt, khối lượng quặng cần lấy là:
A. 2,4 tấn
B. 2,6 tấn
C. 2,8 tấn
D. 3,0 tấn

→ m F e 2 O 3 = ( 1 , 68 . 160 ) : 112 = 2 , 4 t ấ n .
![]()
Đúng 0
Bình luận (0)