Muối Sunfat có dạng RSO4 có khối lượng phân tử là 160 đvC. Hỏi R là kim loại nào?
muối cacbonat có dạng RCO3 có khối lượng phân tử là 100 đvC Hỏi R là kim loại nào ❓
Khối lượng phân tử của RCO3 = MR + MC + 3. MO= MR + 12 + 3.16=100
=> MR = 40
Vậy R là Canxi (Ca)
1.Oxit cao nhất của 1 nguyên tố R có dạng R2Ox. Phân tử khối của oxit là 102 đvC. Xác định R.
2. Cho biết phân tử khối của một oxit kim loại là 160, phần trăm khối lượng của kim loại trong
oxit là 70%. Lập công thức oxit đó.
1)
PTKR2Ox = 2.NTKR + 16x = 102 (đvC)
| x | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| NTKR | 43(Loại) | 35(Loại) | 27(Al) | 19(Loại) | 11(Loại) | 3(Loại) | Loại | Loại |
=> R là Al
2)
CTHH: RxOy
\(\%R=\dfrac{x.NTK_R}{160}.100\%=70\%\)
=> \(NTK_R=\dfrac{112}{x}\left(đvC\right)\)
Chỉ có x = 2 thỏa mãn \(NTK_R=\dfrac{112}{2}=56\left(đvC\right)\)
=> R là Fe
PTKFe2Oy = 160 (đvC)
=> y = 3
CTHH: Fe2O3
Muối Sunfat có dạng RSO4 có khối luong phân tu là 160 đvC. Hỏi R là kim loại nào?
Help meeeeeeee
Ta có:
mR = mRSO4 - mSO4
mR = 160 - ( 32 + 16.4)
mR = 64
Vậy kim loại R là đồng (Cu)
a) phân tử khôi của đồng oxit và đồng sunfat có tỉ lệ 1/2 . biết khối lượng phân tử CuSO4 là 160 đvC . công thức phân tử đồng oxit là:
b) phân tích một khối lượng hợp chất M , người ta nhận thấy thành phần khối lượng của nó có 50% là lưu huỳnh và 50% là oxi . công thức của hợp chất M có thể là:
Phân tử khối của Đồng ôxit và Đồng sunfat có tỉ lệ 1/2
Mà phân tử khối của đồng sunfat (CUSO4) là 160 đvC
=> Phân tử khối của đồng oxit là :
160 * 1/2 = 80 (đvC)
Do đồng oxit gồm Cu và O nêncông thức hóa học của đồng oxit có dạng CuxOy
Ta có :
PTKđồng oxit = NTKCu * x + NTKO * y
=> 80 đvC = 64 * x + 16 * y
=> x < 2 vì nếu x = 2 thì 64 * 2 > 80
=> x = 1 , khi đó :
y = ( 80 - 64*1 ) : 16 = 1
Vậy công thức hóa học của đồng oxit là CuO
b) Gọi công thức của oxit là SxOy
x : y = nS : nO =
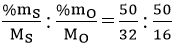
= 1,5625 : 3,125 = 1 : 2
Vậy công thức đơn giản của hợp chất M là: SO2
Một kim loại M tạo muối sunfat có dạng M2(SO4)3 . PTK của M2(SO4)3 là 342 (đvc).Tính PTK của muối nitrat của nó.
Ta có: \(M_M=\dfrac{342-96\cdot3}{2}=27\)
\(\Rightarrow M_{M\left(NO_3\right)_3}=27+62\cdot3=213\left(đvC\right)\)
Một muối cacbonat có phân tử khối là 106 đvC. Tìm công thức hóa học của muối (Biết kim loại trong muối cacbonat có ht là 1)
Vì là kim loại hóa trị I nên có CT là: A2CO3. Muối có M =2A+60=160 nên suy ra A =23 là Natri
Kim loại R có hóa trị 3. Hợp chất tạo bởi R và nhóm SO4 có phân tử khối là 400 đvC. Hãy xác định nguyên tử khối của R
Đặt CTPT của chất là Rx(SO4)y (x, y nguyên dương)
Theo quy tắc hóa trị, ta có: x.III = y.II
=> \(\dfrac{x}{y}=\dfrac{2}{3}\)
=> CTHH của chất lả R2(SO4)3
=> 2.R + (32 + 16.4).3 = 400
=> R = 56 (đvC)
áp dụng quy tắc hóa trị thì công thức hóa học đơn giản là
R2(SO4)3
theo đề bài ta có
PTK[R2(SO4)3]=400(dvC)
=>PTK(R2)=400-(32+16*4)*3=112(dvC)
=>NTK(R)=112:2=56(dvC)
=> R là sắt (Fe)
Khi hòa tan cùng một lượng kim loại R vào dung dịch HNO3 loãng và vào dung dịch H2SO4 loãng thì thu được khí NO và khí H2 có thể tích bằng nhau (đo ở cùng điều kiện). Biết rằng muối nitrat thu được có khối lượng bằng 159,21% khối lượng muối sunfat. Kim loại R là
A. Zn
B. Al
C. Fe
D. Mg
a) trong một tập hợp các phân tử đồng sunfat (CuSO4) có khối lượng 160000 đvC . cho biết tập hợp đó có bn nguyên tử mỗi loại.
b) phhân tử canxi cacbon có phân tử khối là 100 đvC , trong đó nguyên tố canxi chiếm 40% khối lượng , nguyên tố cacbon chiếm 12% khối lượng . khối lượng còn lại là oxi . Công thức phân tử của hợp chất canxi cacbon là
a) Đề bạn xem lại xem có sai xót ở đâu nhé chứ mình thấy nó cho số to quá.
b)\(CaCO_3\)