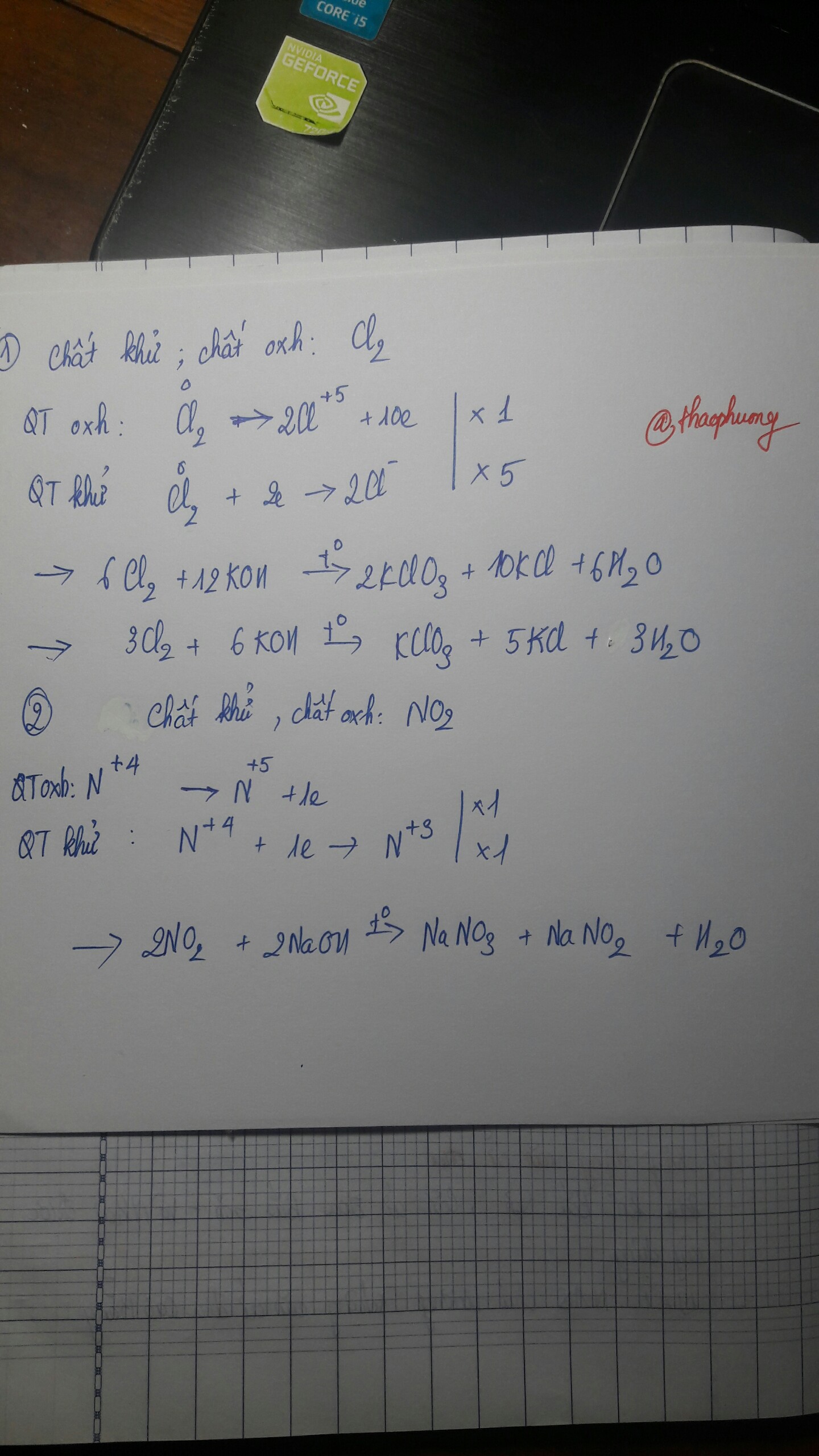Giúp mk vs
Đề : xác định chất khử chất oxi hoá và ghi rõ quá trình khử và quá trình oxi hoá

Những câu hỏi liên quan
Giúp mk vs
Đề là : xác định chất khử chất oxi hoá ghi rõ quá trình khử và quá trình oxi hoá
1) (5x-2y)Fe + (18x-6y)HNO3 --> (5x-2y)Fe(NO3)3 + 3NxOy + (9x-3y)H2O
Chất khử: Fe
Chất oxh: HNO3
| QT oxh | Fe0 -3e --> Fe+3 | x(5x-2y) |
| QT khử | xN+5 + (5x-2y)--> \(N_x^{+\dfrac{2y}{x}}\) | x3 |
2) 2M + 2nH2SO4 --> M2(SO4)n + nSO2 + 2nH2O
Chất khử: M
Chất oxh: H2SO4
| QT oxh | 2M0 -2ne --> M2+n | x1 |
| QT khử | S+6 + 2e --> S+4 | xn |
Đúng 2
Bình luận (0)
Giúp mk vs
Đề là xác định chất khử chất oxi hoá ghi rõ quá trình khử và quá trình oxi hoá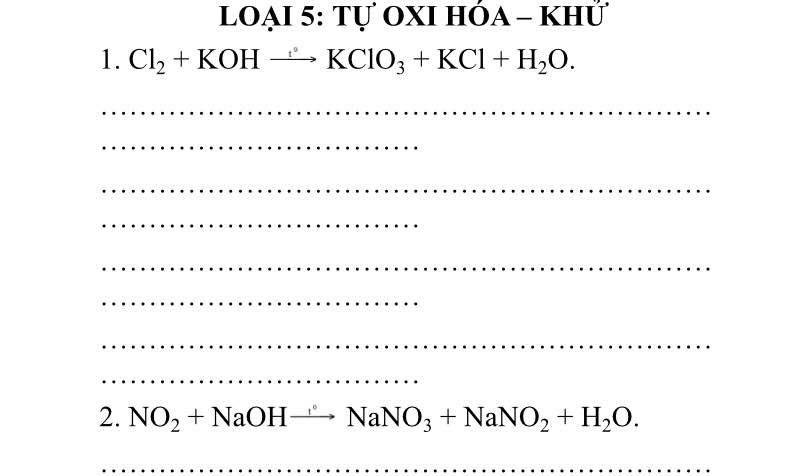
3Cl2 + 6KOH --> KClO3 + 5KCl + 3H2O
Chất oxi hóa: Cl2
Chất khử: Cl2
| QT oxh | Cl0 -5e --> Cl+5 | x1 |
| QT khử | Cl0 + 1e --> Cl-1 | x5 |
2NO2 + 2NaOH --> NaNO3 + NaNO2 + H2O
Chất oxh: NO2
Chất khử: NO2
| QT oxh | N+4 -1e --> N+5 | x1 |
| QT khử | N+4 +1e --> N+3 | x1 |
Đúng 0
Bình luận (0)
Cân bằng PTHH của các phản ứng oxi hoá- khử sau bằng phương pháp thăng bằng electron (xác định chất khử, chất oxi hoá, quá trình khử, quá trình oxi hóa).
A
l
+
H
N
O
3
→
A
l
N
O
3
3
+
N
O
+
N
H
4...
Đọc tiếp
Cân bằng PTHH của các phản ứng oxi hoá- khử sau bằng phương pháp thăng bằng electron (xác định chất khử, chất oxi hoá, quá trình khử, quá trình oxi hóa).
A l + H N O 3 → A l N O 3 3 + N O + N H 4 N O 3 + H 2 O
Cân bằng PTHH của các phản ứng oxi hoá- khử sau bằng phương pháp thăng bằng electron (xác định chất khử, chất oxi hoá, quá trình khử, quá trình oxi hóa).
C
u
+
H
2
S
O
4
đ
,
n
→
C
u
S
O
4
+
S
O...
Đọc tiếp
Cân bằng PTHH của các phản ứng oxi hoá- khử sau bằng phương pháp thăng bằng electron (xác định chất khử, chất oxi hoá, quá trình khử, quá trình oxi hóa).
C u + H 2 S O 4 đ , n → C u S O 4 + S O 2 + H 2 O
B 1 . Xác định số oxi hoá các nguyên tố(thay đổi SOH). Tìm chất khử và chất oxi hóa.B 2 . Viết các quá trình khử và quá trình oxi hóa, cân bằng mỗi quá trình.B 3 . Xác định hệ số cân bằng sao cho: tổng số e nhường tổng số e nhậnB 4 . Đưa hệ số cân bằng vào phương trình, tính ra hệ số các chất khác trong phương trình(kiểm tra lại theo trật tự: kim loại – phi kim – hidro – oxi)Mg + H2SO 4 → MgSO4 + H2S + H2O.
Đọc tiếp
B 1 . Xác định số oxi hoá các nguyên tố(thay đổi SOH). Tìm chất khử và chất oxi hóa.
B 2 . Viết các quá trình khử và quá trình oxi hóa, cân bằng mỗi quá trình.
B 3 . Xác định hệ số cân bằng sao cho: tổng số e nhường = tổng số e nhận
B 4 . Đưa hệ số cân bằng vào phương trình, tính ra hệ số các chất khác trong phương trình(kiểm tra lại theo trật tự: kim loại – phi kim – hidro – oxi)
Mg + H2SO 4 → MgSO4 + H2S + H2O.
\(B1.\overset{0}{Mg}+H_2\overset{+6}{S}O_4\rightarrow\overset{2+}{Mg}SO_4+H_2\overset{2-}{S}+H_2O\\ B2+B3.QToxh:Mg\rightarrow Mg^{2+}+2e|\times4\\ QTkhử:S^{+6}+8e\rightarrow S^{2-}|\times1\\ B4.4Mg+5H_2SO_4\rightarrow4MgSO_4+H_2S+4H_2O\)
Đúng 3
Bình luận (3)
B 1 . Xác định số oxi hoá các nguyên tố(thay đổi SOH). Tìm chất khử và chất oxi hóa.B 2 . Viết các quá trình khử và quá trình oxi hóa, cân bằng mỗi quá trình.B 3 . Xác định hệ số cân bằng sao cho: tổng số e nhường tổng số e nhậnB 4 . Đưa hệ số cân bằng vào phương trình, tính ra hệ số các chất khác trong phương trình(kiểm tra lại theo trật tự: kim loại – phi kim – hidro – oxi)6. Al + HNO3 → Al(NO3)3+ N2O + H2O.7. FeSO4+ H2SO4+ KMnO4 → Fe2(SO4)3+ MnSO4+ K2SO4 + H2O.8. KMnO4+ HCl → KCl + MnCl2...
Đọc tiếp
B 1 . Xác định số oxi hoá các nguyên tố(thay đổi SOH). Tìm chất khử và chất oxi hóa.
B 2 . Viết các quá trình khử và quá trình oxi hóa, cân bằng mỗi quá trình.
B 3 . Xác định hệ số cân bằng sao cho: tổng số e nhường = tổng số e nhận
B 4 . Đưa hệ số cân bằng vào phương trình, tính ra hệ số các chất khác trong phương trình(kiểm tra lại theo trật tự: kim loại – phi kim – hidro – oxi)
6. Al + HNO3 → Al(NO3)3+ N2O + H2O.
7. FeSO4+ H2SO4+ KMnO4 → Fe2(SO4)3+ MnSO4+ K2SO4 + H2O.
8. KMnO4+ HCl → KCl + MnCl2 + Cl2+ H2O.
9. K2Cr2O7+ HCl → KCl + CrCl3+ Cl2 + H2O.
B 1 . Xác định số oxi hoá các nguyên tố(thay đổi SOH). Tìm chất khử và chất oxi hóa.B 2 . Viết các quá trình khử và quá trình oxi hóa, cân bằng mỗi quá trình.B 3 . Xác định hệ số cân bằng sao cho: tổng số e nhường tổng số e nhậnB 4 . Đưa hệ số cân bằng vào phương trình, tính ra hệ số các chất khác trong phương trình(kiểm tra lại theo trật tự: kim loại – phi kim – hidro – oxi)3. Mg + H2SO4 → MgSO4 + H2S + H2O.4. Al + HNO3 → Al(NO3)3 + NH4NO3+ H2O.5. Fe3O4+ HNO3 → Fe(NO3)3+ N2O + H2O.
Đọc tiếp
B 1 . Xác định số oxi hoá các nguyên tố(thay đổi SOH). Tìm chất khử và chất oxi hóa.
B 2 . Viết các quá trình khử và quá trình oxi hóa, cân bằng mỗi quá trình.
B 3 . Xác định hệ số cân bằng sao cho: tổng số e nhường = tổng số e nhận
B 4 . Đưa hệ số cân bằng vào phương trình, tính ra hệ số các chất khác trong phương trình(kiểm tra lại theo trật tự: kim loại – phi kim – hidro – oxi)
3. Mg + H2SO4 → MgSO4 + H2S + H2O.
4. Al + HNO3 → Al(NO3)3 + NH4NO3+ H2O.
5. Fe3O4+ HNO3 → Fe(NO3)3+ N2O + H2O.
B 1 . Xác định số oxi hoá các nguyên tố(thay đổi SOH). Tìm chất khử và chất oxi hóa.B 2 . Viết các quá trình khử và quá trình oxi hóa, cân bằng mỗi quá trình.B 3 . Xác định hệ số cân bằng sao cho: tổng số e nhường tổng số e nhậnB 4 . Đưa hệ số cân bằng vào phương trình, tính ra hệ số các chất khác trong phương trình(kiểm tra lại theo trật tự: kim loại – phi kim – hidro – oxi)7. FeSO4+ H2SO4+ KMnO4 → Fe2(SO4)3 + MnSO4 + K2SO4 + H2O.
Đọc tiếp
B 1 . Xác định số oxi hoá các nguyên tố(thay đổi SOH). Tìm chất khử và chất oxi hóa.
B 2 . Viết các quá trình khử và quá trình oxi hóa, cân bằng mỗi quá trình.
B 3 . Xác định hệ số cân bằng sao cho: tổng số e nhường = tổng số e nhận
B 4 . Đưa hệ số cân bằng vào phương trình, tính ra hệ số các chất khác trong phương trình(kiểm tra lại theo trật tự: kim loại – phi kim – hidro – oxi)
7. FeSO4+ H2SO4+ KMnO4 → Fe2(SO4)3 + MnSO4 + K2SO4 + H2O.
B 1 . Xác định số oxi hoá các nguyên tố(thay đổi SOH). Tìm chất khử và chất oxi hóa.B 2 . Viết các quá trình khử và quá trình oxi hóa, cân bằng mỗi quá trình.B 3 . Xác định hệ số cân bằng sao cho: tổng số e nhường tổng số e nhậnB 4 . Đưa hệ số cân bằng vào phương trình, tính ra hệ số các chất khác trong phương trình(kiểm tra lại theo trật tự: kim loại – phi kim – hidro – oxi)3. Mg + H2SO4→ MgSO4+ H2S + H2O.4. Al + HNO3 → Al(NO3 )3+ NH4NO3 + H2O.5. Fe3O4 + HNO3→ Fe(NO3)3 + N2O + H2O.
Đọc tiếp
B 1 . Xác định số oxi hoá các nguyên tố(thay đổi SOH). Tìm chất khử và chất oxi hóa.
B 2 . Viết các quá trình khử và quá trình oxi hóa, cân bằng mỗi quá trình.
B 3 . Xác định hệ số cân bằng sao cho: tổng số e nhường = tổng số e nhận
B 4 . Đưa hệ số cân bằng vào phương trình, tính ra hệ số các chất khác trong phương trình(kiểm tra lại theo trật tự: kim loại – phi kim – hidro – oxi)
3. Mg + H2SO4→ MgSO4+ H2S + H2O.
4. Al + HNO3 → Al(NO3 )3+ NH4NO3 + H2O.
5. Fe3O4 + HNO3→ Fe(NO3)3 + N2O + H2O.