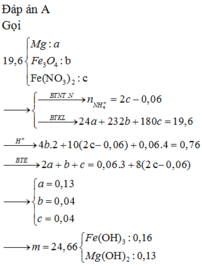Cho 3,04 gam hỗn hợp gồm NaOH và KOH vào dung dịch HCl, thu được 4,15 gam các muối clorua . a/ Viết phương trình phản ứng? b/ Tính số mol mỗi chất trong hỗn hợp ban đầu?

Những câu hỏi liên quan
3,04 gam hỗn hợp NaOH và KOH tác dụng vừa đủ với dung dịch HCl, thu được 4,15 gam các muối clorua. Viết các phương trình hoá học.
Các phương trình hoá học :
HCl + NaOH → NaCl + H 2 O (1)
HCl + KOH → KCl + H 2 O (2
Đúng 0
Bình luận (0)
Cho 3,04 gam hỗn hợp NaOH và KOH tác dụng vừa đủ với dung dịch HCl, thu được 4,15 gam muối clorua. A/ Viết các PTHH xảy ra. B/ Tính khối lượng của mỗi hydroxide ban đầu.
a.
\(NaOH + HCl → NaCl + H_{2}O\)
x x (mol)
\(KOH + HCl → KCl + H_{2}O\)
y y (mol)
Gọi x, y lần lượt là số mol NaOH và KOH
Ta có hệ pt:
\(\begin{cases} 40x + 56y = 3.04\\ 58,5x + 74,5y = 4,15 \end{cases}\) ⇔ \(\begin{cases} x = 0,,02\\ y = 0,04 \end{cases}\)
\(m_{NaOH} = 0,02.40 = 0,8 g\)
\(m_{KOH} = 0,04.56 = 2,24 g\)
Đúng 2
Bình luận (0)
\(NaOH+HCl\rightarrow NaCl+H_2O\)
x------------------>x
\(KOH+HCl\rightarrow KCl+H_2O\)
y------------------>y
Có hệ: \(\left\{{}\begin{matrix}40x+56y=3,04\\58,5x+74,5y=4,15\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,02\\y=0,04\end{matrix}\right.\)
\(m_{NaOH}=0,02.40=0,8\left(g\right)\\ m_{KOH}=0,04.56=2,24\left(g\right)\)
Đúng 0
Bình luận (0)
3,04 gam hỗn hợp NaOH và KOH tác dụng vừa đủ với dung dịch HCl, thu được 4,15 gam các muối clorua. Tính khối lượng của mỗi hiđroxit trong hỗn hợp ban đầu.
Tính khối lượng của mỗi hiđroxit trong hỗn hợp ban đầu :
Đặt x và y là số mol của NaOH và KOH trong hỗn hợp, ta có hệ phương trình :
40x + 56y = 3,04
58,5x + 74,5y = 4,15
Giải hệ phương trình (I) và (II), ta được : x = 0,02 và y = 0,04.
Số gam NaOH và KOH có trong hỗn hợp là :
m NaOH = 40 x 0,02 = 0,8g
m KOH = 56 x 0,04 = 2,24g
*Có thể giải bài toán trên như sau : Đặt x (gam) là khối lượng của NaOH, khối lượng của KOH là (3,04 - x) gam.
Theo (1) : x gam NaOH sinh ra 58,5x/40 gam NaCl.
Theo (2) : (3,04 - x) gam KOH sinh ra 74,5(3,04-x)/56 gam KCl
Rút ra phương trình :
![]()
Giải phương trình, ta có : m NaOH = 0,8 gam và m KOH = 2,24 gam.
Đúng 0
Bình luận (0)
Cho 3,04gam hỗn hợp NaOH và KOH tác dụng với dung dịch HCl thu được 4,15 gam muối a) viết phương trình phản ứng b) tính khối lượng muối bazơ ban đầu c) nếu cho lượng muối trên vào dung dịch AgNO3. tính khối lượng kết tủa thu được
a) NaOH + HCl --> NaCl + H2O
KOH + HCl --> KCl + H2O
b) Gọi số mol của NaOH, KOH là a, b (mol)
=> 40a + 56b = 3,04
Có nNaOH = nNaCl = a (mol)
=> mNaCl = 58,5a (g)
nKOH = nKCl = b (mol)
=> mKCl = 74,5b (g)
=> 58,5a + 74,5b = 4,15
=> a = 0,02; b = 0,04
\(\left\{{}\begin{matrix}m_{NaOH}=0,02.40=0,8\left(g\right)\\m_{KOH}=0,04.56=2,24\left(g\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}m_{NaCl}=0,02.58,5=1,17\left(g\right)\\m_{KCl}=0,04.74,5=2,98\left(g\right)\end{matrix}\right.\)
c)
PTHH: NaCl + AgNO3 --> NaNO3 + AgCl
0,02------------------------>0,02
KCl + AgNO3 --> KNO3 + AgCl
0,04--------------------->0,04
=> \(m_{AgCl}=\left(0,02+0,04\right).143,5=8,61\left(g\right)\)
Đúng 5
Bình luận (0)
\(a,NaOH+HCl\rightarrow NaCl+H_2O\\ KOH+HCl\rightarrow KCl+H_2O\\ b,Đặt:n_{NaOH}=w\left(mol\right);n_{KOH}=e\left(mol\right)\left(w,e>0\right)\\ \Rightarrow\left\{{}\begin{matrix}40w+56e=3,04\\58,5w+74,5e=4,15\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}w=0,02\left(mol\right)\\e=0,04\left(mol\right)\end{matrix}\right.\\ \Rightarrow m_{NaOH}=40w=0,8\left(g\right);m_{KOH}=56e=2,24\left(g\right)\\ c,NaCl+AgNO_3\rightarrow NaNO_3+AgCl\downarrow\\ KCl+AgNO_3\rightarrow KNO_3+AgCl\downarrow\\ n_{AgCl\downarrow}=n_{NaCl}+n_{KCl}=w+e=0,06\left(mol\right)\\ \Rightarrow m_{\downarrow}=m_{AgCl}=143,5.0,06=8,61\left(g\right)\)
Đúng 3
Bình luận (0)
Cho 3,04 g hỗn hợp NaOH và KOH tác dụng với dung dịch HCl, thu được 4,15 g các
muối clorua.
a) Viết các phương trình hóa học xảy ra.
b) Tính khối lượng mỗi bazo trong hỗn hợp ban đầu.
c) Tính khối lượng từng muối thu được sau phản ứng.
PTHH: \(NaOH+HCl\rightarrow NaCl+H_2O\)
a_____________a (mol)
\(KOH+HCl\rightarrow KCl+H_2O\)
b_____________b
Ta lập HPT: \(\left\{{}\begin{matrix}40a+56b=3,04\\58,5a+74,5b=4,15\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,02\\b=0,04\end{matrix}\right.\)
\(\Rightarrow...\)
Đúng 2
Bình luận (1)
Cho 3,04 gam hỗn hợp NaOH và KOH tác dụng với dung dịch axit HCl thu được 4,15 gam hỗn hợp muối clorua. Khối lượng hidroxit trong hỗn hợp là
A. 1,17 g và 2,98 g
B. 1,12 g và 1,6 g
C. 1,12 g và 1,92 g
D. 0,8 g và 2,24 g
Gọi số mol của NaOH và KOH lần lượt là x và y (mol)
PTHH:
NaOH + HCl → NaCl + H2O
x x (mol)
KOH + HCl → KCl + H2O
y y (mol)
\(\left\{{}\begin{matrix}\text{mhh=40x+56y=3,04}\\\text{mmuối=58,5x +74,5y=4,15}\end{matrix}\right.\)⇒\(\left\{{}\begin{matrix}\text{x=0,02}\\\text{y=0,04}\end{matrix}\right.\)
⇒ mNaOH = 40. 0,02= 0,8 (g)
mKOH = 56.0,04= 2,24 (g)
Đúng 0
Bình luận (0)
Cho 3,04 gam hỗn hợp NaOH và KOH tác dụng với dung dịch axit HCl thu được 4,15 gam hỗn hợp muối clorua. Khối lượng hidroxit trong hỗn hợp là:
A. 1,17 g và 2,98 g
B. 1,12 g và 1,6 g
C. 1,12 g và 1,92 g
D. 0,8 g và 2,24 g
Đáp án D.
NaOH + HCl → NaCl + H2O
x(mol) x(mol)
KOH + HCl → KCl + H2O
y(mol) y(mol)
gọi x, y lần lượt là số mol NaOH và KOH
theo bài ra ta có hệ pt
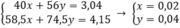
mNaOH = 0,02.40 = 0,8 (g)
mKOH = 0,04.56 = 2,24 (g)
Đúng 0
Bình luận (0)
Cho 19,6 gam hỗn hợp rắn X gồm Mg, Fe3O4 và Fe(NO3)2 vào dung dịch chứa 0,76 mol HCl đun nóng sau khi kết thúc phản ứng phản ứng thu được 0,06 mol khí NO và dung dịch Y chỉ chứa muối clorua (không có muối Fe2+). Cho NaOH dư vào Y thu được m gam kết tủa. Giá trị của m là? A. 24,66 B. 22,84 C. 26,24 D. 25,42
Đọc tiếp
Cho 19,6 gam hỗn hợp rắn X gồm Mg, Fe3O4 và Fe(NO3)2 vào dung dịch chứa 0,76 mol HCl đun nóng sau khi kết thúc phản ứng phản ứng thu được 0,06 mol khí NO và dung dịch Y chỉ chứa muối clorua (không có muối Fe2+). Cho NaOH dư vào Y thu được m gam kết tủa. Giá trị của m là?
A. 24,66
B. 22,84
C. 26,24
D. 25,42
Cho 3,04 gam hỗn hợp NaOH và KOH tác dụng vừa đủ với dung dịch HCl thu được 4,15g các muối clorua
Tính khối lượng của mỗi chất trong hỗn hợp ban đầu
Gọi $n_{NaOH} = a(mol) ; n_{KOH} = b(mol)$
Suy ra : $40a + 56b = 3,04(1)$
$NaOH + HCl \to NaCl + H_2O$
$KOH + HCl \to KCl + H_2O$
Theo PTHH, ta có :
$m_{muối} = 58,5a + 74,5b = 4,15(2)$
Từ (1)(2) suy ra a = 0,02 ; b = 0,04
$m_{NaOH} = 0,02.40 = 0,8(gam)$
$m_{KOH} = 0,04.56 = 2,24(gam)$
Đúng 3
Bình luận (2)
Đặt \(\left\{{}\begin{matrix}n_{NaOH}=a\left(mol\right)\\n_{KOH}=b\left(mol\right)\end{matrix}\right.\)
\(PTHH:NaOH+HCl\rightarrow NaCl+H_2O\\ PTHH:KOH+HCl\rightarrow KCl+H_2O\)
Theo đề bài ta có hpt:
\(\left\{{}\begin{matrix}40a+56b=3,04\\58,5a+74,5b=4,15\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,02\\b=0,04\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}m_{NaOH}=0,8\left(g\right)\\m_{KOH}=2,24\left(g\right)\end{matrix}\right.\)
Đúng 4
Bình luận (2)