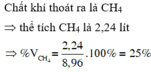Bài 7 .Dẫn 22,4 lít hỗn hợp khí CO và CO2 (đktc) vào dung dịch NaOH dư thấy có 2,24 lít khí ở đktc thoát ra ngoài. Tính % về thể tích và % về khối lượng các khí trong hỗn hợp ban đầu

Những câu hỏi liên quan
Dẫn từ từ 3,36 lít hỗn hợp gồm etilen và propilen (đktc) vào dung dịch brom thấy dung dịch bị nhạt màu và không có khí thoát ra. Khối lượng dung dịch sau phản ứng tăng 4,90gam.
Tính thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp ban đầu.
Gọi số mol của etilen và propilen lần lượt là x và y mol.
Khối lượng dung dịch sau phản ứng tăng lên chính là khối lượng của hỗn hợp etilen và propilen.
Ta có hệ phương trình:
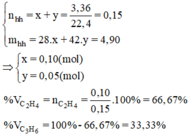
Đúng 1
Bình luận (0)
Bài 7: Dẫn từ từ 6,72 lít hỗn hợp gồm CH4 và C2H2(đktc) lội qua dung dịch Brom dư thấy thoát ra 4,48 lít khí.
a) Viết PTHH xảy ra và tính phần trăm về khối lượng từng chất trong hỗn hợp ban đầu.
b) Tính khối lượng brom tham gia phản ứng
a)
PTHH: C2H2 + 2Br2 --> C2H2Br4
Khí thoát ra là CH4
\(n_{CH_4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(n_{C_2H_2}=\dfrac{6,72}{22,4}-0,2=0,1\left(mol\right)\)
\(\left\{{}\begin{matrix}\%m_{CH_4}=\dfrac{0,2.16}{0,2.16+0,1.26}.100\%=55,17\%\\\%m_{C_2H_2}=\dfrac{0,1.26}{0,2.16+0,1.26}.100\%=44,83\%\end{matrix}\right.\)
b)
PTHH: C2H2 + 2Br2 --> C2H2Br4
0,1--->0,2
=> mBr2 = 0,2.160 = 32 (g)
Đúng 3
Bình luận (0)
Dẫn 6,72 lít một hỗn hợp khí gồm hai hiđrocacbon mạch hở (không phải mạch vòng) qua dung dịch brom dư sao cho phản ứng xảy ra hoàn toàn. Sau thí nghiệm, thấy khối lượng bình đựng dung dịch brom tăng thêm 5,6 gam, đồng thời thoát ra 2,24 lít một chất khí. Mặt khác, nếu đốt cháy toàn bộ 6,72 lít hỗn hợp trên thấy tạo ra 22 gam
CO
2
và 10,8 gam
H
2
O
. Biết các thể...
Đọc tiếp
Dẫn 6,72 lít một hỗn hợp khí gồm hai hiđrocacbon mạch hở (không phải mạch vòng) qua dung dịch brom dư sao cho phản ứng xảy ra hoàn toàn. Sau thí nghiệm, thấy khối lượng bình đựng dung dịch brom tăng thêm 5,6 gam, đồng thời thoát ra 2,24 lít một chất khí. Mặt khác, nếu đốt cháy toàn bộ 6,72 lít hỗn hợp trên thấy tạo ra 22 gam CO 2 và 10,8 gam H 2 O . Biết các thể tích khí đo ở đktc.
Xác định công thức phân tử của hai hiđrocacbon và tính thành phần % về thể tích của mỗi chất trong hỗn hợp
Thể tích khí đã tác dụng với dung dịch brom là : 6,72 - 2,24 = 4,48 (lít).
=> Số mol khí phản ứng với dung dịch brom là : 4,48/22,4 = 0,2 mol
Khối lượng bình brom tăng lên là do khối lượng hiđrocacbon bị hấp thụ. Vậy khối lượng mol phân tử của hiđrocacbon là :
5,6/0,2 = 28 (gam/mol)
=> Công thức phân tử của một hiđrocacbon là C 2 H 4
Dựa vào phản ứng đốt cháy tìm được hiđrocacbon còn lại là CH 4
% V C 2 H 4 = 4,48/6,72 x 100% = 66,67%; V CH 4 = 33,33%
Đúng 0
Bình luận (0)
Dẫn từ từ 3,36 lít hỗn hợp khí etilen và propilen(đktc) vào dung dich brom thấy dung dich bị nhạt màu và không có khí thoát ra .Khối lượng dung dịch sau phản ứng tăng 4,9 gam. Tính % theo thể tích của mỗi khí trong hỗn hợp ban đầu.?
\(n_{C_2H_4} = a\ mol;n_{C_3H_6} = b\ mol\\ \Rightarrow a + b = \dfrac{3,36}{22,4} = 0,15(1)\\ C_2H_4 + Br_2 \to C_2H_4Br_2\\ C_3H_6 + Br_2 \to C_3H_6Br_2\\ m_{tăng} = 28a + 42b = 4,9(2)\\ (1)(2)\Rightarrow a = 0,1; b = 0,05\\ \%V_{C_2H_4} = \dfrac{0,1}{0,15}.100\% = 66,67\%\\ \%V_{C_3H_6} = 100\% -66,67\% = 33,33\%\)
Đúng 2
Bình luận (0)
Hỗn hợp X gồm Al và Cu. Cho 11,8 gam hỗn hợp X vào dung dịch axit clohidric dư thấy thoát ra 6,72 lít khí ở đktc.
a) Viết PTHH
b) Tính thành phần trăm về khối lượng mỗi kim loại trong hỗn hợp X
c) Nếu cho 11,8 gam hỗn hợp X phản ứng hoàn toàn với dung dịch NaOH dư, tính thể tích khí thoát ra ở đktc
a) \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Cu+HCl\rightarrow\)(không phản ứng)
2Al + 6HCl => 2AlCl3 + 3H2
0,3/3*2 (6,72/22,4)
=> mAl = 0,2 *27 =5,4g; mCu = 11,8 - 5,4 = 6,4g
Hỗn hợp X gồm 3 khí: N2O, CO2, C3H8 có % khối lượng bằng nhau. Dẫn 3,36 lít X qua dung dịch Ba(OH)2 dư thấy có V lít khí thoát ra (các thể tích đo ở đktc). Giá trị của V là
A. 2,24 lít. B. 3,36 lít. C. 1,12 lít. D. (3,36 – V) lít.
Gọi số mol của N2O, CO2, C3H8 là a, b, c
=> \(\left\{{}\begin{matrix}a+b+c=\dfrac{3,36}{22,4}=0,15\\44a=44b=44c\end{matrix}\right.\)
=> a = b = c = 0,05 (mol)
Khí thoát ra gồm N2O, C3H8
=> V = (0,05 + 0,05).22,4 = 2,24(l)
=> A
Đúng 1
Bình luận (0)
Gọi số mol của N2O, CO2, C3H8 là a, b, c
=>
Đúng 0
Bình luận (0)
Bài 5. Hỗn hợp B gồm 2 khí metan và etilen. Dẫn 4,48 lít B (đktc) vào dung dịch brom thấy bình brom nhạt màu và có 3,36 lít khí thoát ra.(1) Tính % về thể tích của mỗi khí trong hỗn hợp ………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………(2) Đốt cháy hoàn toàn 3,36 lít khí thoát ra rồi dẫn sản phẩm vào dung dịch Ca(OH)2 dư. Tính khối lượng kết tủa thu được? ………………………………...
Đọc tiếp
Bài 5. Hỗn hợp B gồm 2 khí metan và etilen. Dẫn 4,48 lít B (đktc) vào dung dịch brom thấy bình brom nhạt màu và có 3,36 lít khí thoát ra.
(1) Tính % về thể tích của mỗi khí trong hỗn hợp
………………………………………………………………………………………………
………………………………………………………………………………………………
………………………………………………………………………………………………
………………………………………………………………………………………………
………………………………………………………………………………………………
(2) Đốt cháy hoàn toàn 3,36 lít khí thoát ra rồi dẫn sản phẩm vào dung dịch Ca(OH)2 dư. Tính khối lượng kết tủa thu được?
………………………………………………………………………………………………
………………………………………………………………………………………………
………………………………………………………………………………………………
………………………………………………………………………………………………
………………………………………………………………………………………………
B5:
1)
\(V_{thoát}=V_{CH_4\left(đktc\right)}=3,36\left(l\right)\\ \Rightarrow\%V_{\dfrac{CH_4}{B}}=\dfrac{3,36}{4,48}.100=75\%\Rightarrow\%V_{\dfrac{C_2H_4}{B}}=100\%-75\%=25\%\)
2)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\\ CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\\ n_{CH_4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ \Rightarrow n_{CaCO_3}=n_{CO_2}=n_{CH_4}=0,15\left(mol\right)\\ \Rightarrow m_{\downarrow}=m_{CaCO_3}=100.0,15=15\left(g\right)\)
Đúng 3
Bình luận (0)
Dẫn 8,96 lít hỗn hợp khí X gồm metan và etilen vào dung dịch brom dư, thấy dung dịch nhạt màu và còn lại 2,24 lít khí thoát ra. (Thể tích các khí đều đo ở đktc). Thành phần phần trăm thể tích của metan trong X là A. 25,0% B. 50,0% C. 60,0% D. 37,5%
Đọc tiếp
Dẫn 8,96 lít hỗn hợp khí X gồm metan và etilen vào dung dịch brom dư, thấy dung dịch nhạt màu và còn lại 2,24 lít khí thoát ra. (Thể tích các khí đều đo ở đktc). Thành phần phần trăm thể tích của metan trong X là
A. 25,0%
B. 50,0%
C. 60,0%
D. 37,5%
Dẫn 3,36 lít khí hỗn hợp A gồm propin và eilen đi vào một lượng dư dung dịch AgNO3 trong NH3 thấy còn 0,840 lít khí thoát ra và có m gam kết tủa. Các thể tích khí đo ở đktc Tính m
Thể tích proprin là: 3,36 - 0,84 = 2,52 (l)
nC3H4 = 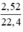 = 0,1125(mol)
= 0,1125(mol)
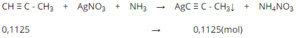
⇒ m = 0,1125. 147 = 16,5375 (g)
Đúng 0
Bình luận (0)









![[柠檬]๛Čɦαŋɦ ČŠツ](https://hoc24.vn/images/avt/avt6342624_256by256.jpg)