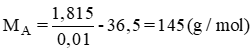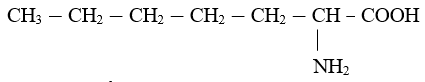Tính khối lượng riêng của dung dịch h2so4 98% biết rằng nếu lấy vừa đủ 1ml dung dịch axit đó đem phã loãng và trung hoà bằng một lượng naoh vừa đủ đem cô cạn thì thu được 2,6128 muối khan

Những câu hỏi liên quan
Để trung hòa 10ml dung dịch hỗn hợp axit gồm H2SO4 và HCl cần dùng 40ml dung dịch NaOH 0,5M. Mặt khác lấy 100ml dung dịch hỗn hợp axit trên đem trung hòa với một lượng dung dịch NaOH vừa đủ rồi cô cạn thì thu được 24,65g muối khan. Tính nồng độ mol/L của mỗi axit
Để trung hòa 10 ml dung dịch hỗn hợp axit gồm HCl và
H
2
S
O
4
cần dùng 40ml dung dịch NaOH 0,5M. Mặt khác lấy 100 ml dung dịch hỗn hợp axit trên đem trung hòa bằng một lượng NaOH vừa đủ rồi cô cạn thì thu được 13,2 gam muối khan. Nồng độ mol của mỗi axit trong dung dịch ban đầu lần lượt là A. 0,8M và 0,6M B. 1M và 0,5M C. 0,6M và 0,7M D. 0,2M và 0,9M
Đọc tiếp
Để trung hòa 10 ml dung dịch hỗn hợp axit gồm HCl và H 2 S O 4 cần dùng 40ml dung dịch NaOH 0,5M. Mặt khác lấy 100 ml dung dịch hỗn hợp axit trên đem trung hòa bằng một lượng NaOH vừa đủ rồi cô cạn thì thu được 13,2 gam muối khan. Nồng độ mol của mỗi axit trong dung dịch ban đầu lần lượt là
A. 0,8M và 0,6M
B. 1M và 0,5M
C. 0,6M và 0,7M
D. 0,2M và 0,9M
Chọn A
Gọi nồng độ mol ban đầu của HCl và H 2 S O 4 lần lượt là x và y (M)


Đúng 0
Bình luận (0)
để trung hòa 50ml dung dịch hỗn hợp axit gồm H2SO4 và HCl cần dg 200ml dung dịch NaOH 1M
. Mặt khác lấy 100ml dung dịch hỗn hợp axit trên đem trung hòa với 1 lượng dung dịch NaOH vừa đủ rồi cô cạn thì thu được 24,65g muối khan. Tinh nồng độ mol/L của mỗi axit trong dung dịch ban đầu
Hoà tan 19,75 gam một muối hiđrocacbonat vào nước thu được dung dịch X. Cho X tác dụng với một lượng dung dịch H2SO4 10% vừa đủ, sau đó đem cô cạn dung dịch thì thu được 16,5 gam một muối sunfat trung hoà khan. Công thức phân tử của muối hiđrocacbonat là A. Ba(HCO3)2 B. NaHCO3 C. Mg(HCO3)2 D. NH4HCO3
Đọc tiếp
Hoà tan 19,75 gam một muối hiđrocacbonat vào nước thu được dung dịch X. Cho X tác dụng với một lượng dung dịch H2SO4 10% vừa đủ, sau đó đem cô cạn dung dịch thì thu được 16,5 gam một muối sunfat trung hoà khan. Công thức phân tử của muối hiđrocacbonat là
A. Ba(HCO3)2
B. NaHCO3
C. Mg(HCO3)2
D. NH4HCO3
Hoà tan hết hỗn hợp X gồm oxit của một kim loại có hoá trị II và muối cacbonat của kim loại đó bằng H2SO4 loãng vừa đủ, sau phản ứng thu được sản phẩm gồm khí Y và dung dịch Z. Biết lượng khí Y bằng 44% lượng X. Đem cô cạn dung dịch Z thu được một lượng muối khan bằng 168% lượng X. Hỏi kim loại hoá trị II nói trên là kim loại gì? Tính thành phần phần trăm của mỗi chất trong hỗn hợp X.
Đọc tiếp
Hoà tan hết hỗn hợp X gồm oxit của một kim loại có hoá trị II và muối cacbonat của kim loại đó bằng H2SO4 loãng vừa đủ, sau phản ứng thu được sản phẩm gồm khí Y và dung dịch Z. Biết lượng khí Y bằng 44% lượng X. Đem cô cạn dung dịch Z thu được một lượng muối khan bằng 168% lượng X. Hỏi kim loại hoá trị II nói trên là kim loại gì? Tính thành phần phần trăm của mỗi chất trong hỗn hợp X.
RO+H2SO4→ RSO4+H2O (1)
RCO3+H2SO4→ RSO4+CO2+H2O (2)
Đặt a là khối lượng hỗn hợp X.
x,y là số mol RO và RCO3
Ta có : (R+16)x+(R+60)y=a (*)
Từ (1) và (2) \Rightarrow (R+96)(x+y)=1,68a (**)
Từ (2) \Rightarrow y=0,01a (***)
Giải (*),(**) và (***) \Rightarrow x=0,004a : R=24
Vậy R là Mg
Đúng 0
Bình luận (2)
Cho 0,01 mol amino axit A tác dụng vừa đủ với 80 ml dung dịch HCI 0,125M; sau đó đem cô cạn thì được 1,815 gam muối. Nếu trung hoà A bằng một lượng vừa đủ NaOH thì thấy tỉ lệ mol giữa A và NaOH là 1 : 1.a) Xác định công thức phân tử và công thức cấu tạo của A, biết rằng phân tử A có mạch cacbon không phân nhánh và A thuộc loại α- amino axit.b) Viết công thức cấu tạo các đồng phân có thể có của A và gọi tên chúng theo danh pháp thay thế, khi- thay đổi vị trí nhóm amino.- thay đổi cấu tạo...
Đọc tiếp
Cho 0,01 mol amino axit A tác dụng vừa đủ với 80 ml dung dịch HCI 0,125M; sau đó đem cô cạn thì được 1,815 gam muối. Nếu trung hoà A bằng một lượng vừa đủ NaOH thì thấy tỉ lệ mol giữa A và NaOH là 1 : 1.
a) Xác định công thức phân tử và công thức cấu tạo của A, biết rằng phân tử A có mạch cacbon không phân nhánh và A thuộc loại α- amino axit.
b) Viết công thức cấu tạo các đồng phân có thể có của A và gọi tên chúng theo danh pháp thay thế, khi
- thay đổi vị trí nhóm amino.
- thay đổi cấu tạo gốc hiđrocacbon và nhóm amino vẫn ở vị trí α.
nHCl = 0,08 . 0,125 = 0,01 (mol)
nHCl = nA ⇒ A chỉ có 1 nhóm NH2
nA : nNaOH = 1 : 1 ⇒ A chỉ có 1 nhóm COOH
Gọi công thức của A là H2N-R-COOH
⇒ mR = 145 -45 -16 = 84 (gam)
Biện luận suy ra R là gốc C6H12 Vì A không phân nhánh nên CTCT của A là:
CTCT của A là
Đúng 1
Bình luận (0)
Cho kim loại X (hóa trị III) tác dụng với dung dịch HCl vừa đủ rồi cô cạn dung dịch sau phản ứng, thu được a gam muối khan. Nếu lấy cùng lượng X như trên cho tác dụng với dd H2SO4 loãng vừa đủ rồi cô cạn dung dịch, thì thu được b gam muối khan. Lập biểu thức tính số mol X theo a, b.
\(n_{XCl_3}=\dfrac{a}{M_X+106,5}\left(mol\right)\)
PTHH: 2X + 6HCl --> 2XCl3 + 3H2
=> \(n_X=\dfrac{a}{M_X+106,5}\left(mol\right)\)
\(n_{X_2\left(SO_4\right)_3}=\dfrac{b}{2.M_X+288}\left(mol\right)\)
PTHH: 2X + 3H2SO4 --> X2(SO4)3 + 3H2
=> \(n_X=\dfrac{b}{M_X+144}\left(mol\right)\)
1,Tính khối lượng riêng của dung dịch H2SO4 98% biết rằng lấy 1 mol dung dịch axit đó đem pha lấy rồi trung hòa bởi dung dịch NAOH và đã thu được dung dịch chứa 2,6128g muối
2, Hòa tan một mol CO3 cần kim loại hóa trị 1 bằng 1 lượng vừa đủ dung dịch H2SO4 1% thu được muối nồng độ 10.89% . Lập CTHH
Hoà tan hoàn toàn 10,8 gam hỗn hợp Al và Fe bằng dung dịch
H
2
S
O
4
loãng vừa đủ. Sau phản ứng thấy khối lượng dung dịch tăng thêm 10,2 gam so với ban đầu. Khối lượng muối khan thu được khi cô cạn dung dịch sau phản ứng là A. 26,4 gam B. 39,6 gam C. 79,2 gam D. 68,4 gam
Đọc tiếp
Hoà tan hoàn toàn 10,8 gam hỗn hợp Al và Fe bằng dung dịch H 2 S O 4 loãng vừa đủ. Sau phản ứng thấy khối lượng dung dịch tăng thêm 10,2 gam so với ban đầu. Khối lượng muối khan thu được khi cô cạn dung dịch sau phản ứng là
A. 26,4 gam
B. 39,6 gam
C. 79,2 gam
D. 68,4 gam