Hợp chất A có khối lượng mol phân tử là 106 g/mol,thành phần các nguyên tố theo khối lượng:43,4%Na,11,3%Cvà 45,3%O.Tìm CTHH của hợp chất A

Những câu hỏi liên quan
Hợp chất a có khối lượng mol là 58,5 gam/mol A: thành phần các nguyên tố theo khối lượng lần lượt là 39,32% Na và 60,68% Cl B: hợp chất b có khối lượng mol là 106 g/mol hành phần các nguyên tố theo khối lượng lần lượt là 43,4% Na, 11,3% c 45,3% O C: hợp chất c có khối lượng mol là 80g/mol thành phần các nguyên tố theo khối lượng lần lượt là 80% Cu và 20%O
Hợp chất B có khối lượng phân tử là 106 g/mol, biết thành phần phần trăm của
các nguyên tố theo khối lượng là 43,4 % Na, 11,3% C và 45,3% O.
Đặt : CTHH của B là : NaxCyOz
\(\%Na=\dfrac{23x}{106}\cdot100\%=43.4\%\)
\(\Rightarrow x=2\)
\(\%C=\dfrac{12x}{106}\cdot100\%=11.3\%\)
\(\Rightarrow y=1\)
\(\%O=\dfrac{16z}{106}\cdot100\%=45.3\%\)
\(\Rightarrow z=3\)
CTHH của B là : Na2CO3
Đúng 2
Bình luận (0)
Tìm công thức hóa học của các hợp chất có thành phần các nguyên tố sau
1) hợp chất A có khối lượng mol là 106 gam / mol thành phần các nguyên tố theo khối lượng : 43,4% Na ; 11,3% C và 45,3% O
2) hợp chất B có thành phần các nguyên tố là : 60,68% Cl và còn lại là Na biết hợp chất B có khối lượng mol phân tử là 80g/mol oxít
Hãy tìm công thức hóa học của những hợp chất có thành phần các nguyên tố như sau:
a) Hợp chất A có khối lượng mol phân tử là 58,5g có thành phần các nguyên tố 60,68% Cl và còn lại là Na.
b) Hợp chất B có khối lượng mol phân tử là 106g, thành phần 43,4% Na 11,3% C và 45,3% O.
a) %Cl = 60,68%
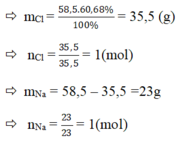
Vậy trong 1 phân tử hợp chất A có : 1 nguyên tử Na, 1 nguyên tử Cl.
⇒ CTHH của hợp chất A : NaCl
b)
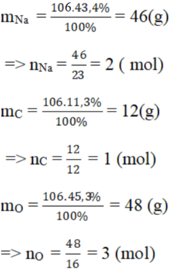
Vậy trong 1 phân tử hợp chất B có: 2 nguyên tử Na, 1 nguyên tử C, 3 nguyên tử O.
⇒ CTHH của hợp chất B : Na2CO3.
Đúng 3
Bình luận (0)
bài 1: hợp chất A có tỉ khối so với H2 là 22. Hãy cho biết 5,6 lít khí A ở(đktc) có khối lượng là bao nhiêu gam?bài 2: tìm công thữ hóa học của những hợp chất có thành phần nguyên tố như sau:a) hợp chất A tạo bởi 2 nguyên tố: C và O có khối lượng mol là 44(g?mol),trong đó cacbon chiếm 27,3% về khối lượng,còn lại là % Ob) hợp chất B tạo bởi 3 nguyên tố: Na,C,O có khối lượng mol là 44(g/mol), thành phần các nguyên tố lần lượt là: 43,4% Na,11,3% C,45,3%c) một hợp chất khí A có thành phần % theo khố...
Đọc tiếp
bài 1: hợp chất A có tỉ khối so với H2 là 22. Hãy cho biết 5,6 lít khí A ở(đktc) có khối lượng là bao nhiêu gam?
bài 2: tìm công thữ hóa học của những hợp chất có thành phần nguyên tố như sau:
a) hợp chất A tạo bởi 2 nguyên tố: C và O có khối lượng mol là 44(g?mol),trong đó cacbon chiếm 27,3% về khối lượng,còn lại là % O
b) hợp chất B tạo bởi 3 nguyên tố: Na,C,O có khối lượng mol là 44(g/mol), thành phần các nguyên tố lần lượt là: 43,4% Na,11,3% C,45,3%
c) một hợp chất khí A có thành phần % theo khối lượng: 82,35% N,17,65% H. Hợp chất A có tỉ khối với H2 là 8,5. Hãy cho biết:
- CTHH của hợp chất A
- số mol nguyên tử của các nguyên tố có trong 0,5 mol hợp chất A.
bài1
ta có dA/H2=22 →MA=22MH2=22 \(\times\) 2 =44
nA=\(\frac{5,6}{22,4}\)=0,25
\(\Rightarrow\)mA=M\(\times\)n=11 g
Đúng 0
Bình luận (0)
MA=dA/\(H_2\)×M\(H_2\)=22×(1×2)=44g/mol
nA=VA÷22,4=5,6÷22,4=0,25mol
mA=nA×MA=0,25×44=11g
Đúng 0
Bình luận (0)
a)
MC=27,3×44÷100\(\approx\)12g/mol
% mO=100-27,3=72,7%
MO=72,7×44÷100\(\approx\)32g/mol
Công thức hóa học chung: CaxOy
Theo công thức hóa học có:
x×\(III\)=y×\(IV\)
Lập tỉ lệ: \(\dfrac{x}{y}=\dfrac{II}{IV}=\dfrac{2}{4}=\dfrac{1}{2}\)
=>x=1 và y=2
Công thức hóa học của hợp chất: CO\(_2\)
Đúng 0
Bình luận (0)
Hãy tìm công thức hóa học của những hợp chất có thành phần các nguyên tố như sau:
a) Hợp chất A có khối lượng mol phân tử là 58,5 g/mol, thành phần các nguyên tố theo khối lượng: 60,68% Cl và còn lại là Na.
b) Hợp chất B có khối lượng mol phân tử là 106 g/mol, thành phần các nguyên tố theo khối lượng: 43,4% Na; 11,3% C; 45,3% O
Đọc tiếp
Hãy tìm công thức hóa học của những hợp chất có thành phần các nguyên tố như sau:
a) Hợp chất A có khối lượng mol phân tử là 58,5 g/mol, thành phần các nguyên tố theo khối lượng: 60,68% Cl và còn lại là Na.
b) Hợp chất B có khối lượng mol phân tử là 106 g/mol, thành phần các nguyên tố theo khối lượng: 43,4% Na; 11,3% C; 45,3% O
a) Hợp chất A có khối lượng mol phân tử là 58,5 g/mol, thành phần các nguyên tố theo khối lượng: 60,68% Cl và còn lại là Na.
b) Hợp chất B có khối lượng mol phân tử là 106 g/mol, thành phần các nguyên tố theo khối lượng: 43,4% Na; 11,3% C; 45,3% O
Bài giải:
a) Ta có:
MA = 58,5 g
%Cl = 60,68% => %Na = 39,32%
=> MCl = = 35,5 đvC => nCl = 1 mol
=> MNa = = 23 đvC => nNa = 1 mol
Vì Na hóa trị I và Cl hóa trị 1 nên CTHH: NaCl
b) Ta có:
MB =106 g
MNa = = 46 => nNa =
= 2 mol
MC = = 12 => nC = 1 mol
MO = = 48 => nO =
= 3 mol
Suy ra trong một phân tử hợp chất B có 2 nguyên tử Na, 1 nguyên tử C và 3 nguyên tử O
Do đó công thức hòa học của hợp chất B là Na2CO3
Đúng 1
Bình luận (1)
a) Ta có:
MA = 58,5 g
%Cl = 60,68% => %Na = 39,32%
=> MCl = = 35,5 đvC => nCl = 1 mol
=> MNa = = 23 đvC => nNa = 1 mol
Vì Na hóa trị I và Cl hóa trị 1 nên CTHH: NaCl
b) Ta có:
MB =106 g
MNa = = 46 => nNa =
= 2 mol
MC = = 12 => nC = 1 mol
MO = = 48 => nO =
= 3 mol
Suy ra trong một phân tử hợp chất B có 2 nguyên tử Na, 1 nguyên tử C và 3 nguyên tử O
Do đó công thức hòa học của hợp chất B là Na2CO3
Đúng 0
Bình luận (2)
a) Ta có: MA=58,5(g/mol)
%Cl=60,68% -> %Na=100%-60,68=39,32%
-> MCl=60,68%÷100%×58,5=35,5 đvC -> nCl=1(mol)
và MNa=58,5%-35,5=23 đvC -> nNa=1(mol)
vậy công thức hóa học của A là: NaCl
b)ta có:
MB=106(g/mol)
MNa=43,4%÷100%×106=46(g/mol)->nNa=2(mol)
MC=11,3%:100%×106=12(g/mol)->nC=1(mol)
MO=45,3%÷100%×106=48(g/mol)->nO=3(mol)
vậy công thức hóa học của B là: Na2CO3
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
một hợp chất R thành phần về khối lượng các nguyên tố là: 43,4%Na; 11,3%C và 45,3%O.Em hãy xác định công thức hóa học của hợp chất khối lượng mol là 106g
Đặt : CTHH có dạng là : \(Na_xC_yO_z\)
\(\%Na=\dfrac{23x}{106}\cdot100\%=43.4\%\)
\(\Rightarrow x=2\)
\(\%C=\dfrac{12x}{106}\cdot100\%=11.3\%\)
\(\Rightarrow y=1\)
\(z=\dfrac{106-23\cdot2-12}{16}=3\)
CTHH có dạng là : Na2CO3
Đúng 1
Bình luận (1)
hãy tìm công thức hóa học của những hợp chất có thành phần các nguyên tố như sau
hợp chất A có khối lượng mol phân tử là 58,5 gam/mol thành phần các nguyên tố theo khối lượng 43,3% Na ; 11,3% C và còn lại là O
hợp chất B có khối lượng mol phân tử là 106 gam/mol thành phần các nguyên tố theo khối lượng 60,68% Cl và còn lại là Na
Hợp chất A:
- Khối lượng của từng nguyên tố là:
\(m_{Na}=\dfrac{58,5\text{x}43,3}{100}=25\left(g\right)\)
\(m_C=\dfrac{58,5x11,3}{100}=7\left(g\right)\)
\(m_O=58,5-25-7=26,5\left(g\right)\)
- Số mol của từng nguyên tố là:
\(n_{Na}=\dfrac{25}{23}=1\left(mol\right)\)
\(n_C=\dfrac{7}{12}=1\left(mol\right)\)
\(n_O=\dfrac{26,5}{16}=2\left(mol\right)\)
Vậy: Công thức hoá học của hợp chất A là \(NaCO_2\)
- Hợp chất B:
- Khối lượng của từng nguyên tố:
\(m_{Cl}=\dfrac{60,68\text{x}106}{100}=64\left(g\right)\)
\(m_{Na}=106-64=42\left(g\right)\)
- Số mol của từng nguyên tố là:
\(n_{Cl}=\dfrac{64}{35,5}=2\left(mol\right)\)
\(n_{Na}=\dfrac{42}{23}=2\left(mol\right)\)
Vậy: Công thức hoá học của hợp chất B là \(Na_2Cl_2\)
Đúng 0
Bình luận (0)
Hãy tìm công thức hóa học của những hợp chất có thành phần các nguyên tố như sau:
a) Hợp chất A có khối lượng mol phân tử là 58,5 g/mol, thành phần các nguyên tố theo khối lượng: 60,68% Cl và còn lại là Na.
b) Hợp chất B có khối lượng mol phân tử là 106 g/mol, thành phần các nguyên tố theo khối lượng: 43,4% Na; 11,3% C; 45,3% O
Khối lượng của mỗi nguyên tố trong 1 mol hợp chất là:
mCl = 58,5.60,6810058,5.60,68100 = 35,5 (g)
mNa = 58,5 - 35,5 = 23 (g)
Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất là:
nCl = 35,535,535,535,5 = 1 (mol)
nNa = 23232323 = 1 (mol)
Suy ra trong một phân tử hợp chất có: 1 nguyên tử Na và 1 nguyên tử Cl.
Công thức hóa học của hợp chất là: NaCl.
b)
Khối lượng của mỗi nguyên tố trong 1 mol hợp chất là:
mNa = 106.43,4100106.43,4100 = 46 (g)
mC = 106.11,3100106.11,3100 = 12 (g)
mO = 106 - 46 - 12 = 48 (g)
Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất là:
nNa = 46234623 = 2 (mol)
nC = 12121212 = 1 (mol)
nO = 48164816 = 3 (mol)
Suy ra trong một phân tử hợp chất có: 2 nguyên tử Na, 1 nguyên tử C và 3 nguyên tử O.
Công thức hóa học của hợp chất là: Na2CO3
Đúng 0
Bình luận (1)
a) \(\%Na=100\%-60,68\%=39,32\%\)
Gọi CTHH là NaxCly
Ta có: \(23x\div35,5y=39,32\div60,68\)
\(\Rightarrow x\div y=\dfrac{39,32}{23}\div\dfrac{60,68}{35,5}\)
\(\Rightarrow x\div y=1\div1\)
Vậy \(x=1;y=1\)
Vậy CTHH đơn giản là (NaCl)n
ta có: \(58,5n=58,5\)
\(\Leftrightarrow n=1\)
Vậy CTHH là NaCl
Đúng 0
Bình luận (0)
b) Gọi CTHH là NaxCyOz
Ta có: \(23x\div12y\div16z=43,4\div11,3\div45,3\)
\(\Rightarrow x\div y\div z=\dfrac{43,4}{23}\div\dfrac{11,3}{12}\div\dfrac{45,3}{16}\)
\(\Rightarrow x\div y\div z=2\div1\div3\)
Vậy \(x=2;y=1;z=3\)
Vậy CTHH đơn giản là (Na2CO3)n
ta có: \(106n=106\)
\(\Leftrightarrow n=1\)
Vậy CTHH là Na2CO3
Đúng 0
Bình luận (0)



























