lập công thức hóa học của 1 oxits sắt chứa 30%oxi về khối lượng biết phân tử khối của oxit là 160

Những câu hỏi liên quan
Oxit Y có 30% oxi về khối lượng, còn lại là sắt. Biết phân tử khối của Y là 160 đvC. Hãy xác định công thức hóa học và tên gọi của Y.
%Fe = 100 - 30 = 70%
CT : FexOy
%Fe = 56x/ 160 * 100% = 70%
=> x = 2
%O = 16y/160 * 100% = 30%
=> y = 3
CTHH : Fe2O3 : Sắt (III) oxit
Đúng 1
Bình luận (0)
Một oxit của Sắt có thành phần trăm của Sắt là 70% và Oxi là 30%. Biết oxit này có khối lượng mol phân tử là 160 g/mol. Hãy tìm công thức hóa học của oxit trên.
Giải nhanh giùm mik
Khối lượng của các nguyên tố trong hợp chất là:
\(m_{FE}=\dfrac{70.160}{100}=112\left(g\right)\)
\(m_O=\dfrac{30.160}{100}=48\left(g\right)\)
Số mol có trong mỗi nguyên tố là:
\(n_{FE}=\dfrac{m_{FE}}{M_{FE}}=\dfrac{112}{56}=2\left(mol\right)\)
\(n_O=\dfrac{m_O}{M_O}=\dfrac{48}{16}=3\left(mol\right)\)
Vậy hợp chất có 2 nguyên tử Fe, 3 nguyên tử O
Công thức hóa học của hợp chất là: \(FE_2O_3\)
Đúng 3
Bình luận (0)
\(m_{Fe}=\dfrac{160.70}{100}=112g\\ m_O=160-112=48g\\ n_{Fe}=\dfrac{112}{56}=2mol\\n_O=\dfrac{48}{16}=3mol\\ \Rightarrow CTHH:Fe_2 O_3\)
Đúng 2
Bình luận (0)
gọi CT tổng quát là FexOy
mFe:mO=56x:16y
=70:30
=70/56:30/16
=2:3
vậy CTHH là Fe2O3
Đúng 0
Bình luận (0)
Trong 1 phân tử của Oxit sắt chứa 2 loại nguyên tử là sắt và Oxi biết Phân tử khối là 160 đvC. Xác định công thức hóa học của Oxi trên.
Giải hộ mik tick choa
lớp 1 học hóa học à
mình học lớp 6 còn chưa học
Đúng 0
Bình luận (0)
Đỗ Khánh Ly ko biet ten Hà Chí Bảo ngu vcl
Đúng 0
Bình luận (0)
Tìm công thức hóa học của một oxit sắt, có phân tử khối là 160. Biết trong phân tử oxit: sắt chiếm 7 phần, oxi chiếm 3 phần
Đặt CTHH của oxit sắt là FexOy
=> 56x + 16y = 160
Lại có : 56x = M(oxit).0,7 => 56x = 160.0,7 => x = 2
16y = M(oxit).0,3 => 16y = 160.0,3 => y = 3
Vậy CTHH của oxit là Fe2O3
Đúng 0
Bình luận (0)
Oxit X có 22,3% oxi về khối lượng, còn lại là sắt. Biết phân tử khối của X là 72 đvC. Hãy xác định công thức hóa học và tên gọi của X.
Oxit : FexOy
Ta có : 56x + 16y = 72(1)
%O = 16y/(56x + 16y) .100% = 22,3%
=> 56x = 55,749y(2)
Từ (1)(2) suy ra x = y = 1
Vậy : CTHH là FeO(Sắt II oxit)
Đúng 1
Bình luận (0)
1) xác định công thức hóa học của nhôm oxit, biết tỉ lệ khối lượng của 2 nguyên tố nhôm và oxit bằng 9 : 8.2) Một oxít của lưu huỳnh trong đó có oxi chiếm 60 phần trăm về khối lượng. Tìm công thức phân tử của oxit đó?3) Cho 11,2 gam sắt vào 200 ml dung dịch H2SO4 2M. Hãy: a) Tính lượng khí H2 tạo ra ở đktc ? b) Chất nào còn dư sau phản ứng và lượng dư là bao nhiêu ? c) Tính nồng độ của các chất sau phản ứng ?
Đọc tiếp
1) xác định công thức hóa học của nhôm oxit, biết tỉ lệ khối lượng của 2 nguyên tố nhôm và oxit bằng 9 : 8.
2) Một oxít của lưu huỳnh trong đó có oxi chiếm 60 phần trăm về khối lượng. Tìm công thức phân tử của oxit đó?
3) Cho 11,2 gam sắt vào 200 ml dung dịch H2SO4 2M. Hãy:
a) Tính lượng khí H2 tạo ra ở đktc ?
b) Chất nào còn dư sau phản ứng và lượng dư là bao nhiêu ?
c) Tính nồng độ của các chất sau phản ứng ?
1.\(\dfrac{m_{Al}}{m_O}=\dfrac{9}{8}\)
\(Al_xO_y\)
\(x:y=\dfrac{9}{27}:\dfrac{8}{16}=\dfrac{1}{3}:\dfrac{1}{2}=2:3\)
Vậy CTHH là \(Al_2O_3\)
2.\(\rightarrow\%S=100-60=40\%\)
\(S_xO_y\)
\(x:y=\dfrac{40}{32}:\dfrac{60}{16}=1,25:3,75=1:3\)
Vậy CTHH là \(SO_3\)
3.
a.b.
\(n_{Fe}=\dfrac{11,2}{56}=0,2mol\)
\(n_{H_2SO_4}=2.0,2=0,4mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,2 < 0,4 ( mol )
0,2 0,2 0,2 0,2 ( mol )
\(V_{H_2}=0,2.22,4=4,48l\)
Chất dư là H2SO4
\(m_{H_2SO_4\left(dư\right)}=\left(0,4-0,2\right).98=19,6g\)
c.Nồng độ gì bạn nhỉ?
Đúng 1
Bình luận (1)
Cho biết khối lượng mol một oxit của kim loại là 160 g/mol, thành phần về khối lượng của kim loại trong oxit đó là 70%. Lập công thức hóa học của oxit. Gọi tên oxit đó
\(CT:M_xO_y\)
\(\%M=\dfrac{xM}{160}\cdot100\%=70\%\)
\(\Rightarrow xM=112\)
\(\text{Với : }\) \(x=2\Rightarrow M=56\)
\(M=56\cdot2+16y=160\left(g\text{/}mol\right)\)
\(\Rightarrow y=3\)
\(CT:Fe_2O_3:\text{Sắt (III) oxit}\)
Đúng 4
Bình luận (0)
Một loại oxi sắt có thành phần là: 7 phần khối lượng sắt kết hợp với 3 phần khối lượng oxi. Em hãy cho biết: Công thức phân tử của oxit sắt, biết công thức phân tử cũng chính là công thức đơn giản.
Giả sử khối lượng oxit là 10g ⇒ m F e = 7g ; m O = 3g
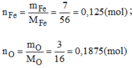
Vậy: 0,125 mol nguyên tử Fe kết hợp với 0,1875 mol nguyên tử O.
Suy ra 2 mol nguyên tử Fe kết hợp với 3 mol nguyên tử O (vì số nguyên tử luôn là số nguyên).
→ Công thức hóa học đơn giản của oxit sắt là: F e 2 O 3
Đúng 0
Bình luận (0)
1 Oxit sắt có phần trăm là 70% và Oxy 30%.Biết Oxi có khối lượng mol phân tử là 160g/mol.Hãy tìm công thức hoá học
\(m_{O_{ }}=\dfrac{160.30\%}{100\%}=48\left(g\right)\)
\(=>n_{O_{ }}=\dfrac{48}{16}=3\left(mol\right)\)
\(m_{Fe}=160-48=112\left(g\right)\)
\(=>n_{Fe}=\dfrac{112}{56}=2\left(mol\right)\)
\(=>CTHH:Fe_2O_3\)
Đúng 1
Bình luận (0)
























