Dẫn 5,61 lít (đ.k.t.c) hỗn hợp 2 khí CO và \(H_2\) từ từ qua hỗn hợp 2 oxit CuO và FeO nung nóng lấy dư, sau phản ứng thấy khối lượng hỗn hợp a giảm a gam
a) Viết các PTHH
b) Tính a
Bài 1: Cho 3,6g một oxit sắt vào dung dịch HCl dư. Sau khi phản ứng xảy ra hoàn toàn thu được một muối sắt clorua. Hãy xác định công thức phân tử của oxit sắt
Bài 2: Dẫn 5,61 lít (đktc) hỗn hợp 2 khí CO và H2 từ từ qua hỗn hợp 2 oxit CuO và FeO nung nóng lấy dư, sau phản ứng thấy khối lượng hỗn hợp giảm a gam
a) Viết các PTHH
b) Tính a
c) Tính % theo thể tích của cá khí, biết tỉ khối hỗn hợp khí so với khí CH4 là 0,4
dẫn 5.6l(đktc)hỗn hợp 2 khí Co và h2 từ từ qua hỗn hợp 2 oxit CUO và FeO nung nóng ,pư xg thấy lim loại hỗn hợp giảm a (G)
a/viết pthh b/tính a
a)
\(FeO + CO \xrightarrow{t^o} Fe + CO_2\\ FeO + H_2 \xrightarrow{t^o} Fe + H_2O\\ CuO + CO \xrightarrow{t^o} Cu + CO_2\\ CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\\)
b) Khối lượng hỗn hợp giảm chính là khối lượng O(oxit) phản ứng .
\(H_2 + O_{oxit} \to H_2O\\ CO + O_{oxit} \to CO_2\\ n_{O(oxit)} = n_{H_2} + n_{CO} = \dfrac{5,6}{22,4} = 0,25(mol)\\ \Rightarrow a = m_O = 0,25.16 = 4(gam)\)
Dẫn 13.44 lít hỗn hợp khí (ĐKTC) CO và H2 từ từ qua hỗn hợp hai oxit CuO và PbO nung nóng ,sau phản ứng thấy khối lượng hỗn hợp giảm a gam.
a) viết PTHH xảy ra
b) tính a
CuO + CO => Cu + CO2
PbO + CO => Pb + CO2
CuO + H2 => Cu + H2O
PbO + H2 => Pb + H2O
n khí = nCO + nH2 = V/22.4 = 13.44/22.4 = 0.6 (mol)
Theo ĐLBTKL:
mCuO + mPbO + m khí = mCu + mPb + mH2O + mCO2
Vì khi phản ứng kết thúc => lượng khí CO2 thoát ra => khối lượng hh giảm
mCO2 = n.M = a
nCO2 = nCO (Mà nH2 + nCO = 0.6)
Đề có thiếu gì không nhỉ
Thổi từ từ V lít hỗn hợp khí (đktc) gồm CO và H2 đi qua ống đựng 16,8 gam hỗn hợp 3 oxit CuO, Fe3O4, Al2O3 nung nóng, phản ứng hoàn toàn. Sau phản ứng thu được m gam chất rắn và một hỗn hợp khí nặng hơn khối lượng của hỗn hợp V là 0,32 gam. Tính V và m
A. 0,224 lít và 14,48 gam
B. 0,672 lít và 18,46 gam
C. 0,112 lít và 12,28 gam
D. 0,448 lít và 16,48 gam
Đáp án D.
Ta có: mO = 0,32 (g) ⟹ nO = 0 , 32 16 = 0,02 (mol) nên số mol của hỗn hợp CO, H2 cũng bằng 0,02 (mol) ⟹ V = 0,02.22,4 = 0,448 (l).
Theo định luật bảo toàn khối lượng, m = 16,8 – 0,02.16 = 16,48 (g).
Dẫn 11,2 lít hỗn hợp khí CO và H2(đktc) từ từ qua hỗn hợp 2 oxit CuO và FeO nung nóng lấy dư, sau phản ứng thấy khối lượng hỗn hợp chât rắn giảm a gam
a)Tính % theo thể tích của các khí có trong hỗn hợp, biết tỉ khối của hỗn hợp khí so với khí oxi là 0,55
b)Tính a
a/ Gọi số mol của CO và H2 lần lược là x, y thì ta có
\(n_{hhk}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(x+y=0,5\left(1\right)\)
Tỉ khối của hỗn hợp khí so với khí oxi là 0,55.
\(\Rightarrow\dfrac{28x+2y}{x+y}=0,55.32=17,6\)
\(\Leftrightarrow3y=2x\left(2\right)\)
Từ (1) và (2) ta có hệ: \(\left\{{}\begin{matrix}x+y=0,5\\3y=2x\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=0,3\\y=0,2\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CO}=\dfrac{0,3}{0,5}.100\%=60\%\\\%V_{H_2}=100\%-60\%=40\%\end{matrix}\right.\)
b/ Khối lượng chất rắn giảm đi đúng bằng khối lượng O thêm vào để tạo CO2, H2O.
\(\Rightarrow n_O=0,5\left(mol\right)\)
\(\Rightarrow a=0,5.16=8\left(g\right)\)
Dẫn luồng khí H 2 dư đi qua 16 g hỗn hợp hai oxit CuO và F e 2 O 3 . nung nóng. Sau phản ứng để nguội, cân lại thấy khối lượng hỗnn hợp giảm 25%. Tính phần trăm khối lượng của mỗi oxit trong hỗn hợp ban đầu.
Phương trình hóa học:
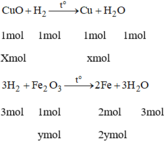
Gọi x là số mol của CuO
y là số mol của F e 2 O 3 .
Ta có: 80x + 160y = 16 (1)
Khối lượng hỗn hợp giảm do oxit tạo thành kim loại:
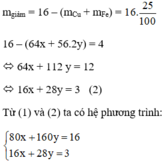
Giải hệ phương trình ta được:
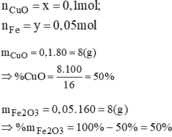
Dẫn a mol hỗn hợp X (gồm hơi nước và khí CO 2 ) qua cacbon nung đỏ, thu được 1,8a mol hỗn hợp khí Y gồm H 2 , CO và CO 2 . Cho Y đi qua ống đựng hỗn hợp gồm CuO và Fe 2 O 3 (dư, nung nóng), sau khi các phản ứng xảy ra hoàn toàn, khối lượng chất rắn giảm 1,28 gam. Giá trị của a là
A. 0,10.
B. 0,04.
C. 0,05.
D. 0,08.
Chọn C
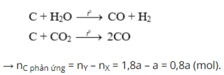
Theo bài ra có khối lượng chất rắn giảm chính bằng khối lượng O bị lấy ra khỏi oxit.
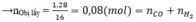
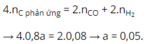
Bảo toàn electron:
dẫn luồng khí H2 dư đi qua 20g hỗn hợp hai oxit Fe2O3 và CuO nung nóng. Sau phản ứng để nguội , cân lại thấy khối lượng hôn hợp giảm 24%. tính phần trăm khối lượng của CuO
$m_{O\ trong\ oxit} = m_{giảm} = 20.24\%= 4,8(gam)$
$\Rightarrow n_O = \dfrac{4,8}{16} = 0,3(mol)$
Gọi $n_{Fe_2O_3} = a(mol) ; n_{CuO} = b(mol) \Rightarrow 160a + 80b = 20(1)$
Ta có : $n_O = 3a + b = 0,3(2)$
Từ (1)(2) suy ra : a = 0,05 ; b = 0,15
$\%m_{CuO} = \dfrac{0,15.80}{20}.100\% = 60\%$
dẫn từ từ V liít hỗn họp X (đktc) gồm CO và H2 qua ống dẫn chứa hỗn hợp gồm CuO,Fe2O3, Fe3O4 nung nóng. Phản ứng hoàn toàn thu được hỗn hợp khí và hơi có khối lượng nặng hơn hỗn hợp khí ban đầu là 0,32gam. viết PTHH xảy ra và tính V
m(tăng) = mO = 0,32 (g)
nO = 0,32/16 = 0,02 (mol)
=> nhh khí = 0,02 (mol)
=> Vhh khí = 0,02 . 22,4 = 0,448 (l)