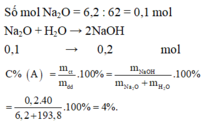Hòa tan 6,2 g natri oxit vào193,8 g nước thì được dung dịch A. Nồng độ % của dung dịch A là? ( Na =23 , O=16 , H=1 )

Những câu hỏi liên quan
Hòa tan 6,2 g natri oxit vào193,8 g nước thì được dung dịch A. Nồng độ % của dung dịch A là? ( Na =23 , O=16 , H=1 )
\(n_{Na_2O}=\dfrac{6,2}{62}=0,1(mol)\\ PTHH:Na_2O+H_2O\to 2NaOH\\ \Rightarrow n_{NaOH}=0,2(mol)\\ \Rightarrow m_{CT_{NaOH}}=0,2.40=8(g)\\ \Rightarrow C\%_{NaOH}=\dfrac{8}{6,2+193,8}.100\%=4\%\)
Đúng 1
Bình luận (0)
\(n_{Na_2O}=\dfrac{m}{M}=\dfrac{6,2}{39}=0,1\) ( mol )
Na2O + H2O → 2NaOH
0,1 → 0,2 ( mol )
⟹ mNaOH = nNaOH. MNaOH = 0,2. 40 = 8 (g)
Khối lượng dung dịch sau là:
mdd sau = \(m_{Na_2O}+m_{H_2O}\) = 6,2 + 193,8 = 200 (g)
dung dịch A thu được là dung dịch NaOH
⇒ C%NaOH = ( mNaOH : m dd sau pư ) . 100% =( 8 : 200 ) .100% = 4%
Do mik bấm phân số không được nên mik để phép chia nha
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
1. Hoà tan 6,2 g natri oxit vào 193,8 g nước thì được dung dịch A. Tính nồng độ phần trăm của dung dịch A.2. Hoà tan 23,5 g kali oxit vào nước được 0,5 lít dung dịch A. Tính nồng độ mol của dung dịch A.3. Hòa tan hết 12,4 gam natrioxit vào nước thu được 500ml dung dịch A . Tính nồng độ mol của dung dịch A.4. Hòa tan 12,6 gam natri sunfit vào dung dịch axit clohidric dư. Thể tích khí SO2 thu được ở đktc.5. Hòa tan hết 5,6 gam CaO vào dung dịch HCl 14,6% . Tính khối lượng dung...
Đọc tiếp
1. Hoà tan 6,2 g natri oxit vào 193,8 g nước thì được dung dịch A. Tính nồng độ phần trăm của dung dịch A.
2. Hoà tan 23,5 g kali oxit vào nước được 0,5 lít dung dịch A. Tính nồng độ mol của dung dịch A.
3. Hòa tan hết 12,4 gam natrioxit vào nước thu được 500ml dung dịch A . Tính nồng độ mol của dung dịch A.
4. Hòa tan 12,6 gam natri sunfit vào dung dịch axit clohidric dư. Thể tích khí SO2 thu được ở đktc.
5. Hòa tan hết 5,6 gam CaO vào dung dịch HCl 14,6% . Tính khối lượng dung dịch HCl đã dùng.
Cho em xin cách giải chi tiết ạ em cảm ơn :DD
1)
$n_{Na_2O} = \dfrac{6,2}{62} = 0,1(mol)$
$Na_2O + H_2O \to 2NaOH$
$n_{NaOH} = 2n_{Na_2O} = 0,2(mol)$
$m_{dd} = 6,2 + 193,8 = 200(gam) \Rightarrow C\%_{NaOH} = \dfrac{0,2.40}{200}.100\% = 4\%$
2)
$n_{K_2O} = \dfrac{23,5}{94} = 0,25(mol)$
$K_2O + H_2O \to 2KOH$
$n_{KOH} = 2n_{K_2O} = 0,5(mol) \Rightarrow C_{M_{KOH}} = \dfrac{0,5}{0,5} = 1M$
3) $n_{Na_2O} = \dfrac{12,4}{62} = 0,2(mol)$
$Na_2O + H_2O \to 2NaOH$
$n_{NaOH} = 2n_{Na_2O} = 0,4(mol)$
$C_{M_{NaOH}} = \dfrac{0,4}{0,5} =0,8M$
Đúng 3
Bình luận (1)
4)
$Na_2SO_3 + 2HCl \to 2NaCl +S O_2 + H_2O$
Theo PTHH :
$n_{SO_2} = n_{Na_2SO_3} = \dfrac{12,6}{126} = 0,1(mol)$
$V_{SO_2} = 0,1.22,4 = 2,24(lít)$
5) $n_{CaO} = \dfrac{5,6}{56} = 0,1(mol)$
$CaO + 2HCl \to CaCl_2 + H_2O$
Theo PTHH :
$n_{HCl} = 2n_{CaO} = 0,2(mol) \Rightarrow m_{dd\ HCl} = \dfrac{0,2.36,5}{14,6\%} = 50(gam)$
Đúng 3
Bình luận (1)
Bài 1 :
\(n_{Na2O}=\dfrac{6,2}{62}=0,1\left(mol\right)\)
Pt : \(Na_2O+H_2O\rightarrow2NaOH|\)
1 1 2
0,1 0,2
\(n_{NaOH}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
⇒ \(m_{NaOH}=0,2.40=8\left(g\right)\)
\(m_{ddspu}=6,2+193,8=200\left(g\right)\)
\(C_{ddNaOH}=\dfrac{8.100}{200}=4\)0/0
Chúc bạn học tốt
Đúng 2
Bình luận (1)
Xem thêm câu trả lời
Hoà tan 6,2 g natri oxit vào 193,8 g nước thì được dung dịch A. Nồng độ phần trăm của dung dịch A là:
A. 4%.
B. 6%.
C. 4,5%
D. 10%
hòa tan hết 12,4 gam Natri oxit (Na2O) vào nước thu được 500ml dung dịch NaOH Tính nồng độ mol của dung dịch bazơ thu được. (Biết Na=23, O=16
\(n_{Na_2O}=\dfrac{12,4}{62}=0,2mol\)
\(Na_2O+H_2O\rightarrow2NaOH\)
0,2 \(\rightarrow\) 0,2 \(\rightarrow\) 0,4
\(C_{M_{NaOH}}=\dfrac{0,4}{\dfrac{500}{1000}}=0,8M\)
Đúng 1
Bình luận (0)
Bài 2:
Cho 9,4 g kali oxit tan hết trong 150,6 g nước được dung dịch A. Tính nồng độ % của A. Tính thể tích dung dịch HCl 0,5M cần dùng để tác dụng vừa đủ với dung dịch A.
Bài 3:
Hòa tan 23,5 g kali oxit vào 176,5 g nước được dung dịch A. Trung hòa vừa đủ A bằng dung dịch H2SO4 20% được dung dịch B. Tính:
a/ Nồng độ % dung dịch A. (14%)
b/ Khối lượng dung dịch H2SO4 cần dùng. (122,5g)
c/ Nồng độ % của muối trong dung dịch B. (13,49%)
Cho: H 1 ; O 16 ; Na 23 ; S 32 ; Cl 35...
Đọc tiếp
Bài 2:
Cho 9,4 g kali oxit tan hết trong 150,6 g nước được dung dịch A. Tính nồng độ % của A. Tính thể tích dung dịch HCl 0,5M cần dùng để tác dụng vừa đủ với dung dịch A.
Bài 3:
Hòa tan 23,5 g kali oxit vào 176,5 g nước được dung dịch A. Trung hòa vừa đủ A bằng dung dịch H2SO4 20% được dung dịch B. Tính:
a/ Nồng độ % dung dịch A. (14%)
b/ Khối lượng dung dịch H2SO4 cần dùng. (122,5g)
c/ Nồng độ % của muối trong dung dịch B. (13,49%)
Cho: H = 1 ; O = 16 ; Na = 23 ; S = 32 ; Cl = 35,5 ; K = 39
Câu 1:
\(n_{K2O}=\frac{9,4}{39.2+16}=0,1\left(mol\right)\)
\(K_2O+H_2O\rightarrow2KOH\)
0,1_____________0,2
\(C\%_{KOH}=\frac{0,2.\left(39+17\right)}{150,6+9,4}.100\%=7\%\)
\(KOH+HCl\rightarrow KCl+H_2O\)
0,2______0,2__________________
\(\Rightarrow V_{dd_{HCl}}=\frac{0,2}{0,5}=0,5\left(l\right)\)
Câu 2:
a, \(n_{K2O}=\frac{23,5}{39.2+16}=0,25\left(mol\right)\)
\(2n_{K2O}=n_{KOH}\Rightarrow n_{KOH}=0,25.2=0,5\left(mol\right)\)
\(C\%_{KOH}=\frac{0,5.\left(39+17\right)}{176,5+23,5}.100\%=14\%\)
b, \(n_{KOH}=2n_{K2SO4}\Rightarrow n_{K2SO4}=\frac{0,5}{2}=0,25\)
\(n_{H2SO4}=n_{K2SO4}=0,25\)
\(m_{dd_{H2SO4}}=\frac{0,25.98}{20\%}=122,5\left(g\right)\)
c,
mdd sau phản ứng=mddA+mddH2SO4
m dd sau phản ứng \(=23,5+176,5+122,5=322,5\)
\(C\%_{K2SO4}=\frac{0,25.\left(39.2+32+16.4\right)}{322,5}.100\%=13,49\%\)
giúp e vs
Câu 32: Cho 31gam natri oxit Na2O tác dụng với nước, thu được 0,5 lít dung dịch bazơ. Tính nồng độ mol của dung dịch bazơ thu được.(Na=23, O=16, H=1)
Ta có: \(n_{Na_2O}=\dfrac{31}{62}=0,5\left(mol\right)\)
\(PTHH:Na_2O+H_2O--->2NaOH\)
Theo PT: \(n_{NaOH}=2.n_{Na_2O}=2.0,5=1\left(mol\right)\)
\(\Rightarrow C_{M_{NaOH}}=\dfrac{1}{0,5}=2M\)
Đúng 3
Bình luận (0)
`Na_2O + H_2O -> 2NaOH`
`n_{Na_2O} = (31)/(62) = 0,5` `mol`
`n_{NaOH} = 2 . n_{Na_2O} = 1` `mol`
`C_{M_(NaOH)} = 1/(0,5) = 2` `M`
Đúng 1
Bình luận (1)
hòa tan hết 6,2 natri oxit vào nước thu đc 400 ml dung dịch A. Nồng độ mol của dd A bằng
\(n_{Na_2O}=\dfrac{6,2}{62}=0,1\left(mol\right)\\ Na_2O+H_2O\rightarrow2NaOH\\ C_{MddA}=C_{MddNaOH}=\dfrac{0,2}{0,4}=0,5\left(M\right)\)
Đúng 0
Bình luận (0)
Hòa tan 18,6 gam Na2O vào nước tạo thành 600ml dung dịch Natri hidroxit ( NaOH) a) Tính nồng độ mol của dung dịch thu được b) Tính thể tích dung dịch HCl 20% ( D 1,05 g/ml ) cần để trung hòa dung dịch trên. Các bạn giải thích kĩ câu ( b ) hộ mình, mình không hiểu câu này cho lắm . ( Cho biết : Na 23 ; O 16 ; H 1 ; Cl 35,5 )P/s : Xin cảm ơn các bạn rất nhiều ^.^
Đọc tiếp
Hòa tan 18,6 gam Na2O vào nước tạo thành 600ml dung dịch Natri hidroxit ( NaOH)
a) Tính nồng độ mol của dung dịch thu được
b) Tính thể tích dung dịch HCl 20% ( D = 1,05 g/ml ) cần để trung hòa dung dịch trên. => Các bạn giải thích kĩ câu ( b ) hộ mình, mình không hiểu câu này cho lắm >.<
( Cho biết : Na = 23 ; O = 16 ; H = 1 ; Cl = 35,5 )
P/s : Xin cảm ơn các bạn rất nhiều ^.^
a, \(n_{Na_2O}=\frac{18,6}{62}=0,3\left(mol\right)\)
600 ml = 0,6 l
\(Na_2O+H_2O->2NaOH\) (1)
theo (1) \(n_{NaOH}=2n_{Na_2O}=0,6\left(mol\right)\)
nồng độ mol của dung dịch thu được là
\(\frac{0,6}{0,6}=1M\)
Đúng 0
Bình luận (0)
nNa2O = \(\frac{18,6}{62}=0,3\left(mol\right)\)
Đổi 600ml = 0,6 l
\(Na_{2_{ }}O+H_{2_{ }}O\rightarrow2NaOH\)
0,3mol 0,6 mol
Nồng độ mol của dung dịch sau phản ứng là:
CM = \(\frac{0,6}{0,6}=1\left(M\right)\)
Đúng 0
Bình luận (0)
Cho 12,4g natri oxit vào 200g nước. Tính nồng độ phần trăm natri hiđroxit trong dung dịch thu được. Biết Na=23, H=1; O=16
Nồng độ phần trăm của dung dịch NaOH thu được:
\(C\%dd_{NaOH}=\dfrac{m_{NaOH}}{m_{ddNaOH}}.100\%=\dfrac{12,4}{12,4+200}.100\approx5,838\%\)
Đúng 0
Bình luận (0)
mddNaOH=12,4+200=212,4(g)
ta có: C%=mNaOH/mddNaOH×100%
=12,4÷212,4×100%=5,838%
Đúng 0
Bình luận (0)
Ta có:
\(m_{ct}=12,4\left(g\right)\)
\(m_{H_20}=200\left(g\right)\)
- Khối lượng dung dịch NaOH:
\(m_{dd}=m_{ct}+m_{H_2O}\)
\(=12,4+200=212,4\left(g\right)\)
- Nồng độ phần trăm NaOH trong dung dịch thu được:
C%=\(\dfrac{m_{ct}}{m_{dd}}\cdot100\%\)
=\(\dfrac{12,4}{212,4}\cdot100\%\)
\(\approx\)\(5,838\%\)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời