Mắc nối tiếp 2 bình điện phân: bình A đựng dung dịch C u S O 4 và anot bằng đồng, bình B đựng dung dịch A g N O 3 và anot bằng Ag. Sau 1 giờ lượng đồng bám vào catot của bình A là 0,64g. Tính khối lượng kim loại bám vào catot của bình B sau 1 giờ

Những câu hỏi liên quan
Một bộ nguồn điện gồm 30 pin mắc thành ba nhóm nối tiếp, mỗi nhóm có 10 pin mắc song song; mỗi pin có suất điện động Eo và điện trở trong r 0,6Ω. Mắc một bình điện phân đựng dung dịch
CuSO
4
có điện trở R 205Ω vào hai cực của bộ nguồn nói trên. Biết anot của bình điện phân bằng đồng và sau 50 phút có 0,013g đồng bám vào caot. Suất điện động
E
o
bằng A. 9V B. 30V C. 0,9V ...
Đọc tiếp
Một bộ nguồn điện gồm 30 pin mắc thành ba nhóm nối tiếp, mỗi nhóm có 10 pin mắc song song; mỗi pin có suất điện động Eo và điện trở trong r = 0,6Ω. Mắc một bình điện phân đựng dung dịch CuSO 4 có điện trở R = 205Ω vào hai cực của bộ nguồn nói trên. Biết anot của bình điện phân bằng đồng và sau 50 phút có 0,013g đồng bám vào caot. Suất điện động E o bằng
A. 9V
B. 30V
C. 0,9V
D. 27V
Một bộ nguồn điện gồm 30 pin mắc thành ba nhóm nối tiếp, mỗi nhóm có 10 pin mắc song song; mỗi pin có suất điện động
E
0
và điện trở trong
r
0
,
6
Ω
. Mắc một bình điện phân đựng dung dịch
C
u
S
O
4
có điện trở
R
25
Ω
vào hai cực của bộ nguồn nói trên. Biết...
Đọc tiếp
Một bộ nguồn điện gồm 30 pin mắc thành ba nhóm nối tiếp, mỗi nhóm có 10 pin mắc song song; mỗi pin có suất điện động E 0 và điện trở trong r = 0 , 6 Ω . Mắc một bình điện phân đựng dung dịch C u S O 4 có điện trở R = 25 Ω vào hai cực của bộ nguồn nói trên. Biết anot của bình điện phân bằng đồng và sau 50 phút có 0,013g đồng bám vào catot. Suất điện động E 0 bằng
A. 9V
B. 30V
C. 0,9V
D. 27V
Đáp án: C
Ta có:
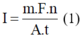
Mặt khác

Từ (1) và (2) ta xác định được: ξ 0 = 0 , 9 V .
Đúng 0
Bình luận (0)
Mắc nối tiếp 2 bình điện phân, bình A đựng dung dịch chứa 0,2 mol CuSO4, bình B đựng dung dịch chứa 0,15 mol NaCl. Điện phân cho đến khi catot bình A bắt đầu xuất hiện bọt khí thì dừng lại. Tính thể tích khí ở catot bình B (đo ở đktc).
A. 1,68 lít
B. 3,36 lít
C. 4,48 lít
D. 5,6 lít
Bình điện phân thứ nhất có anot bằng bạc nhúng trong dung dịch
A
g
N
O
3
, bình điện phân thứ hai có anot bằng đồng nhúng trong dung dịch
C
u
S
O
4
. Hai bình được mắc nối tiếp nhau vào một mạch điện. Sau 1,5 giờ, tổng khối lượng của hai catot tăng lên 2,1g. Cho biết
A
A
g
108...
Đọc tiếp
Bình điện phân thứ nhất có anot bằng bạc nhúng trong dung dịch A g N O 3 , bình điện phân thứ hai có anot bằng đồng nhúng trong dung dịch C u S O 4 . Hai bình được mắc nối tiếp nhau vào một mạch điện. Sau 1,5 giờ, tổng khối lượng của hai catot tăng lên 2,1g. Cho biết A A g = 108 ; n A g = 1 ; A C u = 64 ; n C u = 2 . Khối lượng m 1 bạc bám vào bình thứ nhất và khối lượng m2 đồng bám vào bình thứ hai lần lượt là
A. 1,62g; 0,48g
B. 10,48g; 1,62g
C. 32,4g ; 9,6g
D. 9,6g; 32,4g
Đáp án: A
Khối lượng m 1 bạc bám vào bình thứ nhất và khối lượng m 2 đồng bám vào bình thứ hai lần lượt là:
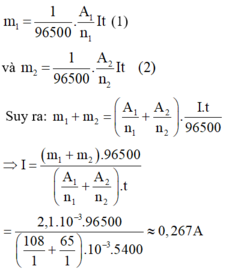
Thay I vào (1) và (2) ta có: m 1 = 1,62g; m 2 = 0,48g.
Đúng 0
Bình luận (0)
Bình điện phân thứ nhất có anot bằng bạc nhúng trong dung dịch
AgNO
3
, bình điện phân thứ hai có anot bằng đồng nhúng trong dung dịch
CuSO
4
. Hai bình được mắc nối tiếp nhau vào một mạch điện. Sau 1,5 giờ, tổng khối lượng của hai catot tăng lên 2,1g. Cho biết
A
Ag
108;
n
Ag
1;
A
Cu...
Đọc tiếp
Bình điện phân thứ nhất có anot bằng bạc nhúng trong dung dịch AgNO 3 , bình điện phân thứ hai có anot bằng đồng nhúng trong dung dịch CuSO 4 . Hai bình được mắc nối tiếp nhau vào một mạch điện. Sau 1,5 giờ, tổng khối lượng của hai catot tăng lên 2,1g. Cho biết A Ag = 108; n Ag = 1; A Cu = 64; n Cu = 2. Khối lượng m 1 bạc bám vào bình thứ nhất và khối lượng m 2 đồng bám vào bình thứ hai lần lượt là
A. 1,62g; 0,48g
B. 10,48g; 1,62g
C. 32,4g ; 9,6g
D. 9,6g; 32,4g
Đáp án A
Khối lượng m 1 bạc bám vào bình thứ nhất và khối lượng m 2 đồng bám vào bình thứ hai lần lượt là:
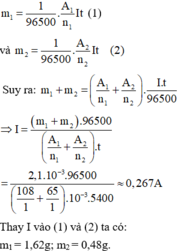
Đúng 0
Bình luận (0)
Một bộ nguồn điện gồm 30 pin mắc thành 3 nhóm nối tiếp, mỗi nhóm có 10 pin mắc song song; mỗi pin có suất điện động 0,9 V và điện trở trong
0
,
6
Ω
. Một bình điện phân đựng dung dịch
C
u
S
O
4
có điện trở
205
Ω
được mắc vào hai cực của bộ nguồn nói trên. Anôt của bình điện phân bằng đồng. Tính khối lượng đồng bám vào catôt của bình trong thời gian 50 phút. Bi...
Đọc tiếp
Một bộ nguồn điện gồm 30 pin mắc thành 3 nhóm nối tiếp, mỗi nhóm có 10 pin mắc song song; mỗi pin có suất điện động 0,9 V và điện trở trong 0 , 6 Ω . Một bình điện phân đựng dung dịch C u S O 4 có điện trở 205 Ω được mắc vào hai cực của bộ nguồn nói trên. Anôt của bình điện phân bằng đồng. Tính khối lượng đồng bám vào catôt của bình trong thời gian 50 phút. Biết đồng có khối lượng mol nguyên tử là A = 64 g/mol và hoá trị n = 2.
Ta có: E b = 3 e = 2 , 7 V ; r b = 3 . r 10 = 0 , 18 Ω ;
I = E b R + r b = 0 , 01316 A ; m = 1 F . A n . I t = 0 , 013 g
Đúng 0
Bình luận (0)
Cho hai bình điện phân, bình (1) đựng 20 ml dung dịch NaOH 1,73M; bình (2) đựng dung dịch gồm 0,225 mol
C
u
N
O
3
2
và 0,2 mol HCl. Mắc nối tiếp bình (1) và bình (2). Điện phân các dung dịch bằng dòng điện một chiều với cường độ dòng điện không đổi một thời gian. Khi dừng điện phân, tháo ngay catot ở các bình. Sau phản ứng thấy nồng độ NaOH ở bình...
Đọc tiếp
Cho hai bình điện phân, bình (1) đựng 20 ml dung dịch NaOH 1,73M; bình (2) đựng dung dịch gồm 0,225 mol C u N O 3 2 và 0,2 mol HCl. Mắc nối tiếp bình (1) và bình (2). Điện phân các dung dịch bằng dòng điện một chiều với cường độ dòng điện không đổi một thời gian. Khi dừng điện phân, tháo ngay catot ở các bình. Sau phản ứng thấy nồng độ NaOH ở bình (1) là 2M, Cho tiếp 14 gam bột Fe vào bình (2) đến khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn không tan. Biết NO là sản phẩm khử duy nhất N + 5 khối lượng riêng của nước là 1 g/ml. Giá trị m là
A. 9,8
B. 10,4
C. 8,3
D. 9,4
Cho hai bình điện phân, bình (1) đựng 20 ml dung dịch NaOH 1,73 M; bình (2) đựng dung dịch gồm 0,225 mol Cu(NO3)2 và 0,2 mol HCl. Mắc nối tiếp bình (1) và Bình (2). Điện phân các dung dịch bằng dòng điện một chiều với cường độ dòng điện không đổi một thời gian. Khi dừng điện phân, tháo ngay catot ở các bình. Sau phản ứng thấy nồng độ NaOH ở bình (1) là 2M, Cho tiếp 14 gam bột Fe vào bình (2) đến khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn không tan. Biết NO là sản phẩm khử duy nhất N+5...
Đọc tiếp
Cho hai bình điện phân, bình (1) đựng 20 ml dung dịch NaOH 1,73 M; bình (2) đựng dung dịch gồm 0,225 mol Cu(NO3)2 và 0,2 mol HCl. Mắc nối tiếp bình (1) và Bình (2). Điện phân các dung dịch bằng dòng điện một chiều với cường độ dòng điện không đổi một thời gian. Khi dừng điện phân, tháo ngay catot ở các bình. Sau phản ứng thấy nồng độ NaOH ở bình (1) là 2M, Cho tiếp 14 gam bột Fe vào bình (2) đến khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn không tan. Biết NO là sản phẩm khử duy nhất N+5. Giá trị m là:
A. 9,8
B. 10,4
C. 8,3
D. 9,4
Giải thích: Đáp án C
+ Bình 1: nNaOH=0,0346 mol
Sau khi x mol H2O bị điện phân thì thể tích dung dịch còn lại là 20-18x (ml)
=> CM=0,0346/[(20-18x)/1000] = 2
=> x=0,15
=> ne = 2x = 0,3
Bình 2:
Tại catot:
Cu2+ +2e → Cu
0,15.....0,3
Cu2+ dư 0,225-0,15=0,075 mol
Tại anot:
Cl- -1e → 0,5 Cl2
0,2→0,2
H2O – 2e → 0,5O2 + 2H+
0,1 → 0,1
Dung dịch trong bình 2 sau điện phân gồm: 0,075 mol Cu2+; H+: 0,2+0,1=0,3 mol
Khi cho 0,25 mol Fe vào:
3Fe + 8H+ + 2NO3- → 3Fe2+ + 2NO + 4H2O
Bđ: 0,25 0,3 0,45
Pư: 0,1125← 0,3 →0,075
Sau: 0,1375
Fe + Cu2+ → Fe2+ + Cu
Bđ:0,1375 0,075
Pư:0,075 ← 0,075 →0,075
Sau:0,0625 0,075
=> m chất rắn = 0,0625.56+0,075.64=8,3 gam
Đúng 0
Bình luận (0)
Cho bình điện phân đựng dung dịch
C
u
S
O
4
có anot bằng đồng. Biết điện trở của bình là
4
Ω
và hiệu điện thế 2 đầu bình điện phân là 40V. Cho biết A 64, n 2,
D
8
,
9.10
3
k
g
/
m
3
, S 400cm2.a, Tính khối lượng...
Đọc tiếp
Cho bình điện phân đựng dung dịch C u S O 4 có anot bằng đồng. Biết điện trở của bình là 4 Ω và hiệu điện thế 2 đầu bình điện phân là 40V. Cho biết A = 64, n = 2, D = 8 , 9.10 3 k g / m 3 , S = 400cm2.
a, Tính khối lượng đồng bám vào katot sau 32 phút 10 giây.
b, Tính bề dày của kim loại bám vào katot.
c, Tính công suất tiêu thụ mạch ngoài









