Viết các phương trình hoá học của các phản ứng sau (ghi rõ điều kiện, nếu có).
KClO 3 → t ° A + B
A + H 2 O → D + E + F
D + E → KCl + KClO + H 2 O
Viết các phương trình hoá học của các phản ứng sau (ghi rõ điều kiện, nếu có).
KClO 3 → t ° A + B
A + H 2 O → D + E + F
D + E → KCl + KClO + H 2 O
2 KClO 3 → t ° 2KCl + 3 O 2
2KCl + 2 H 2 O → 2KOH + H 2 + Cl 2
Cl 2 + 2KOH → KCl + KClO + H 2 O
Viết phương trình hoá học các phản ứng theo sơ đồ sau, ghi rõ điều kiện của phản ứng (nếu có):
CH2=CH2 → CH3CH2OH → CH3COOC2H5.
\(CH_2=CH_2+H_2O\rightarrow\left(H_2SO_4,t^o\right)CH_3CH_2OH\\ CH_3CH_2OH+CH_3COOH⇌\left(H^+,t^o\right)CH_3COOC_2H_5+H_2O\)
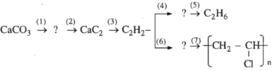
Viết phương trình hoá học của phản ứng thực hiện các biến hoá dưới đây và ghi rõ điều kiện phản ứng (nếu có).
Viết phương trình hoá học của các phản ứng sau (ghi rõ điều kiện phản ứng, nếu có) :
H 2 + A → B
B + Mn O 2 → A + C + D
A + C → B + E
H 2 + Cl 2 → 2HCl
4HCl + Mn O 2 → Cl 2 + 2 H 2 O + Mn Cl 2
Cl 2 + H 2 O → HCl + HClO
Viết các phương trình hoá học của các phản ứng sau (ghi rõ điều kiện phản ứng, nếu có) :
Cl 2 + A → B
B + Fe → C + H 2
C + E → F + NaCl
F + B → C + H 2 O
Cl 2 + H 2 → 2HCl
2HCl + Fe → Fe Cl 2 + H 2
Fe Cl 2 + 2NaOH → Fe OH 2 + 2NaCl
Fe OH 2 + 2HCl → Fe Cl 2 + 2 H 2 O
Viết các phương trình hoá học thực hiện dãy chuyển hoá sau Entylen -> rượu etylic -> axit axitic -> entyl axetat (ghi rõ điều kiện phản ứng )
C2H4+H2O-170,H+>C2H5OH
C2H5OH+O2 -men,to,xt->CH3COOH+H2O
CH3COOH+C2H5OH-H2SO4đ,to->CH3COOC2H5+H2O
CH3COOC2H5 +NaOH->CH3COONa+C2H5OH
*ko đăng lại ạ
Viết phương trình hoá học của phản ứng thực hiện các biến hoá dưới đây, ghi rõ điều kiện của từng phản ứng.
Tinh bột → ( 1 ) Glucozơ → ( 2 ) Ancol etylic → ( 3 ) Anđehit axetic
Từ kim loại đồng, nước, muối ăn NaCl, các thiết bị và dung cụ có đủ. Hãy viết các phương trình phản ứng hoá học (ghi rõ điều kiện nếu có) để điều chế Cu(OH)2.
\(2NaCl+2H_2O\xrightarrow[có.màng.ngăn]{điện.phân}H_2+Cl_2+2NaOH\)
\(2H_2O\overset{t^o}{--->}2H_2+O_2\)
\(2Cu+O_2\overset{t^o}{--->}2CuO\)
\(H_2+Cl_2\overset{t^o}{--->}2HCl\)
\(2HCl+CuO--->CuCl_2+H_2O\)
\(CuCl_2+2NaOH--->2NaCl+Cu\left(OH\right)_2\downarrow\)

ĐỀ KIỂM TRA - HÓA HỌC 10
Câu 1: Bằng phương pháp hoá học hãy phân biệt các dung dịch không màu sau:
NaOH, HCl, NaCl, NaNO3, NaBr
Câu 2: Viết phương trình phản ứng thực hiện dãy biến hoá sau (ghi rõ điều kiện nếu có):
KMnO4 → Cl2 → NaCl → Cl2 → Br2 → I2
Câu 3: Cho 11,1 gam hỗn hợp gồm Al và Fe tác dụng vừa đủ với dung dịch HCl 14,6% thu được 6,72 lít khí H2 (đktc).
a) Tính thành phần phần trăm khối lượng các kim loại trong hỗn hợp trên.
b) Tính nồng độ phần trăm các muối trong dung dịch sau phản ứng.
Câu 4: Cho a gam dung dịch HCl C% tác dụng hết với một lượng hỗn hợp 2 kim loại Na dư và K dư, thấy khối lượng H2 bay ra là 0,05a gam.Tìm C%.
Câu 3 :
\(a) n_{Al} = a(mol) ; n_{Fe} = b(mol) \Rightarrow 27a + 56b =1 1,1(1)\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ n_{H_2} = 1,5a + b = \dfrac{6,72}{22,4} = 0,3(2)\\ (1)(2) \Rightarrow a = 0,1 ; b = 0,15\\ \%m_{Al} = \dfrac{0,1.27}{11,1}.100\% = 24,32\%\\ \%m_{Fe} = 100\% -24,32\% = 75,68\%\)
\(b) n_{HCl} = 2n_{H_2} = 0,3.2 = 0,6(mol)\\ \Rightarrow m_{dd\ HCl} = \dfrac{0,6.36,5}{14,6\%} = 150(gam)\\ m_{dd\ sau\ pư} = m_{hỗn\ hợp} + m_{dd\ HCl} - m_{H_2} = 11,1 + 150 - 0,3.2 = 160,5(gam)\\ n_{AlCl_3} = a = 0,1(mol)\ ;\ n_{FeCl_2} = b = 0,15(mol)\\ C\%_{AlCl_3} = \dfrac{0,1.133,5}{160,5}.100\% =8,32\%\\ C\%_{FeCl_2} = \dfrac{0,15.127}{160,5}.100\% = 11,87\%\)
Câu 2 :
\(2KMnO_4 + 16HCl \to 2MnCl_2 + 2KCl + 5Cl_2 + 8H_2O\\ Cl_2 + 2Na \xrightarrow{t^o} 2NaCl\\ 2NaCl \xrightarrow{đpnc} 2Na + Cl_2\\ Cl_2 + 2NaBr \to 2NaCl + Br_2\\ Br_2 + 2NaI \to 2NaBr + I_2\)
Câu 4 :
\(2Na + 2HCl \to 2NaCl + H_2\\ 2K + 2HCl \to 2KCl + H_2\\ 2Na + 2H_2O \to 2NaOH + H_2\\ 2K + 2H_2O \to 2KOH + H_2\\ n_{HCl} = \dfrac{a.C\%}{36,5} = \dfrac{a.C}{3650}(mol)\\ n_{H_2O} = \dfrac{a-a.C\%}{18} (mol)\)
Theo PTHH :
\(2n_{H_2} = n_{HCl} + n_{H_2O}\\ \Leftrightarrow 2.\dfrac{0,05a}{2} = \dfrac{a.C}{3650} + \dfrac{a-a.C\%}{18}\\ \Leftrightarrow 0,05 = \dfrac{C}{3650} + \dfrac{1-C\%}{18}\\ \Leftrightarrow C = 19,73\)
Vậy C% = 19,73%
Câu1:
- Trích mẫu thử
- Cho quỳ tìm vào các mẫu thử
+ mẫu thử nào làm quỳ tím hóa đỏ là HCl
+ mẫu thử nào làm quỳ tím hóa xanh là NaOH
+ các mẫu thử còn lại không hiện tượng là NaCl,NaNO3,NaBr
- Cho dd \(AgNO_3\) tới dư vào các mẫu thử còn lại :
+ mẫu thử nào tạo kết tủa trắng là NaCl
NaCl+\(AgNO_3\) →AgCl↓+ \(NaNO_3\)
+ mẫu thử nào tạo kết tủa màu vàng nhạt là NaBr
NaBr+ \(AgNO_3\) →AgBr↓+ \(NaNO_3\)
+ mẫu thử nào không có hiện tượng là \(NaNO_3\)
Câu 2:
1. \(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2\uparrow+8H_2O\)
2. \(Cl_2+2Na\underrightarrow{t^o}2NaCl\)
3. \(2NaCl\underrightarrow{đpnc}2Na+Cl_2\)
4.\(2HBr+Cl_2\rightarrow2HCl+Br_2\)
\(2NaI_{\left(lạnh\right)}+Br_2\rightarrow2NaBr+I_2\)