Cho 11,2g kim loại X tác dụng hết với H2SO4 đặc, nóng thu được 6,72 lít khí SO2 (đktc). Tên kim loại là:
A. đồng
B. sắt
C. kẽm
D. nhôm
Cho 19,2 gam một kim loại M tác dụng hết với dung dịch H2SO4 đặc nóng thu được 6,72 lít khí SO2 duy nhất (đktc). Kim loại M là
A. Sắt.
B. Kẽm.
C. Magie.
D. Đồng.
Đáp án D
Số mol các chất là:
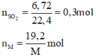
Gọi hoá trị của M là n
Sơ đồ phản ứng: M 0 + H 2 S + 6 2 O 4 ( đặc ) → M + N 2 ( SO 4 ) n + S + 4 O 2 + H 2 O
Các quá trình nhường, nhận electron:
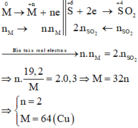
Hòa tan hết 5,4 gam kim loại R (hóa trị III) vào dung dịch H2SO4 loãng thu được 6,72 lít H2 (ở đktc) a/ Xác định tên kim loại b/ Nếu dùng 5,4 gam kim loại trên cho tác dụng hết với H2SO4 đặc nóng thì thể tích khí đo được ở đktc là bao nhiêu
Hòa tan hết 5,4 gam kim loại R (hóa trị III) vào dung dịch H2SO4 loãng thu được 6,72 lít H2 (ở đktc) a/ Xác định tên kim loại b/ Nếu dùng 5,4 gam kim loại trên cho tác dụng hết với H2SO4 đặc nóng thì thể tích khí đo được ở đktc là bao nhiêu
\(n_{H2\left(dktc\right)}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
a) Pt : \(2R+3H_2SO_4\rightarrow R_2\left(SO_4\right)_3+3H_2|\)
2 3 1 3
0,2 0,3
\(n_R=\dfrac{0,3.2}{3}=0,2\left(mol\right)\)
⇒ \(M_R=\dfrac{5,4}{0,2}=27\left(dvc\right)\)
Vậy kim loại R là nhôm
b) \(2Al+6H_2SO_{4\left(đặc,nóng\right)}\rightarrow Al_2\left(SO_4\right)_3+3SO_2+6H_2O|\)
2 6 1 3 6
0,2 0,3
\(n_{SO2}=\dfrac{0,3.3}{2}=0,3\left(mol\right)\)
\(V_{SO2\left(dktc\right)}=0,3.22,4=6,72\left(l\right)\)
Chúc bạn học tốt
a) PTHH: \(2R+3H_2SO_4\rightarrow R_2\left(SO_4\right)_3+3H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\) \(\Rightarrow n_R=0,2\left(mol\right)\)
\(\Rightarrow M_R=\dfrac{5,4}{0,2}=27\) \(\Rightarrow\) R là Nhôm (Al)
b) PTHH: \(2Al+6H_2SO_{4\left(đ\right)}\xrightarrow[]{t^o}Al_2\left(SO_4\right)_3+3SO_2\uparrow+6H_2O\)
Theo PTHH: \(n_{SO_2}=0,3\left(mol\right)\) \(\Rightarrow V_{SO_2}=0,3\cdot22,4=6,72\left(l\right)\)
Cho 11,2g kim loại R hóa trị II tác dụng hết trong dung dịch axit sunfuric (H2SO4), sau phản ứng thu được 4,48 lít khí hiđro (đktc). Tên của kim loại R là:
A. Sắt. B. Magie. C. Niken. D. Kẽm.
Cho 11,2g kim loại R hóa trị II tác dụng hết trong dung dịch axit sunfuric (H2SO4), sau phản ứng thu được 4,48 lít khí hiđro (đktc). Tên của kim loại R là:
A. Sắt. B. Magie. C. Niken. D. Kẽm.
Giai chi tiet :
nH2 = 4,48 : 22,4 = 0,2 (mol)
pthh : R + 2HCl --> RCl2 + H2
0,2 <--------------------- 0,2 (mol )
=> MR= 11,2 : 0,2 = 56 (g/mol)
=> R : Fe
6. Cho 11,2 gam kim loại sắt tác dụng với axit H2SO4 đặc nóng, thu được bao nhiêu lít khí SO2 (đktc). Biết trong quá trình thu khí hao hụt mất 3%.
$n_{Fe} = \dfrac{11,2}{56} = 0,2(mol)$
$2Fe +6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O$
$n_{SO_2} = \dfrac{3}{2}n_{Fe} = 0,3(mol)$
$n_{SO_2\ hao\ hụt} = 0,3.3\% = 0,009(mol)$
$V_{SO_2} = (0,3 - 0,009).22,4 = 6,5184(lít)$
Cho 11,2 gam hỗn hợp gồm Cu và kim loại M tác dụng hết với HCl dư thu được 3,136 lít khí (đktc). Cũng lượng hỗn hợp này cho tác dụng hết với dung dịch H2SO4 đặc nóng dư, thu được 5,88 lít khí SO2 (đktc sản phẩm khử duy nhất). Xác định kim loại M và tính % khối lượng Cu trong hỗn hợp
Cho 11,2 gam hỗn hợp gồm Cu và kim loại M tác dụng hết với HCl dư thu được 3,136 lít khí (đktc). Cũng lượng hỗn hợp này cho tác dụng hết với dung dịch H2SO4 đặc nóng dư, thu được 5,88 lít khí SO2 (đktc sản phẩm khử duy nhất). Xác định kim loại M và tính % khối lượng Cu trong hỗn hợp
Cho 11,2 gam hỗn hợp gồm Cu và kim loại M tác dụng hết với HCl dư thu được 3,136 lít khí (đktc). Cũng lượng hỗn hợp này cho tác dụng hết với dung dịch H2SO4 đặc nóng dư, thu được 5,88 lít khí SO2 (đktc sản phẩm khử duy nhất). Xác định kim loại M và tính % khối lượng Cu trong hỗn hợp
Hỗn hợp X gồm các kim loại Mg, Al, Zn. Lấy m gam hỗn hợp X tác dụng hết với dung dịch HCl dư thu được 6,72 lít khí (đktc). Cũng lấy m gam X tác dụng hết với dung dịch H 2 S O 4 đặc, nóng, dư thu được V lít khí S O 2 (sản phẩm khử duy nhất, ở đktc) và (m+a) gam muối. Giá trị của V và a lần lượt là
A. 3,36 và 28,8
B. 6,72 và 28,8
C. 6,72 và 57,6
D. 3,36 và 14,4