Bằng những phương pháp nào có thể chứng minh được thành phần định tính và định lượng của nước? Viết các phương trình hóa học xảy ra?

Những câu hỏi liên quan
Bằng những phương pháp nào có thể chứng minh được thành phần định tính và định lượng của nước? Viết các phương trình hóa học có thể xảy ra?
trong SGK hóa 8 có mà bạn ,bạn chịu khó tìm nha
Đúng 0
Bình luận (0)
Bằng phương pháp hóa học (dùng dòng điện tách nước, đốt bằng tia lửa điện, hay tác dụng với một số kim loại ở nhiệt độ thường) hay phương pháp vật lí (nhiệt độ sôi, hóa rắn thành đá và tuyết), ta có thể chứng minh được thành phần định tính và định lượng của nước. Phương trình hóa học:
\(2H_2O\rightarrow^{t^o}2H_2+O_2\)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
Đúng 0
Bình luận (0)
Bằng phương pháp hóa học (dùng dòng điện tách nước, đốt bằng tia lửa điện, hay tác dụng với một số kim loại ở nhiệt độ thường) hay phương pháp vật lí (nhiệt độ sôi, hóa rắn thành đá và tuyết), ta có thể chứng minh được thành phần định tính và định lượng của nước.
PTHH: (1) 2H2O -đp-> 2H2 + O2 (đp: điện phân)
(2) Ca + 2H2O -> Ca(OH)2 + H2
Đúng 0
Bình luận (0)
Bằng những phương pháp nào có thể chứng minh được thành phần định tính và định lượng của nước? Viết các phương trình hóa học có thể xảy ra?
Bằng phương pháp hóa học (dùng dòng điện tách nước, đốt bằng tia lửa điện, hay tác dụng với một số kim loại ở nhiệt độ thường) hay phương pháp vật lí (nhiệt độ sôi, hóa rắn thành đá và tuyết), ta có thể chứng minh được thành phần định tính và định lượng của nước. Phương trình hóa học:
2H2O 2H2 + O2
2Na+ 2H2O → 2NaOH + H2↑
Đúng 0
Bình luận (0)
Từ sự phân hủy và tổng hợp nước, ta thấy: Nước là hợp chất tạo bởi hai nguyên tố là hiđro và oxi. Chúng đã kết hợp với nhau:
a) Theo tỉ lệ thể tích là hai phần khí hiđro và một phần khí oxi.
b) Theo tỉ lệ khối lượng là 1 phần khí hiđro và 8 phần khí oxi. Như vậy bằng thực nghiệm người ta tìm ra công thức hóa học của nước là H2O.
Đúng 0
Bình luận (0)
Bằng phương pháp hóa học (dùng dòng điện tách nước, đốt bằng tia lửa điện, hay tác dụng với một số kim loại ở nhiệt độ thường) hay phương pháp vật lí (nhiệt độ sôi, hóa rắn thành đá và tuyết), ta có thể chứng minh được thành phần định tính và định lượng của nước. Phương trình hóa học:
2H2O dp→→dp 2H2 + O2
2Na+ 2H2O → 2NaOH + H2↑
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Ở nhiệt độ phòng, hỗn hợp khí X gồm hiđrocacbon A và lượng dư hiđro có tỉ khối so với H2 là 3,375. Khi cho X qua Ni đun nóng cho đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Y có tỉ khối so với H2 là 4,5. a) Xác định công thức phân tử của A. b) Tính thành phần phần trăm theo thể tích của các chất có trong X. Nếu cho X qua Pd/BaSO4 đun nóng cho đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Z. Trong Z chỉ có hai chất khí là B và hiđro. c) Viết phương trình phản ứng tạo thành B...
Đọc tiếp
Ở nhiệt độ phòng, hỗn hợp khí X gồm hiđrocacbon A và lượng dư hiđro có tỉ khối so với H2 là 3,375. Khi cho X qua Ni đun nóng cho đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Y có tỉ khối so với H2 là 4,5.
a) Xác định công thức phân tử của A.
b) Tính thành phần phần trăm theo thể tích của các chất có trong X.
Nếu cho X qua Pd/BaSO4 đun nóng cho đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Z. Trong Z chỉ có hai chất khí là B và hiđro.
c) Viết phương trình phản ứng tạo thành B trên. Tính tỉ khối của Z so với hiđro.
d) B có thể cho phản ứng polime hóa. Viết phương trình phản ứng này.
Hợp chất B cho phản ứng với Cl2 ở 500 tạo thành C (có chứa 46,4% khối lượng Cl). C phản ứng với dung dịch NaOH loãng thu được D. Cho D phản ứng với nước và Cl2 thu được E (có chứa 32,1% khối lượng Cl). Sau cùng E phản ứng với dung dịch NaOH loãng thu được F.
e) Viết công thức cấu tạo của các chất từ B đến F và viết các phương trình hóa học xảy ra
a.
BTKL ta có mX = mY => nX . MX = nY . mY
MX / My = nY / mY =0.75
Đặt nX = 1 mol => nY = 0,75 mol => nH2 phản ứng = 1 – 0,75 = 0,25mol
* TH hidrocacbon là anken: n anken = n H2 = 0,25 mol => n H2 trong X = 0,75 => M = (6,75 – 0,75 . 2)/0,25 = 21 (loại) * TH là ankin: => n akin = 0,25/2 = 0,125 => n H2 trong X = 0,875 mol => M = (6,75 – 0,875 . 2)/0,125 = 40 =>C3H4
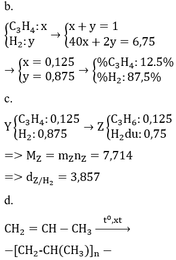

Đúng 0
Bình luận (0)
Bằng phương pháp hoá học nào có thể Xác định được có khí clo lẫn trong khí hiđro clorua ?
Viết PTHH của các phản ứng xảy ra.
Cách 1: Cho hỗn hợp khí đi qua dung dịch HBr hoặc dung dịch HI, Cl 2 sẽ oxi hoá HBr hoặc HI thành Br 2 hoặc I 2 làm cho dung dịch không màu ban đầu chuyển thành màu vàng hoặc màu nâu.
Cl 2 + 2HBr → 2HCl + Br 2 (dung dịch có màu vàng)
hoặc Cl 2 + 2HI → 2HCl + I 2 (dung dịch có màu vàng nâu)
Cách 2: Có thể nhận ra Cl 2 có trong hỗn hợp khí bằng quỳ tím ấm.
Khi cho quỳ tím ẩm vào bình khí nếu quỳ tím ẩm chuyển sang màu đỏ sau đó mất màu đỏ chứng tỏ trong hỗn hợp khí có Cl 2
Đúng 0
Bình luận (0)
- Tính chất hóa học của oxi, hiđro, nước (xác định được những chất phản ứng và viết phương trình minh họa)
* Oxi:
- Tác dụng với phi kim:
PTHH:C+O2---to--->CO2
- Tác dụng với kim loại:
PTHH:3Fe+2O2--to--->Fe3O4
- Tác dụng với hợp chất:
PTHH:C2H4+3O2--to--->2CO2+2H2O
* Hiđrô:
- Tác dụng với oxi:
PTHH:2H2+O2--to--->2H2O
- Tác dụng với đồng (II) oxit:
PTHH:CuO+H2--to--->Cu+H2O
* Nước:
- Tác dụng với một số kim loại:
PTHH:2Na+2H2O→2NaOH+H2↑
- Tác dụng với oxit axit:
PTHH:SO3+H2O→H2SO4
- Tác dụng với oxit bazơ:
PTHH:BaO+H2O→Ba(OH)2
Đúng 2
Bình luận (0)
1) Viết phương trình phản ứng điều chế magie sunàt từ Mg(OH)2 và dung dịch axit sunfuric loãng 2) Có những chất sau: CuO, Mg, Al2O3, Fe(OH)3, Fe2O3. Chất nào tác dụng với HCl sinh ta dung dịch không có màu. 3) Viết phương trình hóa học giữa Magie oxit và axit nitric 4) Có 10g hỗn hợp bột hai kim loại Fe và Cu. Hãy nêu phương pháp xác định thành phần phần trăm (theo khối lượng) của mỗi kim loại trong hỗn hợp theo phương pháp hóa học và vật lý. Viết phương trình hóa học. (Biết Cu ko tác dụng với H...
Đọc tiếp
1) Viết phương trình phản ứng điều chế magie sunàt từ Mg(OH)2 và dung dịch axit sunfuric loãng
2) Có những chất sau: CuO, Mg, Al2O3, Fe(OH)3, Fe2O3. Chất nào tác dụng với HCl sinh ta dung dịch không có màu.
3) Viết phương trình hóa học giữa Magie oxit và axit nitric
4) Có 10g hỗn hợp bột hai kim loại Fe và Cu. Hãy nêu phương pháp xác định thành phần phần trăm (theo khối lượng) của mỗi kim loại trong hỗn hợp theo phương pháp hóa học và vật lý. Viết phương trình hóa học.
(Biết Cu ko tác dụng với HCl và H2SO4)
Bài 1)
Mg(OH)2 + H2SO4 => MgSO4 + 2H20
Bài 2)
sinh ra dd ko màu thì chỉ có Al2O3 thôi
Bài 3)
MgO + 2HNO3 => Mg(NO3)2 + H2O
Bài 4)
phương pháp hóa học
+ lấy hh Fe, Cu tác dụng với HCl
Fe +2 HCl => FeCl2 + H2
+ còn đồng ko tác dụng dc với HCl : ta lọc đồng ra khỏi hh òi phơi khô. Ta giả định cho đồng là 4g => mFe = 6g
% Cu = 4*100/10 = 40(%)
% Fe = 100- 40= 60 (%)
phương pháp vật lý
dùng nam châm hút sắt ra khỏi hỗn hợp. Ta có mFe là 6g => m Cu = 4 (g)
% Cu = 4*100/10 = 40(%)
% Fe = 100-40 = 60(%)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 4,6 gam rượu etylic trong oxi thu được khí cacbonđioxit và hơi nước. a. Viết phương trình hóa học xảy ra? b. Tính thể tích khí oxi (ở đktc) cần dùng ? c. Tính khối lượng khí cacbonic và khối lượng hơi nước tạo thành?
a) $C_2H_5OH + 3O_2 \xrightarrow{t^o} 2CO_2 + 3H_2O$
b) $n_{C_2H_5OH} = \dfrac{4,6}{46} = 0,1(mol)$
$n_{O_2} = 3n_{C_2H_5OH} = 0,3(mol)$
$V_{O_2} = 0,3.22,4 = 6,72(lít)$
c)
Theo PTHH :
$n_{CO_2} = 2n_{C_2H_5OH} = 0,2(mol) \Rightarrow V_{CO_2} = 0,2.22,4 = 4,48(lít)$
$n_{H_2O} = 3n_{C_2H_5OH} = 0,3(mol) \Rightarrow m_{H_2O} = 0,3.18 = 5,4(gam)$
Đúng 2
Bình luận (0)
Những kim loại nào có thể điều chế bằng phương pháp trên từ các oxit X tương ứng sau: MgO, Fe3O4, Al2O3, CuO, CaO? Viết phương trình hóa học minh họa cho các quá trình trên
Những oxit bị khử là: Fe3O4, CuO
Pt: Fe3O4 + 4H2 → 3Fe + 4H2O
CuO + H2 → Cu + H2O
Chú ý: Nhiệt luyện là phương pháp dùng (H2, CO) khử các oxit kim loại trung bình (–K, Na, Ca, Ba, Mg, Al)
Đúng 0
Bình luận (0)
Câu 1: Ngâm một đinh sắt sạch trong dung dịch đồng (II) sunfat. Nêu hiện tượng quan sát được? Viết PTHH xảy ra ( nếu có)Câu 2: Nhỏ vài giọt dung dịch bạc nitrat vào ống nghiệm đựng dd Natri clorua. Nêu hiện tượng quan sát được? Viết PTHH xảy ra (nếu có).Câu 3: Dẫn từ từ 6,72 lít khí CO2 ( ở đktc) vào dung dịch nước vôi trong dư.a) Viết phương trình hóa học của phản ứng xảy ra.b) Tính số gam kết tủa thu được sau phản ứng.Câu 4: Nêu và giải thích hiện tượng xảy ra trong các trường hợp sau:a) Nhỏ v...
Đọc tiếp
Câu 1: Ngâm một đinh sắt sạch trong dung dịch đồng (II) sunfat. Nêu hiện tượng quan sát được? Viết PTHH xảy ra ( nếu có)
Câu 2: Nhỏ vài giọt dung dịch bạc nitrat vào ống nghiệm đựng dd Natri clorua. Nêu hiện tượng quan sát được? Viết PTHH xảy ra (nếu có).
Câu 3: Dẫn từ từ 6,72 lít khí CO2 ( ở đktc) vào dung dịch nước vôi trong dư.
a) Viết phương trình hóa học của phản ứng xảy ra.
b) Tính số gam kết tủa thu được sau phản ứng.
Câu 4: Nêu và giải thích hiện tượng xảy ra trong các trường hợp sau:
a) Nhỏ vài giọt dung dịch Ba(OH)2 vào ống nghiệm chứa dung dịch H2SO4.
b) Nhỏ từ từ đến dư dung dịch NaOH vào ống nghiệm chứa dung dịch HCl có sẵn mẩu quỳ tím.
Câu 5: Cho các chất sau: Zn(OH)2, NaOH, Fe(OH)3, KOH, Ba(OH)2.
a) Những chất nào có phản ứng với khí CO2?
b) Những chất nào bị phân hủy bởi nhiệt?
c) Những chất nào vừa có phản ứng với dung dịch HCl, vừa phản ứng với dung dịch NaOH?
Câu 6: Cho những oxit sau: BaO, Fe2O3, N2O5, SO2. Những oxit nào tác dụng với: a. Nước b. Axit clohiđric c. Natri hiroxit
Viết phương trình phản ứng xảy ra
Câu 7: Có 3 ống nghiệm, mỗi ống đựng một dung dịch các chất sau: Na2SO4 ; HCl; NaNO3. Hãy nhận biết chúng bằng phương pháp hóa học. Viết các PTHH xảy ra (nếu có).
Câu 8: Bằng phương pháp hóa học, hãy phân biệt các lọ đựng các dung dịch sau: KOH; Ba(OH)2 ; K2SO4; H2SO4; HCl. Viết các phương trình phản ứng xảy ra (nếu có).
hyyyyyyyyyyyyyyyyyyyyyyyyyyyyyyyyyyyydjyh





















