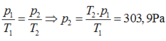Một bình được nạp khí ở nhiệt độ 57 o C dưới áp suất 280kPa. Sau đó bình được chuyển đến một nơi có nhiệt độ 86 o C . Tính độ tăng áp suất của khí trong bình.

Những câu hỏi liên quan
Một bình được nạp khí ở nhiệt độ 430C dưới áp suất 285kPa. Sau đó bình được chuyển đến một nơi có nhiệt độ 570C. Tính độ tăng áp suất của khí trong bình.
Ta có : \(T_1=273+43=313^0K;T_2=273+57=330^0K\)
Theo định luật Sác lơ:
\(\frac{p_1}{T_1}=\frac{p_2}{T_2}\rightarrow p_2=\frac{T_2}{T_1}p_1=\frac{330}{313}285=330,5kPa\)
Độ tăng áp suất:
\(\Delta p=p_2-p_1=300,5-285=15,5kPa\)
Đúng 0
Bình luận (1)
Một bình được nạp khí ở 330C dưới áp suất 300 Pa. Sau đó bình được chuyển đến một nơi có nhiệt độ 370C. Tính độ tăng áp suất của khí trong bình. A. 303,9Pa B. 3,9 Pa C. 336,4Pa D. 36,4.10-5Pa
Đọc tiếp
Một bình được nạp khí ở 330C dưới áp suất 300 Pa. Sau đó bình được chuyển đến một nơi có nhiệt độ 370C. Tính độ tăng áp suất của khí trong bình.
A. 303,9Pa
B. 3,9 Pa
C. 336,4Pa
D. 36,4.10-5Pa
một bình kín được nạp khí ở nhiệt độ 17 độ C với áp suất 100 KpA sau đó bình được chuyển đến một nơi có nhiệt độ 31,5 độ C tính độ tăng áp suất của khí trong bình
Do thể tích bình không đổi (điều kiện đẳng tích)
=> \(\dfrac{P_2}{P_1}=\dfrac{T_2}{T_1}\)
=> \(\dfrac{P_2}{100}=\dfrac{31,5+273}{17+273}=1,05\)
=> P2 = 105 (KpA)
=> Độ tăng áp suất khí = 105 - 100 = 5 (KpA)
Đúng 2
Bình luận (0)
Một bình được nạp khí ở 33 ° C dưới áp suất 300 Pa. Sau đó bình được chuyển đến một nơi có nhiệt độ 37 ° C, coi thể tích của bình không thay đổi. Tính độ tăng áp suất của khí trong bình.
Một bình được nạp khí ở 330C dưới áp suất 300 Pa. Sau đó bình được chuyển đến một nơi có nhiệt độ 370C, coi thể tích của bình không thay đổi. Tính độ tăng áp suất của khí trong bình
Ta có
T 1 = 273 + 33 = 306 ( K ) T 2 = 273 + 37 = 310 ( K )
Theo quá trình đẳng nhiệ
p 1 T 1 = p 2 T 2 ⇒ p 2 = T 2 . p 1 T 1 = 310.300 306 ≈ 304 P a ⇒ Δ p = p 2 − p 1 = 304 − 300 = 4 P a
Đúng 0
Bình luận (0)
3) Biết áp suất của một lượng khí hydro 0oC là 700mmHg.Nếu thể tích của khí được giử không đổi thì áp suất của lượng đó ở 30oC sẽ là bao nhiêu?
4) Một bình được nạp khí ở nhiệt độ 33oC dưới áp suất 3.105Pa. Sau đó bình được chuyển đến một nơi có nhiệt độ 37oC thì áp suất của bình là bao nhiêu?
Câu 3.
\(T_1=0^oC=273K\)
\(T_2=30^oC=30+273=303K\)
Qúa trình đẳng tích:
\(\dfrac{p_1}{T_1}=\dfrac{p_2}{T_2}\Rightarrow\dfrac{700}{273}=\dfrac{p_2}{303}\)
\(\Rightarrow p_2=776,92mmHg\)
Câu 4.
\(T_1=33^oC=33+273=306K\)
\(T_2=37^oC=37+273=310K\)
Qúa trình đẳng tích:
\(\dfrac{p_1}{T_1}=\dfrac{p_2}{T_2}\Rightarrow\dfrac{3\cdot10^5}{306}=\dfrac{p_2}{310}\)
\(\Rightarrow p_2=303921Pa\)
Đúng 3
Bình luận (0)
Một bình nạp khí ở nhiệt độ 33 độ C dưới áp suất 300kPa . Tăng nhiệt độ cho bình đến nhiệt độ 37 độ C đẳng tích thì độ tăng áp suất của khí trong bình là
Trạng thái 1: \(\left\{{}\begin{matrix}p_1=300kPa\\T_1=33^oC=306K\end{matrix}\right.\)
Trạng thái 2: \(\left\{{}\begin{matrix}p_2=???\\V_2=37^oC=310K\end{matrix}\right.\)
Quá trình đẳng tích:
\(\dfrac{p_1}{T_1}=\dfrac{p_2}{T_2}\Rightarrow\dfrac{300}{306}=\dfrac{p_2}{310}\)
\(\Rightarrow p_2=303,92kPa\)
Độ tăng áp suất khí trong bình:
\(\Delta p=p_2-p_1=303,92-300=3,92kPa\)
Đúng 4
Bình luận (0)
bơm khí nitơ vào một bình thép có thể tích cố định V1=8,31 đến áp suất p1=15at ở nhiệt độ 27C. Sau đó hơ nóng bình khí này đến nhiệt độ 127C ta có áp suất p2. Khối lượng của khối khí Nitơ và áp suất lúc sau tính được là bao nhiêu?
Người ta điều chế khí hiđrô và chứa vào một bình lớn dưới áp suất 1 atm, ở nhiệt độ 20 ° C. Tính thể tích khí phải lấy từ bình lớn ra để nạp vào một bình nhỏ thể tích 20 lít dưới áp suất 25 atm. Coi nhiệt độ không đổi.