Viết phương trình hoá học dạng phân tử và dạng ion rút gọn của phản ứng giữa axit photphoric với lượng dư của: K2CO3

Những câu hỏi liên quan
Viết phương trình hoá học dạng phân tử và dạng ion rút gọn của phản ứng giữa axit photphoric với lượng dư của: BaO
Các chất lấy dư nên muối tạo ra là muối trung hoà: 2H3PO4 + 3BaO → Ba3(PO4)2 + 3H2O
Phương trình phân tử trùng với phương trình ion thu gọn
Đúng 0
Bình luận (0)
Viết phương trình hoá học dạng phân tử và dạng ion rút gọn của phản ứng giữa axit photphoric với lượng dư của: Ca(OH)2
2H3PO4 + 3Ca(OH)2 → Ca3(PO4)2 + 6H2O
2H3PO4 + 3Ca2+ + 6OH- → Ca3(PO4)2 + 6H2O
Đúng 0
Bình luận (0)
Viết phương trình hóa học dạng phân tử vào dạng ion rút gọn của phản ứng giữa H3PO4 với lượng dư của
a. BaO.
b. Ca(OH)2.
c. K2CO3.
$a) 3BaO + 2H_3PO_4 → Ba_3(PO_4)_2 + 3H_2O$
$b) 3Ca(OH)_2 + 2H_3PO_4 → Ca_3(PO_4)_2 + 6H_2O$
$c) 3K_2CO_3 + 2H_3PO_4 → 2K_3PO_4 + 3CO_2 + 3H_2O$
Đúng 1
Bình luận (0)
Dạng rút gọn :
$a) 3BaO + 2H_3PO_4 \to 3Ba^{2+} + 2PO_4^{3-} + 3H_2O$
$b) Ca^{2+} + 6OH^- + 2H_3PO_4 \to Ca_3(PO_4)_2 + 6H_2O$
$c) 3CO_3^{2-} + H_3PO_4 \to 2PO_4^{3-} + 3CO_2 + 3H_2O$
Đúng 1
Bình luận (0)
Viết phương trình hoá học ở dạng phân tử và dạng ion rút gọn của phản ứng xảy ra trong dung dịch giữa các chất sau:
1. bari clorua và natri photphat.
2. axit photphoric và canxi hiđroxit, tạo ra muối axit ít tan.
3. axit nitric đặc, nóng và sắt kim loại.
4. natri nitrat, axit sunfuric loãng và đồng kim loại.
Phương trình hoá học ở dạng phân tử và dạng ion rút gọn của các phản ứng xảy ra trong dung dịch :
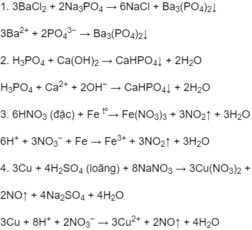
Đúng 0
Bình luận (0)
Trong y học, dược phẩm Nabica (
N
a
H
C
O
3
) là chất được dùng để trung hoà bớt lượng dư axit HCl trong dạ dày. Hãy viết phương trình hoá học dưới dạng phân tử và ion rút gọn của phản ứng đó. Tính thể tích dung dịch HCl 0,035M (nồng độ axit trong dạ dày) được trung hoà và thể tích khí
C
O
2
) sinh ra ở đktc khi uống 0,336 g
N
a
H...
Đọc tiếp
Trong y học, dược phẩm Nabica ( N a H C O 3 ) là chất được dùng để trung hoà bớt lượng dư axit HCl trong dạ dày. Hãy viết phương trình hoá học dưới dạng phân tử và ion rút gọn của phản ứng đó. Tính thể tích dung dịch HCl 0,035M (nồng độ axit trong dạ dày) được trung hoà và thể tích khí C O 2 ) sinh ra ở đktc khi uống 0,336 g N a H C O 3 ).
NaHCO3 + HCl → CO2↑ + H2O + NaCl
HCO3− + H+ → CO2↑ + H2O
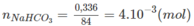
Theo phản ứng cứ 1 mol N a H C O 3 tác dụng với 1 mol HCl và tạo ra 1 mol C O 2 . Từ đó :
Thể tích HCl được trung hoà :
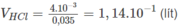
Thể tích khí C O 2 tạo ra :
V C O 2 = 4.10−3.22,4 = 8,96.10−2 (lít).
Đúng 0
Bình luận (0)
Lấy thí dụ và viết các phương trình hoá học dưới dạng phân tử và ion rút gọn cho phản ứng sau: Tạo thành chất khí
Tạo thành chất khí:
1/ FeS + 2HCl → FeCl2 + H2S
FeS + 2H+ → Fe2+ + H2S
2/ K2SO3 + 2HCl → 2KCl + H2O + SO2
2H+ + SO32- → H2O + SO2
3/ NaOH + NH4Cl → NaCl + NH3 + H2O
NH4+ + OH- → NH3 + H2O
Đúng 0
Bình luận (0)
Lấy thí dụ và viết các phương trình hoá học dưới dạng phân tử và ion rút gọn cho phản ứng sau:
Tạo thành chất kết tủa
Tạo thành chất kết tủa:
1/ AgNO3 + HCl → AgCl + HNO3
Ag+ + Cl- → AgCl
2/ K2SO4 + Ba(OH)2 → 2KOH + BaSO4
Ba2+ + SO42- → BaSO4
3/ Na2CO3 + MgCl2 → 2NaCl + MgCO3
Mg2+ + CO32- → MgCO3
Đúng 0
Bình luận (0)
Viết phương trình hoá học (dưới dạng phân tử và ion rút gọn) của phản ứng trao đổi ion trong dung dịch tạo thành từng chất kết tủa sau:Cr(OH)3 ; Al(OH)3; Ni(OH)2
CrCl3 + 3NaOH (đủ) → Cr(OH)3 ↓ + 3 NaCl
Cr3+ + 3OH- → Cr(OH)3 ↓
AlCl3 + 3NaOH (đủ) Al(OH)3 ↓ + 3 NaCl
Al3+ + 3OH- → Al(OH)3 ↓
Hoặc AlCl3 + 3NH3 (dư) + 3H2O → Al(OH)3 ↓ + 3NH4Cl
Al3+ + 3NH3 (dư) + 3H2O → Al(OH)3 ↓ + 3NH4+
Ni(NO3)2 + 2NaOH → Ni(OH)2 ↓ + 2NaNO3
Ni2+ + 2OH- → Ni(OH)2 ↓
Đúng 0
Bình luận (0)
Lấy thí dụ và viết các phương trình hoá học dưới dạng phân tử và ion rút gọn cho phản ứng sau: Tạo thành chất điện li yếu
Tạo thành chất điện li yếu:
1/ 2CH3COONa + H2SO4 → 2CH3COOH + Na2SO4
CH3COO- + H+ → CH3COOH
2/ NaOH + HNO3 → NaNO3 + H2O
H+ + OH- → H2O
3/ NaF + HCl NaCl + HF
H+ + F- → HF
Đúng 0
Bình luận (0)





