Cho m gam hỗn hợp Zn, Fe tác dụng với vừa đủ với 73g dd HCl 10%. Cô cạn dd thu được 13,15g muối. Giá trị m là:
A. 7,05 g
B. 5,3 g
C. 4,3 g
D. 6,05 g
Cho 12,1 g hỗn hợp Zn, Fe tác dụng với vừa đủ với m g dd HCl 10%. Cô cạn dd thu được 19,2 g muối. Giá trị m là:
A. 73 g
B. 53 g
C. 43 g
D. 63 g
Đáp án A
mmuối = mKL + mgốc axit => 19,2 = 12,1 + mCl-
![]() = nHCl
= nHCl
![]() .100%
.100%
=> m = 73 g
Cho m gam hỗn hợp Zn, Fe tác dụng vừa đủ với dd 73g dd HCl 10%. Cô cạn dd thu được 13,15g muối. Giá trị m là ???
\(m_{HCl}=\frac{73.10}{100}=7,3\left(g\right)\)
\(n_{HCl}=\frac{7,3}{36,5}=0,2\left(mol\right)\)
\(Zn+2HCl-->ZnCl2+H2\)
\(Fe+2HCl-->FeCl2+H2\)
\(n_{H2}=\frac{1}{2}n_{HCl}=0,1\left(mol\right)\)
\(m_{H2}=0,2.2=0,2\left(g\right)\)
\(m=m_{KL}=m_{H2}+m_{muối}-m_{HCl}=13,15+0,2-7,3=6,05\left(g\right)\)
Ta có :
\(C\%_{HCl}=\frac{m_{HCl}}{m_{dd}}.100\%\Leftrightarrow10\%=\frac{m_{HCl}}{73}.100\%\)
\(\Rightarrow m_{HCl}=7,3\left(g\right)\)
\(\Rightarrow n_{HCl}=0,2\left(mol\right)\)
\(m_{muoi}=m_{kl}+m_{goc.axit}=m+0,2.35,5=13,15\)
\(\Rightarrow m=6,05\left(g\right)\)
Cho m gam hỗn hợp Zn, Fe tác dụng với vừa đủ với 73 gam dung dịch HCl 10%. Cô cạn dung dịch thu được 13,15 g muối. Giá trị m là
A. 7,05
B. 5,3
C. 4,3
D. 6,05
Câu 6: Cho 6,05 g hỗn hợp gồm Zn và Al tác dụng vừa đủ với m gam dd HCl 10% cô cạn dd sau phản ứng thu được 13,15 g
muối khan. Tìm giá trị của m.
Câu 7: Cho 2,24g sắt tác dụng với dung dịch HCl dư. Khí sinh ra cho qua ống đựng 4,2g CuO được đun nóng. Xác định khối
lượng của chất rắn ở trong ống sau phản ứng.
Câu 7 nCuO=0,0525mol
Fe+2HCl->FeCl2+H2
0,04 0,04mol
H2+CuO-> Cu+H2O
Ta có 0,04/1 <0,0525/1
=> CuO dư
Chất rắn gồm Cu: 0,04mol; CuO:0,0125mol
m(chất rắn)=3,56g
Câu 6:
Gọi x=nH2=> nHCl=2x
2Al+6HCl->2AlCl3+3H2
Zn+2HCl-> ZnCl2+H2
Bảo toàn khối lượng
6,05+ 36,5.2x=13,15+2x
=>x=0,1mol
mHCl= 0,1.2.36,5=7,3g
mddHCl= 7,3.100/10=73g
Cho 6,05 g hỗn hợp gồm Zn và Al tác dụng vừa đủ với m gam dd HCl 10% cô cạn dd sau phản ứng thu được 13,15 g muối khan. Tìm giá trị của m
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Ta có:
\(m_{muoi}=m_{kl}+m_{Cl^-}\)
Nên m chất rắn tăng lên là khối lượng gốc clorua nhập vào
\(m_{cr\left(tanglen\right)}=m_{Cl^-}\Rightarrow m_{Cl^-}=13,15-6,05=7,1\left(g\right)\)
\(\Rightarrow n_{Cl^-}=0,2\left(mol\right)\)
\(\Rightarrow m_{HCl}=7,3\left(g\right)\Rightarrow m=73\left(g\right)\)
Gọi số mol Zn và Al là a và b
Ta có 65a+27b=6,05
Zn+2HCl->ZnCl2+H2
a 2a a a
2Al+6HCl->2AlCl3+3H2
b 3b b 1,5b
Lại có 136a+133,5b=13,15
->a=17/188; b=3/470
a. nH2=a+1,5b=0,1mol
. nHCl phản ứng=2a+3b=2nH2=0,2mol
->nHCl dư=0,2.20%=0,04
->nHCl ban đầu=0,24mol
->mHCl=0,24.36,5=8,76g
->mddHCl=8,76/10%=87,6g
Cho 6,05 g hỗn hợp gồm Zn và Al tác dụng vừa đủ với dd HCl 10% cô cạn dd sau phản ứng thu được 13,15 g muối khan. a/ Tìm thể tích khí hidro thoát ra ở đktc b/ Tìm khối lượng dd HCl đã dùng biết lượng axit dùng dư 20% so với lượng phản ứng
Zn+2HCl→ZnCl2+H2
2Al+6HCl→2AlCl3+3H2
Gọi số mol HCllà x
n H2=\(\dfrac{1}{2}\)n HCl=0,5x
Bảo toàn khối lượng: mkl+mHCl=mmuối+mH2
6,05+36,5x=13,15+0,5x.2
→x=0,2 mol
mHCl=0,2.36,5=7,3 gam
=>m =mddHCl=\(\dfrac{7,3}{10\%}\)=73gam
cho 12,1 g hỗn hợp Zn, Fe tác dụng vừa đủ với m g dd HCL 10% . Cô cạn dd thu được 19,2g muối. Giá trị m là :
Bạn qua đây tham khảo:
https://moon.vn/hoi-dap/cho-121-g-hon-hop-zn-fe-tac-dung-voi-vua-du-voi-m-g-dd-hcl-10-co-can-dd-thu-duoc-192-520026
Cho m gam hỗn hợp các oxit CuO, F e 2 O 3 , ZnO tác dụng vừa đủ với 50 ml dd HCl 2M. Cô cạn dung dịch sau phản ứng thu được 3,071 g muối clorua. Giá trị của m là:
A. 0,123g
B. 0,16g
C. 2,1g
D. 0,321g
Tương tự bài 1 và bài 4, ta có:
m 3 o x i t + m H C l = m m u o i + m H 2 O s a n p h a m
⇔ m 3 o x i t = m m u o i + m H 2 O s a n p h a m - m H C l
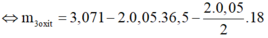
⇔ m 3 o x i t = 0,321g
⇒ Chọn D.
Cho x gam hỗn hợp gồm MgO, F e 2 O 3 , ZnO, CuO tác dụng vừa đủ với 50g dd H 2 S O 4 11,76%. Cô cạn dd sau phản ứng thu được 8,41 g muối khan. Giá trị của m là:
A. 3,2g
B. 3,5g
C. 3,61g
D. 4,2g
Tương tự bài 1, ta có:
m 4 o x i t = m m u o i - m H 2 S O 4 + m H 2 O s a n p h a m
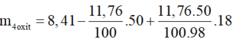
m 4 o x i t = 3,61g
⇒ Chọn C.