ΔU=Q là hệ thức của nguyên lí I áp dụng cho:
A. quá trình đẳng áp
B. quá trình đẳng nhiệt
C. quá trình đẳng tích
D. cả ba quá trình nói trên
Một khí lí tưởng thực hiện quá trình đẳng tích 1 – 2 rồi đẳng áp 2 – 3. Trong mỗi đoạn, khí nhận nhiệt hay tỏa nhiệt?
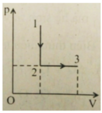
A. 1 – 2 nhận nhiệt; 2 – 3 nhận nhiệt
B. 1 – 2 nhận nhiệt; 2 – 3 tỏa nhiệt
C. 1 – 2 tỏa nhiệt; 2 – 3 nhận nhiệt
D. 1 – 2 tỏa nhiệt; 2 – 3 tỏa nhiệt
Từ đồ thị, ta có:
Quá trình 1→2: Quá trình đẳng tích, trong quá trình này
Thể tích không đổi
Lại có: p 1 T 1 = p 2 T 2 và p 1 > p 2
Ta suy ra T 2 > T 1
=> Nhiệt độ tăng nên nội năng tăng
=> Khí tỏa nhiệt
Quá trình 2→3: Quá trình đẳng áp, trong quá trình này:
Áp suất không đổi
Thể tích khí tăng V 3 > V 2
=> Nhiệt độ khí tăng => Nội năng tăng
=> Khí sinh công => Khí nhận nhiệt
Đáp án: C
Một khí lí tưởng thực hiện quá trình đẳng tích 1 – 2 rồi đẳng áp 2 – 3 (Hình 33.2) Trong mỗi đoạn, khí nhận nhiệt hay tỏa nhiệt?
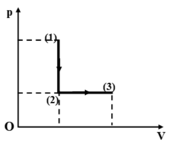
A. 1 – 2 nhận nhiệt; 2 – 3 nhận nhiệt
B. 1 – 2 nhận nhiệt; 2 – 3 tỏa nhiệt.
C. 1 – 2 tỏa nhiệt; 2 – 3 nhận nhiệt
D. 1 – 2 tỏa nhiệt; 2 – 3 tỏa nhiệt
Chọn C.
Quá trình 1-2 là làm lạnh đẳng tích → khí tỏa nhiệt, ∆ U = Q 12 < 0
Quá trình 2-3 là làm giãn nở đẳng áp → khí nhận nhiệt và sinh công A = - p 2 V 3 - V 2
Một lượng khí lí tưởng thực hiện quá trình đẳng áp 1 – 2 rồi đẳng nhiệt 2 – 3. Trong mỗi đoạn, khí nhận công hay sinh công?
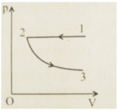
A. 1 – 2 nhận công; 2 – 3 sinh công
B. 1 – 2 nhận công; 2 – 3 nhận công
C. 1 – 2 sinh công; 2 – 3 sinh công
D. 1 – 2 sinh công; 2 – 3 nhận công
Từ đồ thị, ta có:
Quá trình 1→2: Quá trình đẳng áp, trong quá trình này
Áp suất không đổi
Thể tích giảm V 2 < V 1
Lại có V 1 T 1 = V 2 T 2
⇒ V 1 V 2 = T 1 T 2 > 1 ⇒ T 1 > T 2
=> Nhiệt độ giảm
=> Vật nhận công
Quá trình 2→3: Quá trình đẳng nhiệt, trong quá trình này:
Nhiệt độ không đổi
Thể tích khí tăng nên vật thực hiện công
Đáp án: A
Một lượng khí lí tưởng thực hiện quá trình đẳng áp 1 – 2 rồi đẳng nhiệt 2 – 3 (Hình 33.1). Trong mỗi đoạn, khí nhận công hay sinh công?
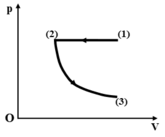
A. 1 – 2 nhận công; 2 – 3 sinh công
B. 1 – 2 nhận công; 2 – 3 nhận công
C. 1 – 2 sinh công; 2 – 3 sinh công.
D. 1 – 2 sinh công; 2 – 3 nhận công.
Chọn A.
Đoạn 1-2 là quá trình nén đẳng áp → khí nhận công
Quá trình 2-3 là giãn nở đẳng nhiệt → khí sinh công
Một khối khí ban đầu có các thông số trạng thái là: p 0 , V 0 , T 0 . Biến đổi đẳng áp đến 2 V 0 sau đó nén đẳng nhiệt về thể tích ban đầu. Đồ thị diễn tả quá trình biến đổi trên là
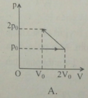
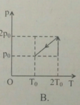
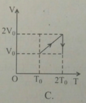
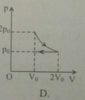
Chọn C.
Trong đồ thị (V, T) đường biểu diễn quá trình đẳng áp là đường thẳng có đường kéo dài đi qua gốc O, đường biểu diễn quá trình đẳng nhiệt là đường thẳng song song với trục OV.
Trong một quá trình nung nóng đẳng áp ở áp suất 1 , 5 . 10 5 P a , một chất khí tăng thể tích từ 40 d m 3 đến 60 d m 3 và tăng nội năng một lượng là 4,28J. Nhiệt lượng truyền cho chất khí là:
A. 1280 J
B. 3004,28 J
C. 7280 J
D. – 1280 J
Công do chất khí thực hiện
A = p . Δ V = 1 , 5.10 5 .2.10 − 2 = 3000 J
Vì khí nhận nhiệt lượng và thực hiện công nên A<0
Theo nguyên lí I:
Q = Δ U − A = 4 , 28 − − 3000 = 3004 , 28 J
Đáp án: B
Trong một quá trình nung nóng đẳng áp ở áp suất 1,5. 10 5 Pa, một chất khí tăng thể tích từ 40 d m 3 đến 60 d m 3 và tăng nội năng một lượng là 4,28 J. Nhiệt lượng truyền cho chất khí là
A. 1280 J
B. 3004,28 J
C. 7280 J
D. – 1280 J
Chọn B.
Áp dụng công thức nguyên lí I NĐLH: ∆U = A + Q
Vì chất khí thực hiện công nên A = -p.∆V
= -1,5. 10 5 .(60. 10 - 3 – 40. 10 - 3 ) = 3000J.
Khi tăng nội năng một lượng là 4,28 J nên ∆U = 4,28 J
Do đó: Q = ∆U - A = 4,28 + 3000 = 3004,28J.
Trong một quá trình nung nóng đẳng áp ở áp suất 1 , 5 . 10 5 P a , một chất khí tăng thể tích từ 40 d m 3 đến 60 d m 3 và tăng nội năng một lượng là 4,28 J. Nhiệt lượng truyền cho chất khí là
A. 1280 J.
B. 3004,28 J.
C. 7280 J.
D. – 1280 J.
Chọn B.
Áp dụng công thức nguyên lí I NĐLH: ∆U = A + Q
Vì chất khí thực hiện công nên A = -p.∆V = -1,5.105.(60.10-3 – 40.10-3) = 3000J.
Khis tăng nội năng một lượng là 4,28 J nên ∆U = 4,28 J
Do đó: Q = ∆U - A = 4,28 + 3000 = 3004,28J.
Hệ thức không liên quan đến các đẳng quá trình là:
A. p/T = const
B. p/V = const
C. p 1 V 1 = p 2 V 2
D. V/T = const
Phát biểu nào sau đây là đúng khi nói về quá trình đẳng nhiệt của một lượng khí xác định?
A. Áp suất tỉ lệ thuận với thể tích.
B. Thương của áp suất và thể tích là một hằng số.
C. Trên giản đồ p – V, đồ thị là một đường hypebol.
D. Thể tích không phụ thuộc vào áp suất
Đáp án: C
Ta có: Định luật Bôilơ - Mariốt:
Trong quá trình đẳng nhiệt của một lượng khí nhất định, áp suất tỉ lệ nghịch với thể tích.
p ~ 1 V → p V = h / s
=> Các phương án:
A, D – sai vì: áp suất tỉ lệ nghịch với thể tích
B – sai vì: Tích của áp suất và thể tích là một hằng số chứ không phải thương
C - đúng