Bình chứa được 4g hiđrô ở 53 ° C dưới áp suất 44,4.10 5 N / m 2 . Thay Hiđrô bởi khí khác thì bình chứa được 8g khí mới ở 27 ° C dưới áp suất 5. 10 5 pa. Khí thay Hiđro là khí gì? Biết khí này là đơn chất.
A. O 2
B. N 2
C.He
D. C l 2
Một bình chứa 4,8 lít khí hiđrô ở 5 . 10 5 P a ở 14 ∘ C . Người ta tăng nhiệt độ của khí lên tới 26 ° C . Vì bình không thật kín nên có một phần khí thoát ra ngoài và áp suất trong bình không thay đổi. Biết khối lượng mol của hiđrô là μ = 2 . 10 - 3 k g / m o l . Khối lượng khí thoát ra ngoài là:
A. 9 , 09 . 10 - 5 k g
B. 7 , 08 . 10 - 5 k g
C. 10 , 7 . 10 - 5 k g
D. 8 , 07 . 10 - 5 k g
Chọn D.
Áp dụng phương trình Cla-pê-rôn – Men-đê-lê-ép:
+ Trạng thái 1 (khi chưa tăng nhiệt độ):
Khối lượng m1, p1 = 5.105 Pa, V1 = 4,8 lít, T1 = 287 K
Từ phương trình:
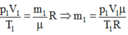
+ Trạng thái 2 (khi đã tăng nhiệt độ):
Khối lượng m2, p2 = p1 = 5.105 Pa, V2 = V1 = 4,8 lít, T2 = 26 + 273 = 287 K.
Từ phương trình:
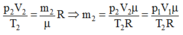
Khối lượng khí thoát ra ngoài:
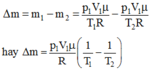
Thay số:
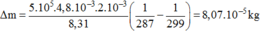
Người ta điều chế khí hiđrô và chứa vào một bình lớn dưới áp suất 1 atm, ở nhiệt độ 20 ° C. Tính thể tích khí phải lấy từ bình lớn ra để nạp vào một bình nhỏ thể tích 20 lít dưới áp suất 25 atm. Coi nhiệt độ không đổi.
Một bình chứa 4,8 lít khí hiđrô ở 5 . 10 5 P a ở 14 o C . Người ta tăng nhiệt độ của khí lên tới 26 o C . Vì bình không thật kín nên có một phần khí thoát ra ngoài và áp suất trong bình không thay đổi. Tính khối lượng khí thoát ra ngoài biết khối lượng mol của hiđrô là 2 . 10 - 3 k g / m o l .
Một bình bằng thép dung tích 62 lít chứa khí hiđrô ở áp suất 4,5Mpa và nhiệt độ 27 o C . Dùng bình này bơm được bao nhiêu quả bóng bay, dung tích mỗi quả 8,5 lít, tới áp suất 1 , 05 . 10 5 P a . Nhiệt độ khí trong bóng bay là 13 o C .
Một bình có dung tích V = 10 lít chứa một lượng khí hiđrô bị nén ở áp suất p = 50atm và nhiệt độ 7 ° . Khi nung nóng bình, do bình hờ nên có một phần khí thoát ra; phần khí còn lại có nhiệt độ 17 ° C và vẫn dưới áp suất như cũ. Tính khối lượng khí đã thoát ra.
Gọi m i , rrn là khối lượng khí trong bình trước và sau khi nung nóng bình.
Áp dụng phương trình Menđêlêep - Clapêrôn ta có:
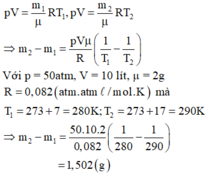
Làm thí nghiệm người ta thấy bình chứa 1kg khí nitơ bị nổ ở nhiệt độ 350 ° C. Tính khối lượng khí hiđrô có thế chứa trong bình cùng loại nếu nhiệt độ tối đa bị nổ là 50 ° C và hệ số an toàn là 5, nghĩa là áp suất tối đa chỉ bằng 1/5 áp suất gây nổ. Cho H = 1; N = 14; R = 8,31J/mol.K.
+ Gọi V là thể tích của bình và p n là áp suất gây nổ.
+ Đối với khí nitơ ta có:
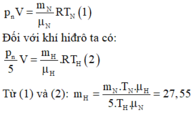
Làm thí nghiệm người ta thấy bình chứa 1kg khí nitơ bị nổ ở nhiệt độ 3500C. Tính khối lượng khí hiđrô có thể chứa trong bình cùng loại nếu nhiệt độ tối đa bị nổ là 500C và hệ số an toàn là 5, nghĩa là áp suất tối đa chỉ bằng 1/5 áp suất gây nổ. Cho H = 1; N = 14; R = 8,31J/mol.K.
Gọi V là thể tích của bình và pn là áp suất gây nổ.
Đối với khí nitơ ta có: p n V = m N μ N R T N (1)
Đối với khí hiđrô ta có: p n 5 V = m H μ H R T H (2)
Từ (1) và (2) ⇒ m H = m N . T N . μ H 5. T H . μ N = 27 , 55 g
Một bình có dung tích V = 10 lít chứa một lượng khí hiđrô bị nén ở áp suất p = 50atm và nhiệt độ 70. Khi nung nóng bình, do bình hở nên có một phần khí thoát ra; phần khí còn lại có nhiệt độ 170C và vẫn dưới áp suất như cũ. Tính khối lượng khí đã thoát ra.
Gọi m1, m2 là khối lượng khí trong bình trước và sau khi nung nóng bình. Áp dụng phương trình Menđêlêep – Clapêrôn ta có:
p V = m 1 μ R T 1 , p V = m 2 μ R T 2 . ⇒ m 2 − m 1 = p V μ R ( 1 T 1 − 1 T 2 )
Với p = 50atm, V = 10 lít, μ = 2 g
R = 0 , 082 ( a t m . l / m o l . K ) Mà T 1 = 273 + 7 = 280 K ; T 2 = 273 + 17 = 290 K
⇒ m 2 − m 1 = 50.10.2 0 , 082 ( 1 280 − 1 290 ) m 2 - m 1 = 1 , 502 ( g )
Một bình hình trụ đặt thẳng đứng có dung tích 8 lít và đường kính trong 20 cm, được đậy kín bằng một nắp có khối lượng 2 kg. Trong bình chứa khí ở nhiệt độ 100 ° C dưới áp suất bằng áp suất khí quyển ( 10 5 N/ m 2 ). Khi nhiệt độ trong bình giảm xuống còn 20 ° C thì: Áp suất khí trong bình bằng bao nhiêu?
Xét lượng khí trong bình.
Trạng thái đầu: V 1 = 8 lít; T 1 = 100 + 273 = 373 K ; p 1 = 10 5 N/ m 2
Trạng thái cuối: V 2 = 8 lít; T 2 = 20 + 273 = 293 K; p 2 = ?
Vì thể tích không đổi nên:
p 1 / T 1 = p 2 / T 2 ⇒ p 2 = p 1 T 2 / T 1 = 7,86. 10 4 N/ m 2