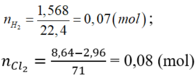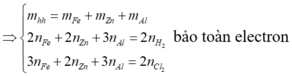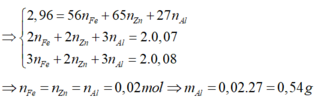hòa tan 11.9 gam hỗn hợp gồm Zn va Al trong dd hcl loãng dư Sau khi pứng xảy ra thu dc 40.3 gam muối tính khối lượng cua al va zn

Những câu hỏi liên quan
BT1. cho hỗn hợp A gồm 24,9 gam Al và Zn tác dụng HCl dư . sau phản ứng thu đc 13,44 lít H2 (đktc) . tính :
a) khối lượng muối thu đc
b) phần trăm khối lượng mỗi khối lượng trong hỗn hợp A?
giải giúp mik va ạk
2Al+6HCl->2AlCl3+3H2
x-----------------x---------\(\dfrac{3}{2}\)x
Zn+2HCl->ZnCl2+H2
y---------------y--------y
Ta có :
\(\left\{{}\begin{matrix}27x+65y=24,9\\\dfrac{3}{2}x+y=0,6\end{matrix}\right.\)
=>x=0,2 mol ,y=0,3 mol
=>m AlCl3= 0,2.133,5=26,7g
=>m ZnCl2 =0,3.136=40,8g
=>%mAl=\(\dfrac{0,2.27}{24,9}.100\)=21,69%
=>%m Zn=78,31%
Đúng 2
Bình luận (4)
Một hỗn hợp X gồm (Al, Fe, Zn) có tổng khối lượng là 20,4 gam. Hòa tan X trong dung dịch HNO, loãng, nóng, dư thu được hỗn hợp khí Y gồm (0,05 mol N2: 0,075 mol N2O) và dung dịch G ( không chứa muối NH4NO3). Biết các phản ứng hóa học xảy ra hoàn toàn. Tổng khối lượng muối trong dung dịch G là
\(m_{Muối}=m_{kl}+m_{NO_3-}=20.4+62\cdot\left(0.05\cdot10+0.075\cdot8\right)=88.6\left(g\right)\)
Đúng 1
Bình luận (0)
Hoà tan 9,2 gam hỗn hợp X gồm Zn và AL vào 200 gam dd HCL dư thu được 0,5 gam khí.
a. Tìm phần trăm khối lượng các chất có trong hỗn hợp ban đầu.
b. Tính nồng độ phần trăm của dd HCL
a) Gọi số mol Zn, Al là a,b (mol)
=> 65a + 27b = 9,2 (1)
\(n_{H_2}=\dfrac{0,5}{2}=0,25\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
a---->2a-------------->a
2Al + 6HCl --> 2AlCl3 + 3H2
b----->3b--------------->1,5b
=> a + 1,5b = 0,25 (2)
(1)(2) => a = 0,1 (mol); b = 0,1 (mol)
=> \(\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{0,1.65}{9,2}.100\%=70,65\%\\\%m_{Al}=\dfrac{0,1.27}{9,2}.100\%=29,35\%\end{matrix}\right.\)
b) nHCl = 2a + 3b = 0,5 (mol)
=> \(C\%_{dd.HCl}=\dfrac{0,5.36,5}{200}.100\%=9,125\%\)
Đúng 2
Bình luận (0)
Chia 31,2g hỗn hợp X gồm Cr, Zn, Ni, Al thành 2 phần bằng nhau. Hòa tan hết phần 1 trong lượng dư HCl loãng nóng thu được 7,281 H2. Cho phần 2 tác dụng với khí Cl2 dư đốt nóng thu được 42,225 gam muối Clorua. Phần trăm khối lượng của Crom trong hỗn hợp là: A.26,04% B. 66,67% C. 33,33% D. 39,07%
Đọc tiếp
Chia 31,2g hỗn hợp X gồm Cr, Zn, Ni, Al thành 2 phần bằng nhau.
Hòa tan hết phần 1 trong lượng dư HCl loãng nóng thu được 7,281 H2.
Cho phần 2 tác dụng với khí Cl2 dư đốt nóng thu được 42,225 gam muối Clorua.
Phần trăm khối lượng của Crom trong hỗn hợp là:
A.26,04%
B. 66,67%
C. 33,33%
D. 39,07%
Đáp án C:
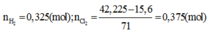
Tác dụng vói HCl: Cr, Zn, Ni tạo muối (II).
Ta gọi R là công thức chung của 2 kim loại Zn và Ni
Gọi x, y, z lần lượt là số mol của R, Al và Cr.
Bảo toàn electron ta có: ne cho= ne nhận
![]()
Tác dụng với Cl2 Zn và Ni tạo muối (II)
Bảo toàn electron ta có: necho = ne nhận
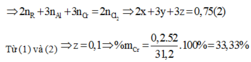
Đúng 0
Bình luận (0)
cho 4 gam hỗn hợp gồm 2 kim loại Zn ,Al tác dụng với dd HCL loãng dư thì thu được 3808ml (đktc).tính khối lượng từng kim loại trong hỗn hợp ban đầu
Zn+2HCl->ZnCl2+H2
x-------------------------x mol
2Al+6HCl->2AlCl3+3H2
y----------------------------3\2 y mol
=> ta có :
65x+27y=4
x+3\2y=0,17
=>x=0,02mol
y=0,1 mol
=>%m Zn=0,02.65\4 100=32,5%
=>%m Al=67,5%
Đúng 1
Bình luận (0)
hòa tan hoàn toàn 11.9 gam hỗn hợp gồm Al và Zn bằng dung dịch HCl 0.8M,sau phản ứng thu được 8.96 lít khí (đktc)
a. tính thành phần % khối lượng mỗi kim loại trong hỗn hợp đầu'
b. tính thể tích dung dịch HCl cần dùng để hòa tan hết hỗn hợp 2 kim loại trên
Hòa tan hoàn toàn m gam hỗn hợp A gồm Mg, Zn, Al trong dung dịch HSO4 dư thu dược m1 gam muối và 10,08 lít khí ở đkc. Nếu dem m gam A phản ứng với oxi thu được hỗn hợp B gồm các oxitvà kim loại dư . Hòa tan B trong dung dịch HCl loãng dư thu được m2 gam muối. Giá trị của m1-m2 gần với giả trị nào nhất A. 15,2 B. 14,5 C. 16,8 D. 11,4
Hòa tan hỗn hợp Zn và Al tác dụng vs dd HCl thu được dd X và 8,96 lít khí thoát ra (đktc). Cô cạn dd X thu đc 40,3 gam muối khan, tính %khối lượng các kim loại
\(n_{Zn}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(n_{H_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+H_2\)
\(n_{H_2}=a+1.5b=0.4\left(mol\right)\left(1\right)\)
\(m_{Muối}=m_{ZnCl_2}+m_{AlCl_3}=136a+133.5b=40.3\left(g\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.2\)
\(m_{hh}=0.1\cdot65+0.2\cdot27=11.9\left(g\right)\)
\(\%Zn=\dfrac{0.1\cdot65}{11.9}\cdot100\%=54.62\%\)
\(\%Al=100-54.62=45.38\%\)
Đúng 2
Bình luận (1)
Đốt cháy 34,44 g hỗn hợp kl gồm Mg,Zn,Al trong không khí, sau pứng thu đc 48,84 g chất rắn A. Hòa tan chất rắn A trong dd Hcl vừa đủ thu đc đ B và 4,032 l khí Hidro(đktc). Cô cạn dd B thu đc bao nhiêu gam muối khan
Bảo toàn khối lượng
\(m_{O_2}=m_{Oxit}-m_{KL}=48,84-34,44=14,4g\)
\(\rightarrow n_{O_2}=\frac{14,4}{32}=0,45mol\)
BTNT (O) \(n_{H_2O}=2n_{O_2}=0,9mol\)
\(n_{H_2}=\frac{4,032}{22,4}=0,18mol\)
BTNT (H) \(n_{HCl}=2n_{H_2O}+2n_{H_2}=2,16mol\)
\(\rightarrow m_{HCl}=2,16.36,5=78,84g\)
\(m_{H_2}=0,18.2=0,36g\) và \(m_{H_2O}=0,9.18=16,2g\)
Bảo toàn khối lượng \(m_A+m_{HCl}=m_{\text{muối}}+m_{H_2O}+m_{H_2}\)
\(\rightarrow m_{\text{muối}}=48,84+78,84-0,36-16,2=111,12g\)
Hòa tan hoàn toàn 2,96 gam hỗn hợp X gồm Fe, Zn, Al bằng dung dịch HCl dư, thu được 1,568 lít khí
H
2
(đktc). Mặt khác, cho 2,96 gam X phản ứng hoàn toàn với khí
C
l
2
dư, thu được 8,64 gam muối. Khối lượng Al trong 2,96 gam X là A. 0,54 gam. B. 0,81 gam. C. 0,27 gam. D. 1,08 gam.
Đọc tiếp
Hòa tan hoàn toàn 2,96 gam hỗn hợp X gồm Fe, Zn, Al bằng dung dịch HCl dư, thu được 1,568 lít khí H 2 (đktc). Mặt khác, cho 2,96 gam X phản ứng hoàn toàn với khí C l 2 dư, thu được 8,64 gam muối. Khối lượng Al trong 2,96 gam X là
A. 0,54 gam.
B. 0,81 gam.
C. 0,27 gam.
D. 1,08 gam.