Cốc A đựng 0,3mol Na2CO3 và 0,2mol NaHCO3. Cốc B đựng 0,4mol HCl. Đổ rất từ từ cốc B vào cốc A, số mol khí thoát ra có giá trị là

Những câu hỏi liên quan
Có hai cốc, cốc A đựng dung dịch chứa 0,3 mol Na2CO3, cốc B đựng dung dịch chứa 0,5 mol HCl. Tiến hành thí nghiệm như sau:
- Thí nghiệm 1: đổ rất từ từ cốc B vào A.
- Thí nghiệm 2: đổ rất từ từ cốc A vào B.
Tính thể tích(đktc) thoát ra khi đổ hết cốc này vào cốc kia.
Ở thí nghiệm 1:
Phản ứng xảy ra như sau :
H+ + (CO3)2- --- > (HCO3)- (1)
0,1-------0,1----------------0,1
Sau khi hết (CO3)2- thì H+ dư phản ứng tiếp (HCO3)-
H+ + (HCO3)- ---- > CO2 + H2O (2)
0,3--------0,3-------------0,3
Vậy thể tích CO2 = 0,3. 22,4 = 6,72 lit
Ở TN3 khi trộn hai dung dịch cùng lúc thì cũng xảy ra
Thứ tự phản ứng như trên (do tốc độ của phản ứng (1)
Lớn hơn rất nhìu tốc độ phản ứng (2))
Vậy thể tích CO2 = 6,72 lit
TN2 : Cho từ từ A vào B
Ta chia nhỏ dung dịch A thành 10 phần. Vậy mỗi phần
Có 0,01 mol Na2CO3 và 0,03 mol NaHCO3.
Cho 1 phần trên vào dung dịch HCl thì H+ dư nên xảy ra
Đồng thời 2 phản ứng :
2H+ + (CO3)2- --- > CO2
0,02-------0,01------------0,01
H+ + (HCO3)- ---- > CO2 + H2O
0,03------0,03------------0,03
ở đây ta lưu ý là H+ sẽ không đủ để tác dụng với ddA
Vậy ta thấy :
cứ 0,05 mol H+ tạo 0,04 mol CO2
nên 0,4 mol H+ tạo 0,32 mol CO2 (tam suất)
vậy thể tích CO2 = 0,32. 22,4 = 7,168 lit CO2
Đúng 0
Bình luận (0)
Ba cốc nước thủy tinh giống nhau ban dầu cốc Á đựng nước đá cốc B đựng nước nguội cốc C đựng nước nóng đổ hết ra và rót nước sôi vào cả 3 cốc . Cốc nào dễ vỡ nhất
Cốc A vì Vận dụng sự nở vì nhiệt của các chất: Các chất rắn, lỏng và khí nở ra khi nóng lên và co lại khi lạnh đi
Đúng 1
Bình luận (1)
Cốc A dễ vỡ nhất vì cốc A đựng nước đá nên thủy tinh đang co lại nhiều nhất trong các cốc, khi bị đổ nước sôi vào sẽ bị dãn nở đột ngột làm cốc bị nứt vỡ
*TK.
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Trong một cái cốc đựng muối cacbonat của kim loại hóa trị I. Thêm từ từ dung dịch H2SO4 10% vào cốc cho đến khi khí vừa thoát ra hết thu được dung dịch muối sunfat nồng độ 13,63%. Kim loại hóa trị I là:
A. Li
B. Na
C. K
D. Ag
Đáp án B
Đặt công thức muối cacbonat kim loại là M2CO3
M2CO3+ H2SO4 → M2SO4 + CO2+ H2O
Giả sử n M 2 C O 3 = 1 mol
→ n H 2 S O 4 = n M 2 S O 4 = n C O 2 = 1mol
→ m H 2 S O 4 = 98 gam; m M 2 S O 4 = 2M+96 gam;
m C O 2 = 44 gam; m d d H 2 S O 4 10 % =980 g
Ta có: mdd sau pứ = m M 2 C O 3 + m d d H 2 S O 4 - m C O 2
=2M + 60+980-44= 2M+996 (gam)
C % M 2 S O 4 = 2 M + 96 2 M + 996 . 100 % = 13 , 63 % → M = 23 → M l à N a
Đúng 0
Bình luận (0)
Ba cốc thuỷ tinh giống nhau, ban đầu cốc A đựng nước đá, cốc B đựng nước nguội (ở nhiệt độ phòng), cốc C đựng nước nóng. Đổ hết nước và rót nước sôi vào cả ba cốc. Cốc nào dễ vỡ nhất?
A. Cốc A dễ vỡ nhất
B. Cốc B dễ vỡ nhất
C. Cốc C dễ vỡ nhất
D. Không có cốc nào dễ vỡ
Đáp án A
Ba cốc thuỷ tinh giống nhau, ban đầu cốc A đựng nước đá, cốc B đựng nước nguội (ở nhiệt độ phòng), cốc C đựng nước nóng.
Đổ hết nước và rót nước sôi vào cả ba cốc, khi đó cốc A dễ vỡ nhất
Vì: Ban đầu nhiệt độ ở cốc A thấp nhất (cốc thủy tinh đang ở trạng thái co lại) khi đổ nước đá ra và rót nước nóng vào thì nhiệt độ ở cốc A tăng lên (sẽ nở ra) thay đổi quá nhanh ⇒ nên dễ vỡ nhất
Đúng 0
Bình luận (0)
Ba cốc thủy tinh giống nhau, ban đầu cốc A đựng nước đá, cốc B đựng nước nguội (ở nhiệt độ phòng), cốc C đựng nước nóng. Đổ hết nước và rót nước sôi vào cả ba cốc. Cốc nào dễ vỡ nhất? A. Cốc A dễ vỡ nhất B. Cốc B dễ vỡ nhất C. Cốc C dễ vỡ nhất D. Không có cốc nào dễ vỡ cả
Đọc tiếp
Ba cốc thủy tinh giống nhau, ban đầu cốc A đựng nước đá, cốc B đựng nước nguội (ở nhiệt độ phòng), cốc C đựng nước nóng. Đổ hết nước và rót nước sôi vào cả ba cốc. Cốc nào dễ vỡ nhất?
A. Cốc A dễ vỡ nhất
B. Cốc B dễ vỡ nhất
C. Cốc C dễ vỡ nhất
D. Không có cốc nào dễ vỡ cả
Đặt cốc A đựng dd H2SO4 và cốc B đựng dd HCl vào 2 đĩa cân sao cho cân ở vị trí thăng bằng. Cho m g Fe vào cốc đựng dd H2SO4 . Cho 5,4 g nhôm vào cốc đựng dd HCl
Trong một cái cốc đựng một muối cacbonat của kim I loại hoá trị. Thêm từ từ dung dịch H2SO4 10% vào cốc cho đến khi khí vừa thoát ra hết thu được dung dịch muối sunfat nồng độ 13,63%. Kim loại hoá trị I là A. Li. B. Na. C. K. D. Ag.
Đọc tiếp
Trong một cái cốc đựng một muối cacbonat của kim I loại hoá trị. Thêm từ từ dung dịch H2SO4 10% vào cốc cho đến khi khí vừa thoát ra hết thu được dung dịch muối sunfat nồng độ 13,63%. Kim loại hoá trị I là
A. Li.
B. Na.
C. K.
D. Ag.
Đáp án B
Giả sử

khối lượng dung dịch sau phản ứng:
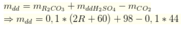
![]()
![]()
Đúng 0
Bình luận (0)
Cho từ từ đến hết 150ml dung dịch NaOH 2M vào một cốc đựng 100ml dung dịch AlCl3 nồng độ x mol/l, sau khi phản ứng hoàn toàn thấy trong cốc có 0,1 mol chất kết tủa. Thêm tiếp 100ml dung dịch NaOH 2M vào cốc, sau khi phản ứng hoàn toàn thấy trong cốc có 0,14 mol chất kết tủa. Giá trị của x là: A. 1,6 B. 1,0 C. 0,8 D. 2,0
Đọc tiếp
Cho từ từ đến hết 150ml dung dịch NaOH 2M vào một cốc đựng 100ml dung dịch AlCl3 nồng độ x mol/l, sau khi phản ứng hoàn toàn thấy trong cốc có 0,1 mol chất kết tủa. Thêm tiếp 100ml dung dịch NaOH 2M vào cốc, sau khi phản ứng hoàn toàn thấy trong cốc có 0,14 mol chất kết tủa. Giá trị của x là:
A. 1,6
B. 1,0
C. 0,8
D. 2,0
Ta thấy tỉ lệ số mol NaOH và số mol kết tủa không bằng nhau
Như vậy, phản ứng đầu chưa có kết tủa bị tan, ở phản ứng sau có kết tủa bị hòa tan
Phản ứng sau:
⇒
n
A
l
(
O
H
)
4
-
=
0
,
25
.
2
-
0
,
14
.
3
4
=
0
,
02
⇒
n
A
l
C
l
3
=
0
,
02
+
0
,
14
=
0
,
16
⇒
x
=
1
,
6
Đáp án A
Đúng 0
Bình luận (0)
Trên một cân có 2 đĩa đặt 2 cốc a và b sao cho cân thăng bằng cho 26 g Zn vào cốc a đựng dung dịch HCl Cho m gam Al vào cốc B đựng dung dịch H2 SO4 loãng khi cả Zn và Al đều tan hết thấy cân ở vị trí thăng bằng Tính giá trị m
- Xét cốc A
\(n_{Zn}=\dfrac{26}{65}=0,4\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,4-------------------->0,4
=> \(m_{tăng}=26-0,4.2=25,2\left(g\right)\) (1)
- Xét cốc B
\(n_{Al}=\dfrac{m}{27}\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
\(\dfrac{m}{27}\)--------------------------->\(\dfrac{m}{18}\)
=> \(m_{tăng}=m-\dfrac{m}{18}.2=\dfrac{8}{9}m\left(g\right)\) (2)
(1)(2) => \(\dfrac{8}{9}m=25,2\)
=> m = 28,35 (g)
Đúng 3
Bình luận (0)




















